Попри значні досягнення в галузі діагностики та лікування захворювань органів дихання, на початку ХХІ століття вони продовжують поширюватися. У зв’язку з цим видано накази МОЗ України, в яких затверджено інструкцію щодо діагностики, клінічної класифікації та лікування хронічних обструктивних захворювань легень, бронхіальної астми тощо. Матеріали наказів відображено у розділі підручника.
Визначення. Пневмонія — гостре інфекційне захворювання переважно бактеріальної етіології, яке характеризується вогнищевим ураженням респіраторних відділів легень та обов’язковою наявністю внутрішньоальвеолярної ексудації.
Терміни «гостра пневмонія» та «хронічна пневмонія» застарілі і нині не використовуються. Щороку в США реєструють 4 млн хворих на госпітальну пневмонію; 600 тис. із них потребують госпіталізації. Смертність від негоспітальної пневмонії (НП) в амбулаторних хворих становить 1–5%, у стаціонарних — понад 25% випадків.
Етіологія. У розвитку пневмоній велике значення мають такі чинники:
І. Бактеріальна інфекція:
1) грампозитивна флора (пневмокок, стрептокок, стафілокок);
2) грамнегативна флора (гемофільна паличка, паличка Фрідлендера, ентеробактерії, кишкова паличка, протей, псевдомонас).
ІІ. Атипова флора (мікоплазма, хламідії, легіонела).
ІІІ. Вірусна інфекція (віруси грипу, парагрипу, герпесу).
IV. Грибкова інфекція.
Таблиця 3.1. Класифікація пневмонії
| НП | Госпітальна пневмонія |
| 1. НП у пацієнтів без виражених порушень імунітету.
2. НП у пацієнтів із вираженими порушеннями імунітету: а) із синдромом набутого імунодефіциту (ВІЛ/СНІД); б) з іншими захворюваннями/патологічними станами. 3. Негоспітальна аспіраційна пневмонія |
1. Власне госпітальна пневмонія.
2. Вентилятор-асоційована пневмонія. 3. Госпітальна пневмонія у пацієнтів із вираженими порушеннями імунітету: а) у реципієнтів донорських органів; б) у пацієнтів, що отримують цитостатичну терапію. 4. Госпітальна аспіраційна пневмонія |
3.1.1. Негоспітальна пневмонія
Визначення. Під НП слід розуміти гостре захворювання, що виникло в позалікарняних умовах (за межами стаціонару або пізніше 4 тиж після виписки із нього чи було діагностовано в перші 48 год від моменту госпіталізації) та супроводжується симптомами інфекції нижніх дихальних шляхів (лихоманка; кашель; виділення мокротиння, можливо гнійного; біль у грудях; задишка) і рентгенологічними ознаками нових вогнищево-інфільтративних змін у легенях за відсутності очевидної діагностичної альтернативи.
Етіологічні особливості пневмонії:
- З-поміж численних мікроорганізмів (понад 100 видів) тільки деякі з підвищеною вірулентністю здатні при потраплянні у нижні дихальні шляхи спричиняти запальний процес. Відомо, що мікробіологічна ідентифікація збудників можлива тільки в 40–60% випадків, що доведено в 41 проспективному дослідженні.
- S. pneumoniaе є основною причиною позалікарняних пневмоній і спричиняє захворювання у 30–70% випадків.
- Друге місце серед причин посідають «атипові» мікроорганізми — Mycoplasma pneumoniaе та Chlamіdophila pneumoniae (10–20% випадків). У 30–40% випадків визначається поєднання типових і атипових збудників.
- Третє місце посідають Staphylococcus aureus, Legionella pneumoniaе і грамнегативні бактерії (Klebsiella pneumoniae, Pseudomonas aeuruginosa тощо), які відіграють велику роль у розвитку позалікарняних пневмоній. Legionella spp. зустрічається здебільшого в країнах з теплим кліматом (Середземномор’я) і рідко — в країнах Північної Європи.
- Роль анаеробів у розвитку НП незначна, але вона помітно зростає при аспіраційних пневмоніях (50%).
- Вірусні пневмонії становлять 5–15% випадків захворювання.
Більш детальну епідеміологічну характеристику та фактори ризику НП наведено в табл. 3.2.
Таблиця 3.2. Епідеміологія та фактори ризику розвитку НП відомої етіології
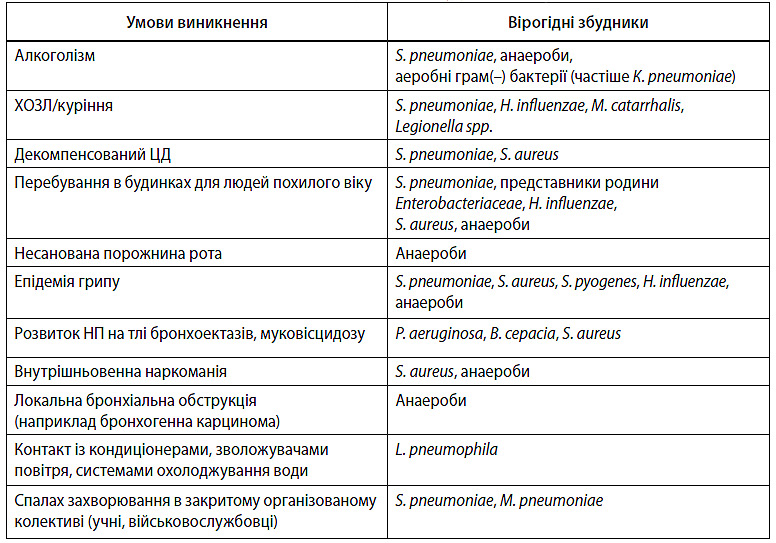
Таблиця 3.3. Групи хворих на НП та ймовірні збудники захворювання
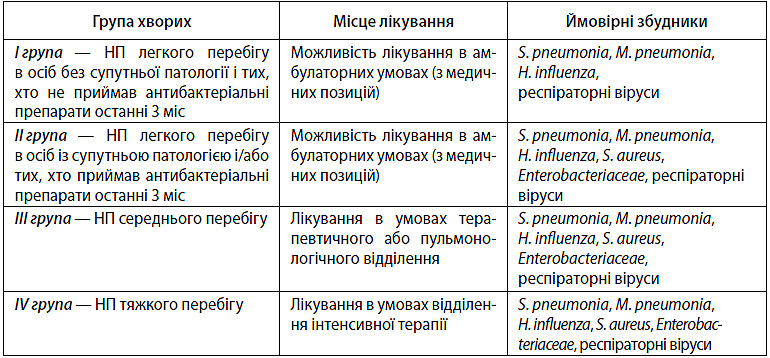
У хворих на НП найбільш характерними збудниками є анаеробні бактерії та представники родини Enterobacterisceae. Слід пам’ятати, що захворювання може спричинятися новими, раніше не відомими збудниками. До них належать коронавірус, асоційований із тяжким гострим респіраторним синдромом, вірус пташиного і свинячого грипу, метапневмовірус та ін. Водночас деякі мікроорганізми не спричиняють розвиток бронхолегеневого запалення. До таких мікроорганізмів належать A. viridans, S. epidemidis та інші коагулазонегативні стафілококи: Enterococcus spp.; Neisseria spp.
Усім хворим із пневмонією, госпіталізованим до стаціонару, рекомендоване проведення бактеріологічного дослідження крові (забір крові здійснюється з двох різних вен до початку антибактеріальної терапії). Тривалість досліджень коливається від 1 до 3 тиж.
Патогенез. Виникнення, розвиток, перебіг і наслідки пневмонії залежать від вірулентних властивостей збудника і ступеня імунної реакції макроорганізму на інфекцію [35, 36].
Основні патогенетичні ланки розвитку пневмонії:
1. Проникнення збудника пневмонії до легеневої тканини: інгаляційним, бронхогенним, гематогенним та лімфогенним шляхами.
2. Зміни системи місцевого бронхолегеневого захисту: мукоциліарного транспорту, бронхолегеневої імунної системи, факторів неспецифічної резистентності (лізоцим, лактоферин, β-лізин, ІgA, інтерферон; сурфактантна система).
3. Розвиток під впливом інфекції локального запального процесу і його поширення по легеневій тканині, що залежить від виду збудника.
4. Сенсибілізація до інфекційних агентів і розвиток гіперергічної, нормо- або гіпоалергічної реакції, формування імунних комплексів, їх взаємодія з комплементом, виділення медіаторів запалення.
5. Підвищення агрегації тромбоцитів, порушення в системі мікроциркуляції.
6. Нервово-трофічні порушення бронхів і легень.
7. Посилення окиснення ліпідів клітинних мембран, активація ендогенних фосфоліпаз, зниження впливу антиоксидантів, що призводить до пошкодження структури і порушення функції мембран клітин.
Групи хворих на НП:
І група — пневмонія у хворих віком до 60 років без супутньої патології, з легким перебігом захворювання, лікування в амбулаторних умовах, хто не приймав за останні 3 міс антибактеріальні препарати;
ІІ група — пневмонія легкого перебігу у хворих із супутньою патологією або віком до 60 років і більше за можливості амбулаторного лікування і/або тих, хто приймав за останні 3 міс антибактеріальні препарати;
ІІІ група — середньотяжка пневмонія, яка вимагає госпіталізації, але без застосування інтенсивної терапії;
IV група — пневмонія тяжкого перебігу; необхідна інтенсивна терапія у стаціонарі.
З метою встановлення етіології НП виконують бактеріоскопію пофарбованого за Грамом мазка мокротиння та культуральне дослідження мокротиння. Таке дослідження є обов’язковим у стаціонарі і необов’язковим в амбулаторних умовах. У пацієнтів з тяжким перебігом НП доцільним є мікробіологічне дослідження крові. Матеріал для дослідження необхідно забирати до початку антибактеріальної терапії. Чутливість методів бактеріологічного дослідження обмежена, оскільки етіологію НП не вдається встановити у 25–60% пацієнтів.
Оцінка тяжкості перебігу НП та вибір місця лікування
Сучасні показання до госпіталізації базуються на низці відомих клініко-лабораторних шкал PORT (Pneumonia Patient Outcomes Research Team). Використання зазначених шкал потребує відповідного рівня лабораторної діагностики у лікарні; вони доступні у переважній більшості медичних закладів.
Більш простою та доступною для рутинного застосування в амбулаторних умовах є прогностична шкала CRB-65. В її основі лежать модифікована шкала Британського торакального товариства, в якій передбачена оцінка 4 параметрів: віку, порушень свідомості, частоти дихання, рівня САД та ДАТ. Виходячи з вірогідності летального наслідку, пацієнтів розподіляють на 3 групи. Кожна з них відповідає тяжкості перебігу захворювання і для кожної рекомендують відповідне місце лікування (алгоритм 3.1). Мінімальна кількість балів за цією шкалою становить 0; максимальна — 4. Пацієнти, які набирають більше 1 бала, повинні лікуватися в стаціонарних умовах. Шкала CRB-65 досить проста у використанні, тому її можна застосовувати як скринінг у хворих в амбулаторних умовах.
| Алгоритм 3.1. Шкала CRB-65 оцінки ризику несприятливого наслідку та вибору місця лікування НП
Симптоми і ознаки (1 бал за наявність кожного з наведених симптомів та ознак):
Примітки. *Для осіб віком понад 65 років. ВІТ — відділення інтенсивної терапії. |
Обмеження шкали:
- не враховує важливі показники, які характеризують легеневу недостатність (ЛН) (наприклад рівень оксигенації);
- не враховує декомпенсацію супутньої патології внаслідок позалікарняної пневмонії;
- не враховує соціальні фактори та супутні захворювання;
- невисока інформативність при визначенні прогнозу у пацієнтів похилого віку.
Фактори, що зумовлюють тяжкість перебігу НП:
- Вік понад 65 років.
- Неефективність стартової антибактеріальної терапії.
- Наявність супутніх захворювань (ХОЗЛ, бронхоектази, злоякісне новоутворення, ЦД, хронічна ниркова або печінкова недостатність, застійна СН, хронічний алкоголізм, наркоманія, цереброваскулярні захворювання та ін.).
- Вагітність.
- Бажання пацієнта та/або членів його родини.
Приклад формулювання діагнозу:
НП правої легені, сегмента S6, І група, ЛН І ступеня.
Клінічні ознаки пневмонії наведено в алгоритмі 3.2.
Алгоритм 3.2. Діагностика пневмонії [8]
|
Найбільш ефективними для визначення показань до направлення у відділення реанімації та інтенсивної терапії є рекомендації IDSA/ATS (Infectious Diseases Society of America (Американське товариство інфекційних хвороб)/American Thoracic Society (Американське торакальне товариство)). Критерії IDSA/ATS засновані на використанні двох «великих» і дев’яти «малих» критеріїв тяжкості НП. Наявність одного «великого» або трьох «малих» критеріїв є показанням до госпіталізації пацієнта до відділення реанімації та інтенсивної терапії.
Таблиця 3.4. Критерії тяжкості НП за IDSA/ATS
| «Великі» критерії | «Малі» критерії |
|
|
Примітка. До малих критеріїв можуть зараховуватися додаткові критерії — гіпоглікемія (у пацієнтів без ЦД), гіпонатріємія, не зумовлений іншими причинами метаболічний ацидоз/підвищення рівня лактату, цироз, аспленія, передозування/різке припинення вживання алкоголю у залежних пацієнтів.
Мікробіологічне дослідження виявляє у мазках значну кількість грампозитивних і грамнегативних мікроорганізмів. Досліджують також посів мокротиння на чутливість до антибіотиків. Європейський консенсус рекомендує усім госпіталізованим хворим визначати рівень СРБ.
Розрізняють пневмонії з нетяжким і тяжким перебігом.
Пневмонії з тяжким перебігом — це особлива форма захворювання, що може мати різну етіологію і проявляється тяжким інтоксикаційним синдромом, гемодинамічними змінами, вираженою ЛН та/або ознаками тяжкого сепсису чи септичного шоку. Захворювання характеризується несприятливим прогнозом та потребує інтенсивного лікування.
Особливості клінічної діагностики та перебігу окремих форм НП:
1. Стафілококова пневмонія характеризується деструктивним ураженням легень з утворенням окремих порожнин (бул). Розрізняють такі форми стафілококової пневмонії: первинна (бронхогенна); метастатична (стафілококова) деструкція легень; абсцедуюча; легенево-плевральна; інфільтративно-бульозна. Початок захворювання гострий: температура тіла підвищується до високих позначок, спостерігаються озноб, кашель з виділенням гнійного або кров’янистого мокротиння, біль у боці, задишка, ціаноз. Пневмонія підтверджується рентгенологічно, а в мокротинні визначають стафілокок.
2. Кандидозна пневмонія характеризується повільним початком з виникненням загальної слабкості, втрати апетиту, підвищеного потовиділення, тривалої субфебрильної температури тіла. При перкусії визначають притуплення; аускультативно — звучні вологі хрипи чи крепітацію. Під час повторного дослідження в мокротинні зростає кількість грибів у динаміці.
3. Легіонельозна пневмонія (хвороба легіонерів) характеризується тяжким перебігом і нагадує тотальну пневмонію. У пацієнтів часто виникають діарея, неврологічна симптоматика, ускладнення: абсцедування, парапневмонічний плеврит, спонтанний піопневмоторакс. Виникає важка інтоксикація, часто спостерігається ІТШ, інтерстиціальний набряк легень, порушення функції печінки. Діагноз встановлюють на основі зростання в 4 рази титру антитіл до легіонели, визначення збудника в мокротинні та бронхіальних змивах.
4. Клебcієла-пневмонія часто виникає у пацієнтів з алкоголізмом, а також у фізично ослаблених людей старечого та похилого віку. Ця пневмонія може бути гострою, затяжною або «повзучою»; починається бурхливо з ознобу, кашлю з виділенням тягучого мокротиння, періодичного чи хвилеподібного підвищення температури тіла. Фізикально спостерігаються притуплення, бронхіальне дихання, вологі звучні хрипи. Рентгенологічно визначають затемнення. Діагноз підтверджує бактеріологічне дослідження мокротиння.
5. Аспергільозна пневмонія починається гостро з гектичної температури тіла, болю в грудях, кашлю з виділенням мокротиння без запаху, схуднення, анемії. Клінічна картина характерна для абсцедуючої пневмонії. Рентгенологічно визначають абсцедуючу форму пневмонії. З різних причин пневмонія може мати затяжний характер з подовженим перебігом; для такої пневмонії характерними є наступні ознаки:
1) тривалість більше 4 тиж;
2) наявність на рентгенограмі вогнищевої та перибронхіальної інфільтрації сегментарної локалізації, яка не розсмоктується протягом 4 тиж;
3) локальний сегментарний бронхіт, який діагностується за допомогою бронхоскопії;
4) збереження лабораторних ознак запального процесу (лейкоцитозу, підвищеної ШОЕ, рівня сіалових кислот, серомукоїду, фібриногену);
5) характерні імунологічні порушення (підвищення в крові ІgA і зниження IgM, С4, С5, С9-компонентів, підвищення активності Т-супресорів, зниження Т-хелперів і кілерів);
6) обов’язкове одужання (клінічне, рентгенологічне і лабораторне) впродовж терміну від 3 міс до 1 року.
Характер рентгенологічних змін залежно від етіології пневмонії наведено в табл. 3.5.
Таблиця 3.5. Характер рентгенологічних змін залежно від етіології пневмонії
| Рентгенологічна картина | Можливий збудник |
| Часткова та багаточасткова інфільтрація | Бактерії (пневмокок, легіонела, анаероби), гриби |
| Вогнищево-зливна двобічна інфільтрація | Вірус грипу, пневмокок, стафілокок, легіонела |
| Негомогенна вогнищева та багатовогнищева інфільтрація | Віруси, стафілококи, мікоплазма |
| Інтерстиціальні зміни | Сальмонела, мікобактерія туберкульозу, гриби |
| Поєднання інфільтративних та інтерстиціальних змін | Віруси, мікоплазми, пневмоцисти |
| Інтерстиціальні зміни у вигляді сітки | Віруси, мікоплазми, пневмококи, хламідії |
| Поєднання інфільтративних чи інтерстиціальних змін з лімфаденопатією | Віруси кору, вітряної віспи, мікобактерії туберкульозу, гриби, мікоплазми, хламідії |
| Множинні перибронхіальні легкодренажні абсцеси | Стафілокок |
| Однакові крупні абсцеси легень | Клебсієла |
Застосування прогностичних шкал для оцінки стану хворого на НП дозволяє знизити частоту необґрунтованої госпіталізації пацієнтів з низьким ризиком несприятливого прогнозу і виділити категорію осіб, яким потрібна інтенсивна терапія. Недоліками цих шкал є оцінка тяжкості стану пацієнта та/або прогнозу в конкретний період без урахування варіабельності клінічної картини НП та можливості швидкого прогресування захворювання, а також недооцінка декомпенсації супутніх хронічних захворювань, які нерідко є основною причиною госпіталізації пацієнта. Таким чином, прогностичні шкали можуть слугувати лише орієнтиром у виборі місця лікування.
Госпіталізація при НП показана за наявності хоча б однієї з наступних ознак:
1. Дані фізикального обстеження: температура тіла <35,5 °С або ≥39,9 °С; ЧСС ≥125/хв; частота дихання ≥30/хв; САТ < 90 мм рт. ст.; ДАТ ≤ 60 мм рт. ст.; порушення свідомості.
2. Лабораторні та рентгенологічні дані: кількість лейкоцитів у периферичній крові <4,0•109/л або >20,0•109/л; SpO2 <92% (за даними пульсоксиметрії), креатинін сироватки крові >180 мкмоль/л чи азот сечовини >7,0 ммоль/л (азот сечовини = сечовина (ммоль/л) : 2,14); пневмонічна інфільтрація, що локалізується більше ніж в одній частці; наявність порожнин розпаду; плевральний випіт; швидке прогресування вогнищево-інфільтративних змін у легенях (збільшення розмірів інфільтрації >50% протягом найближчих 2 діб); гематокрит >30% або гемоглобін <90 г/л; позалегеневі вогнища інфекції (менінгіт, септичний артрит тощо).
Лікування пневмонії залежить від збудника захворювання. У США та багатьох країнах Європи понад 80% хворих на госпітальну пневмонію отримують лікування в амбулаторно-поліклінічних умовах.
Антибактеріальну терапію необхідно починати одразу після встановлення діагнозу, оскільки затримка введення першої дози антибіотика понад 4 год (а за наявності септичного шоку — на 1 год і більше) зумовлює значне підвищення ризику смерті.
Призначення антибіотиків проводять емпірично [18, 34, 45], оскільки наразі не існує достатньо ефективних методів етіологічної експрес-діагностики. Антибіотики поділяють на препарати вибору та альтернативні препарати. Розпочинають лікування НП препаратами вибору, а за неможливості їх призначення (відсутність, непереносимість чи використання впродовж останніх 3 міс з будь-яких причин) або у разі неефективності препаратів вибору протягом 48–72 год лікування здійснюється альтернативними препаратами.
Хворим І та ІІ груп, які госпіталізовані за соціальних обставин, призначають відповідну пероральну антибактеріальну терапію; пацієнтам, що належать до ІІІ та ІV груп, — парентеральну.
У випадку легіонельозної пневмонії ефективним є поєднання макроліда з рифампіцином; альтернативною терапією є фторхінолон ІІІ–ІV покоління.
Лікування НП, спричиненої метицилінрезистентним Staphylococcus aureus (MRSA), із застосуванням β-лактамів, макролідів, респіраторних фторхінолонів є неефективним, оскільки збудник має високу резистентність до цих антибіотиків. Препаратами вибору є глікопептиди (ванкоміцин, тейкопланін) та оксазолідинони (лінезолід).
Застосування антибіотиків при НП систематизовано в табл. 3.6.
Таблиця 3.6. Антибактеріальна терапія НП
| Групи хворих | Імовірні збудники | Препарати вибору | Альтернативні препарати |
| І група
НП з легким перебігом, без супутньої патології та попередньої антибактеріальної терапії за останні 3 міс |
S. pneumoniae, М. pneumoniae, С. pneumoniae, H. іnfluenzaе, респіраторні віруси | Амоксицилін або макролід для перорального прийому | 1. Макролід або доксициклін або фторхінолон ІІІ–ІV покоління перорально за неефективності амінопеніциліну.
2. Амінопеніцилін або фторхінолон ІІІ–ІV покоління за неефективності макроліда |
| ІІ група
НП з легким перебігом із супутньою патологією; і/або пацієнти, які приймали антибактеріальні препарати протягом останніх 3 міс |
S. pneumoniae, H. іnfluenzaе, М. pneumoniae, С. pneumoniae, S. aureus, M. catarrhalis, ентеробактерії, респіраторні віруси |
Амоксицилін/клавуланова кислота або цефуроксиму аксетил перорально | Пероральний прийом: додати до β-лактаму макролід або застосувати монотерапію фторхінолоном ІІІ–ІV покоління |
| ІІІ група
НП з перебігом середньої тяжкості в осіб, що госпіталізовані до терапевтичного відділення |
S. pneumoniae, H. іnfluenzaе, атипові збудники, грамнегативні ентеробактерії, респіраторні віруси |
Парентерельно (в/в, в/м): амінопеніцилін (переважно захищений) + макролід або цефалоспорин ІІІ покоління + макролід (перорально) | В/в: фторхінолон ІІІ–ІV покоління або карбапенем (неактивний щодо синьогнійної палички ертапенем) + макролід (per os), або цефалоспорин V покоління (цефтаролін) + макролід (per os) |
| ІV група
Хворі на НП з тяжким перебігом, госпіталізовані до відділення інтенсивної терапії |
S. pneumoniae, Legionella spp., H. іnfluenzaе, S. aureus, М. pneumoniae, грамнегативні ентеробактерії, Pseudomonas spp., полімікробні асоціації | В/в: захищений амінопеніцилін + макролід або цефалоспорин ІІІ покоління + макролід, або ертапенем + макролід, або цефтаролін + макролід | В/в: фторхінолон ІІІ–ІV покоління + β-лактам |
| У разі підозри на P. aeruginosа: в/в цефалоспорин ІІІ–ІV покоління, активний до P. аeruginosа, + аміноглікозид або ципрофлоксацин (левофлоксацин) | В/в: іміпенем (меропенем, дорипенем) + аміноглікозид або ципрофлоксацин (левофлоксацин) |
Серед можливих причин повільного розсмоктування НП суттєвою є вторинна резистентність збудників до антибіотиків. Факторами ризику антибіотикорезистентності S. pneumoniae є вік понад 65 років, терапія β-лактамами впродовж попередніх 3 міс, алкоголізм, імунодефіцитні захворювання/стани, зокрема прийом системних кортикостероїдів, множинні супутні захворювання внутрішніх органів.
Затяжний перебіг НП
У хворих на НП після 3–5 днів потенційно ефективної антибактеріальної терапії нормалізується температура тіла та регресують інші ознаки захворювання, однак рентгенологічні позитивні зміни, як правило, спостерігаються пізніше. У випадку, коли не вдається досягти повного рентгенологічного розсмоктування вогнищево-інфільтративних змін у легенях до кінця 4-го тижня від початку захворювання, це зумовлено затяжним перебігом захворювання.
До факторів ризику затяжного перебігу захворювання належать:
- вік понад 50 років;
- алкоголізм;
- наявність супутніх інвалідизуючих захворювань внутрішніх органів (ХОЗЛ, застійна СН, ХХН, злоякісна пухлина, ЦД та ін.);
- тяжкий перебіг пневмонії;
- мультичасткова поширеність пневмонічної інфільтрації;
- вірулентні збудники пневмонії (L. pneumophila, S. aureus, грамнегативні ентеробактерії);
- тютюнопаління;
- вторинна бактеріємія;
- клінічна неефективність стартової терапії (зберігаються лейкоцитоз, лихоманка);
- набута антибіотикорезистентність збудника захворювання.
Ускладнення НП [15, 18, 28, 41]
До ускладнень НП належать:
- плевральний випіт (неускладнений і ускладнений);
- емпієма плеври;
- деструкція/абсцедування легеневої тканини;
- гострий респіраторний дистрес-синдром;
- гостра дихальна недостатність;
- ІТШ;
- вторинна бактеріємія, сепсис, гематогенні вогнища відсіву;
- перикардит, міокардит;
- нефрит;
- гнійно-деструктивні зміни в легенях (найбільш тяжке ускладнення).
Останнім часом в усьому світі спостерігається стрімке зростання резистентності збудників пневмонії до антибактеріальних препаратів. Оскільки пневмокок є найбільш поширеним збудником НП, особливе значення має зниження чутливості до нього пеніциліну.
Факторами ризику пеніцилінрезистентності до пневмокока є вік 60–70 років, наявність тяжких соматичних захворювань, часте і тривале лікування антибіотиками, проживання в будинках для людей похилого віку. У таких пацієнтів резистентність до пеніцилінів коливається в межах 5–50%, що залежить від географічного регіону проживання, відбору матеріалу дослідження і перебування пацієнта в стаціонарі [41].
За даними світової літератури, частота розвитку резистентності до лікування є найвищою в Саудівській Аравії — 55,4% випадків. Високий рівень резистентності зареєстрований у країнах Азії (Китай, Гонконг, Південна Корея, Таїланд) — 44,1% випадків. Нижчий рівень резистентності до пневмокока відмічається в країнах Європи (Франція, Німеччина, Італія, Іспанія) — 11,1% випадків; у Південній Америці, Мексиці резистентні штами пеніциліну виділені в 26%; в Бразилії — в 7,9%; у США — в 22,5%; в Росії — в 9% випадків.
В Україні дані стосовно резистентності пневмокока до пеніциліну відсутні, тож варто орієнтуватися на показники країн Європи.
Заходи комплексного лікування тяжких пневмоній [29, 39, 42, 45]:
- Імунозамісна терапія не застосовується, оскільки її ефективність не доведена і не підтверджена РКД. Наразі немає доказів доцільності призначення біогенних стимуляторів, антигістамінних препаратів, вітамінів, імуномодуляторів (за винятком гранулоцитарного колонієстимулювального фактора та IgG для в/в введення), а також тривалого застосування НПЗП, ненаркотичних анальгетиків у хворих на НП. Ефективність та безпека зазначених лікарських засобів не підтверджена результатами РКД, що не дає підстав рекомендувати їх для лікування хворих на НП.
- Дезінтоксикаційна терапія: сольові розчини (фізіологічний, Рінгера тощо) 1000–3000 мл; глюкоза 400–800 мл/добу 5% розчину; неогемодез 400 мл/добу. Розчини вводять в/в під контролем центрального венозного тиску чи діурезу.
- Корекція мікроциркуляторних порушень: гепарин 20 000 ОД/добу, реополіглюкін 400 мл/добу.
- Корекція диспротеїнемії: альбумін 100–200 мл/добу в/в (залежно від показників крові).
- Киснева терапія: кисень через маску, катетери, ШВЛ залежно від ЛН.
- Гормонотерапія: тільки при ІТШ, інфекційно-токсичному ураженні нирок, печінки, міокарда, бронхіальній обструкції. Вводять гідрокортизон у дозі 50–75 мг в/в чи еквівалентні дози інших препаратів ситуаційно, проте слід пам’ятати, що глюкокортикоїди (ГК) знижують захисні властивості організму.
- Бронхолітична терапія застосовується у разі виникнення бронхообструктивного синдрому: комбінацію бета-2-агоністів (сальбутамол або фенотерол) чергують із холінолітиком іпратропію бромідом (2–4 вдихи 4 рази на добу); застосовують відхаркувальні (амброксол — 100 мг/добу, ацетилцистеїн — 600 мг/добу). Відхаркувальні та бронхолітичні засоби при інтенсивній терапії вводять через змішувач при кисневій терапії.
Для лікування негоспітальної та госпітальної пневмонії здебільшого застосовують 5 груп антибіотиків:
1) пеніциліни;
2) цефалоспорини;
3) макроліди;
4) фторхінолони;
5) аміноглікозиди.
Основоположниками антибіотикотерапії є лауреати Нобелівської премії С. Ваксман, А. Флемінг і Р. Майор (див. кольорову вкл., рис. 9).

1. Пеніциліни. У зв’язку з набутою резистентністю до пеніцилінів при пневмоніях застосовують переважно інгібіторзахищені пеніциліни (під впливом клавуланової кислоти, сульбактаму і тазобактаму):
- амоксицилін/клавуланова кислота по 375–625 мг 3 рази на добу або по 1 г 2 рази на добу, або по 1,2 г 3 рази на добу в/в, а в хірургії — по 1,2 г в/в, в/м за 30–60 хв до операції;
- ампіцилін/сульбактам по 1,5 г 3 рази на добу в/в;
- тикарцилін/клавуланова кислота (комбінація антисиньогнійного карбоксипеніциліну тикарциліну з інгібітором β-лактамаз клавулановою кислотою) по 3,2 г 3–4 рази на добу в/в.
2. Цефалоспорини поділяють на 5 поколінь залежно від спектра антимікробної активності.
Цефалоспорини І покоління активні переважно стосовно грампозитивних мікроорганізмів (пневмококи, стафілококи, стрептококи). До них належить цефазолін, який призначається в/м, в/в (струминно та крапельно) по 1–2 г 2 рази на добу; при тяжких інфекціях доза може бути підвищена до 6–8 г за 3–4 введення.
Цефалоспорини ІІ покоління більш активні до грамнегативних бактерій (гемофільна паличка, паличка Фрідлендера, ентерококи, кишкова паличка, протей, псевдомонас, легіонела, хламідії). До цієї групи препаратів належать цефуроксим, який призначають по 0,75–1,5 г 3 рази за добу в/в болюсно або в/м, перед операцією — по 1,5 г за 30–60 хв; цефуроксиму аксетил (по 500 мг 2 рази на добу перорально).
Цефалоспорини ІІІ покоління активні переважно до грамнегативних мікробів та пневмококів/стрептококів (антистафілококова активність невисока). До них належать:
- цефотаксим, який застосовують по 1–2 г 2–3 рази на добу в/м, в/в болюсно;
- цефоперазон (по 1–2 г 2–3 рази на добу) та цефтазидим — активні проти синьогнійної палички;
- цефоперазон/сульбактам по 4 г з інтервалом 12 год в/в;
- цефтріаксон по 1–2 г 1 раз на добу в/в болюсно або в/м (при сечових інфекціях — 1 г, інших — 2 г).
Цефалоспорини ІV покоління поєднують високу активність цефалоспоринів І–ІІ покоління до стафілококів та цефалоспоринів ІІІ покоління стосовно грамнегативних мікроорганізмів. До цієї групи належить цефепім, який призначають по 2 г 2 рази на добу в/в. Він має виражену антисиньогнійну активність.
Цефалоспорини V покоління:
- цефтаролін по 600 мг в/в 2 рази на добу — діє на грампозитивну і грамнегативну флору та на стафілокок;
- цефтобіпрол по 500 мг 3 рази на добу в/в — діє на грампозитивну і грамнегативну флору, основним показанням є інфікування діабетичної стопи.
3. Макроліди використовують з 1952 р. Вони проникають у клітини, де перебувають 5–7 днів, і є ефективним засобом терапії негоспітальної та госпітальної пневмонії за наявності грампозитивних та грамнегативних мікроорганізмів. Добре діють на атипову флору (хламідії, мікоплазми, легіонели). Вони виводяться з жовчю і не спричиняють розвитку дисбактеріозу.
Найчастіше в амбулаторній практиці використовуються такі макроліди:
- азитроміцин — найбільш ефективний, застосовується перорально по 0,5 г на добу в 1-й день, а з 2-го по 5-й день — по 0,25 г 1 раз на добу або по 0,5 г 1 раз на добу 3 дні;
- кларитроміцин по 500 мг 2 рази на добу перорально; в/в по 0,5 г 2 рази на добу впродовж 5 днів;
- спіраміцин по 3 млн ОД 4 рази на добу перорально, в/в впродовж 10 днів;
- еритроміцин по 0,5 г в/в, перорально 2 рази на добу упродовж 7–10 днів.
4. Фторхінолони — це порівняно більш ефективна група антибіотиків, які діють на різні групи мікроорганізмів (табл. 3.7). Їх застосовують при тяжких інфекціях дихальних і сечовивідних шляхів, кишкових інфекціях, сепсисі тощо.
Таблиця 3.7. Класифікація фторхінолонів
| Покоління | Характеристика | Препарати |
| І | Пероральні фторхінолони для лікування інфекції сечовивідних шляхів |
|
| ІІ | Фторхінолони, високоактивні до грамнегативних мікроорганізмів (кишкова паличка тощо) |
|
| ІІІ | Респіраторні фторхінолони, високоактивні до грамнегативних мікроорганізмів |
|
| IV | Респіраторні фторхінолони, високоактивні до грамнегативних, атипових та анаеробних мікроорганізмів, а також туберкульозної палички |
|
Дозування фторхінолонів, які застосовуються в пульмонології:
- левофлоксацин по 500 мг 1–2 рази на добу перорально або в/в протягом 5–7 днів;
- моксифлоксацин по 400 мг на добу перорально або в/в протягом 5 днів;
- ципрофлоксацин по 500 мг 2 рази на добу перорально або по 400 мг 2 рази на добу в/в протягом 7–10 днів;
- офлоксацин по 400 мг 2 рази на добу перорально та по 200 мг 2 рази на добу в/в, всередину протягом 7–10 днів;
- гатифлоксацин по 400 мг в/в або перорально 1 раз на добу. Доведено, що найбільш небезпечною побічною реакцією фторхінолонів є порушення ритму серця: вони здатні подовжувати інтервал Q–T (таку виражену властивість мають спарфлоксацин, гатифлоксацин, левофлоксацин та інші фторхінолони). При їх застосуванні інколи виникають тяжкі шлуночкові аритмії з розвитком ФШ та асистолії. Найбільш безпечним є моксифлоксацин.
5. Аміноглікозиди рідше застосовують для лікування пневмоній, однак вони є досить ефективними препаратами, особливо в комбінаціях з іншими антибіотиками. Але слід пам’ятати, що вони зовсім не діють на пневмокок. З-поміж аміноглікозидів застосовують наступні:
- гентаміцину сульфат (3–5 мг/кг) в/в 1 раз на добу;
- нетилміцин по 4–6 мг/кг в/в 1 раз на добу;
- амікацину сульфат в/в (15 мг/кг 1 раз на добу).
У третьому тисячолітті для лікування позалікарняних інфекцій переважно використовують три групи антимікробних засобів: 1) b-лактами (до них належать також карбапенеми); 2) макроліди; 3) фторхінолони (!).
6. Препарати різних груп:
- ванкоміцин по 1 г в/в з інтервалом 12 год;
- рифампіцин по 0,6–0,9 г 1 раз на добу перорально або 0,5 г в/в через день;
- кліндаміцин по 0,45–0,6 г 3–4 рази на добу в/в, в/м, усередину.
7. Карбапенеми — це β-лактамні антибіотики, які мають найбільш широкий спектр дії як до грампозитивних, так і до грамнегативних мікробів. Їх застосовують при тяжких бактеріальних пневмоніях. Іміпенем з’явився у клінічній практиці в 1986 р., дорипенем — у 2010 р. До цієї групи належать такі препарати:
- меропенем (призначають по 1 г 3 рази на добу в/в, в/м);
- іміпенем/циластатин (по 0,5–1 г 3–4 рази на добу в/в);
- дорипенем (по 0,5 г 3 рази на добу в/в);
- ертапенем (по 1 г 1 раз на добу в/в, в/м).
Варто зауважити, що препарати, які ще кілька років тому були ефективними, нині втрачають свою ефективність внаслідок виникнення резистентності. Саме тому не рекомендується застосовувати β-лактами тим, хто приймав їх впродовж попередніх 3 міс. В Європі зростає резистентність до макролідів [15, 28, 30, 40].
Важливим етапом лікування хворих на НП є призначення антибіотиків спочатку парентерально, а потім перорально (як правило, пероральне застосування антибіотика можливе через 2–4 доби від початку лікування), а також застосування ступеневої терапії (табл. 3.8–3.10).
Таблиця 3.8. Тактика застосування антибактеріальних препаратів для ступеневої терапії НП [8, 39, 42]
| Оптимальний препарат для парентерального (в/в) введення | Оптимальний препарат для перорального прийому | Альтернативний препарат для перорального прийому |
| Фторхінолони | ||
| Ципрофлоксацин | Ципрофлоксацин | Фторхінолони ІІ покоління |
| Левофлоксацин | Левофлоксацин | Фторхінолони ІІІ покоління |
| β-лактами | ||
| Ампіцилін | Амоксицилін | Амоксицилін/клавуланова кислота |
| Амоксицилін/клавуланова кислота | Амоксицилін | Цефуроксиму аксетил |
| Цефалоспорини | ||
| Цефуроксим | Цефуроксиму аксетил | Амоксицилін/ клавуланова кислота або фторхінолони ІІІ–IV поколінь |
| Цефтріаксон або цефотаксим | Цефуроксиму аксетил | Фторхінолони ІІІ–IV поколінь або цефіксим, або цефтибутен |
| Цефтазидим або іміпенем | Цефуроксиму аксетил | Фторхінолони IV покоління |
| Макроліди | ||
| Еритроміцин | Еритроміцин | Азитроміцин або кларитроміцин, або фторхінолони ІІІ–IV поколінь |
| Спіраміцин | Спіраміцин | |
| Тетрацикліни | ||
| Доксициклін | Доксициклін | Азитроміцин або фторхінолони ІІІ покоління |
| Лінкозаміни | ||
| Кліндаміцин | Кліндаміцин | Метронідазол + β-лактам, фторхінолон IV покоління |
Таблиця 3.9. Антибактеріальна терапія при позалікарняній пневмонії (переваги та недоліки)
| Антибіотики | Переваги | Недоліки |
| Амінопеніциліни | Недорогі, безпечні, широко розповсюджені | Розповсюдженість стійких S. рneumoniaе, штамів H. influenzaе, що продукують β-лактамази; відсутність активності проти атипових збудників |
| Захищені амінопеніциліни | Активність проти H. Influenzaе, безпека, добра переносимість | Розповсюдженість стійких S. рneumoniaе, відсутність активності проти атипових збудників |
| Цефалоспорини | Широкий спектр активності in vitro | Низька біодоступність при пероральному застосуванні, розповсюдженість стійких S. рneumoniaе, відсутність активності до атипових збудників |
| Кларитроміцин | 12-годинний інтервал дозування, активність проти атипових збудників | Розповсюдженість стійких S. рneumoniaе, низька активність проти H. іnfluenzaе |
| Доксициклін | Активність проти атипових збудників, 12-годиний інтервал дозування | Розповсюдженість S. рneumoniaе, небажані явища |
| Офлоксацин, ципрофлоксацин | Активність проти атипових збудників, 12-годинний інтервал дозування | Низька антимікробна активність |
Таблиця 3.10. Режими ступеневої терапії абсцедуючої пневмонії
| Режими в/в терапії | Режими пероральної терапії |
| Кліндаміцин по 300–600 мг в/в 2 рази на добу | Кліндаміцин по 300–450 мг 4 рази на добу |
| Амоксицилін/клавуланова кислота 1,2 г 2–3 рази на добу | Амоксицилін/клавуланова кислота по 625 мг 3 рази на добу чи 1 г 2 рази на добу |
| Ампіцилін/сульбактам по 3 г 4 рази на добу | Амоксицилін/клавуланова кислота по 625 мг 3 рази на добу чи 1 г 2 рази на добу |
| Тикарцилін/клавуланова кислота по 3,2 г 3–4 рази на добу | Амоксицилін/клавуланова кислота по 625 мг 3 рази на добу чи 1 г 2 рази на добу |
| Моксифлоксацин по 400 мг 1 раз на добу | Моксифлоксацин по 400 мг 1 раз на добу |
| Левофлоксацин по 500 мг 1–2 рази на добу | Левофлоксацин по 500–750 мг 1 раз на добу |
| Іміпенем по 1000 мг 3–4 рази на добу | Левофлоксацин по 500 мг 1 раз на добу чи моксифлоксацин по 400 мг 1 раз на добу |
| Меропенем по 500 мг 3–4 рази на добу | Левофлоксацин по 500 мг 1 раз на добу чи моксифлоксацин по 400 мг 1 раз на добу |
| Хлорамфенікол 500 мг 4 рази на добу | Хлорамфенікол 500 мг 4 рази на добу |
| Цефоперазон/сульбактам по 1–2 г 2 рази на добу | Амоксицилін/клавуланова кислота по 625 мг 3 рази на добу чи 1 г 2 рази на добу |
| Лінкоміцин по 600 мг 3 рази на добу | Лінкоміцин по 600 мг 3 рази на добу |
За даними рекомендацій Британського торакального товариства, менше половини дорослих осіб, госпіталізованих із тяжкою НП, отримують антибіотики перед госпіталізацією до стаціонару, незважаючи на те, що їх оглядав лікар загальної практики; більшість смертей настає через нетривалий термін після госпіталізації, оскільки відбувається запізніла госпіталізація хворих без застосування антибіотиків. Необхідно підкреслити, що у більшості хворих на НП діагноз повинен бути верифікований до застосування антибіотиків. У Великобританії госпіталізують лише приблизно 20% хворих на НП.
Перехід на пероральний прийом антибіотика відбувається через 3–5 днів парентерального лікування у разі зменшення лихоманки та симптомів інтоксикації.
Патогенетичне лікування хворих на пневмонію слід скеровувати у таких напрямках:
1) покращення дренажної функції бронхів за допомогою відхаркувальних засобів і муколітиків (амброксол, ацетилцистеїн);
2) нормалізація тонусу бронхолегеневих м’язів (теофілін, сальбутамол, фенотерол);
3) корекція мембранних процесів в альвеолоцитах (кверцетин, вітамін Е, полівітаміни + мінерали) [40, 41].
РКД з доказової медицини у пульмонології дозволили встановити наступне:
1. Бета-лактамні антибіотики при НП залишаються препаратами вибору.
2. Лікування НП бета-лактамними антибіотиками, макролідами та фторхінолонами однаково ефективне, якщо оцінку результатів дослідження здійснювати за такими показниками, як клінічне видужування чи смертність (!).
3. При НП пероральне застосування амоксициліну або амоксициліну/клавуланової кислоти більш ефективне, ніж цефалоспоринів.
4. У хворих із легіонельозною пневмонією застосування левофлоксацину призводить до більш вираженого клінічного ефекту порівняно зі старими макролідами.
Критерії достатності антибактеріальної терапії: температура <37,5 °С; відсутність інтоксикації, гнійного мокротиння; частота дихання <20/хв; кількість лейкоцитів <10•109/л; нейтрофільних лейкоцитів — <80%; юні форми — <6%; відсутність негативної динаміки за даними рентгенологічного обстеження легень.
Ступенева антибактеріальна терапія хворих на НП спирається на такі загальні рекомендації:
1) пероральне застосування антибіотика можливе через 2–4 доби від початку в/в лікування при значній позитивній динаміці;
2) перехід від парентерального введення на пероральний прийом слід здійснювати з урахуванням клінічного стану пацієнта.
Критерії ефективності тривалої антибактеріальної терапії:
1. Ефективність застосування антибіотиків оцінюють через 2–3 доби від початку лікування (спостерігається зменшення інтоксикації, нормалізація температури тіла, відсутність ознак ЛН); у випадку позитивної динаміки захворювання лікування продовжують; у разі відсутності ефекту від лікування антибіотик замінюють на інший.
2. У пацієнтів із нетяжким перебігом захворювання антибактеріальну терапію можна завершувати після досягнення стійкої нормалізації температури тіла протягом 3–5 днів (у цілому тривалість лікування становить 7–10 днів).
3. У хворих із тяжким перебігом і невстановленою етіологією пневмонії тривалість терапії антибіотиками становить, як правило, близько 10 днів і більше (у ці терміни зникає лейкоцитоз).
4. При хламідійній пневмонії тривалість антибактеріальної терапії становить 10–14 днів, при стафілококовій пневмонії — 14–21 день, при легіонельозній етіології — 21 день.
5. Тривалий субфебрилітет, імовірно, є не ознакою бактеріальної інфекції, а проявом післяінфекційної астенії.
6. Регрес рентгенологічних змін відбувається повільніше, ніж клінічних показників (тільки в 25% випадків у людей похилого віку з супутніми захворюваннями та ускладненнями повне розсмоктування легеневої інфільтрації спостерігається протягом 1 міс).
7. У хворих із позитивною динамікою захворювання парентеральне введення антибіотиків можна замінити на пероральне з наступною випискою зі стаціонару.
8. Якщо клінічна, лабораторна та рентгенологічна симптоматика пневмонії зберігається тривалий час, необхідно здійснювати диференційну діагностику з такими захворюваннями, як рак легені, туберкульоз, застійна ХСН тощо (табл. 3.11).
Таблиця 3.11. Тривалість антибактеріальної терапії при НП
| Особливості перебігу НП | Тривалість лікування | Ефективність лікування |
| Легкий неускладнений | 3–5 днів (азитроміцин, «респіраторні фторхінолони») | Недостатньо ефективні у пацієнтів похилого віку, з хронічними супутніми захворюваннями, при повільній клінічній відповіді на лікування |
| Легкий та середньо-тяжкий перебіг | 7–10 днів | Лікування може бути завершене після досягнення стійкої нормалізації температури тіла протягом 3–5 днів |
| Тяжкий перебіг з невстановленою етіологією |
10 днів | |
| Мікоплазмова або хламідійна НП | 10–14 днів | У разі отримання клінічних або епідеміологічних даних |
| НП, спричинена S. aureus, Enterobacteriacea, P. aeruginosa | ≥14 днів | |
| Легіонельозна НП | 21 день |
При ускладненому перебігу НП, наявності позалегеневих вогнищ інфекції та повільній «відповіді» на лікування термін введення антибіотиків у хворого визначають індивідуально.
Клінічні ознаки та стани, при яких антибактеріальна терапія не продовжується і не модифікується, наведено в табл. 3.12.
Таблиця 3.12. Клінічні ознаки та стани, які не є показаннями до продовження антибактеріальної терапії або її модифікації при НП
| Клінічна ознака | Характеристика недоцільності застосування |
| Стійкий субфебрилітет (температура тіла в межах 37,0–37,5 °С) | За відсутності інших ознак бактеріальної інфекції може бути проявом неінфекційного запалення, постінфекційної астенії (вегетативної дисфункції), медикаментозної лихоманки |
| Збереження залишкових змін на рентгенограмі (інфільтрація, посилення легеневого малюнка) | Можуть зберігатися впродовж 1–2 міс та більше після перенесеної пневмонії |
| Сухий кашель | Може зберігатися протягом 1–2 міс після перенесеної пневмонії, особливо у курців та пацієнтів із ХОЗЛ |
| Збереження хрипів під час аускультації | Сухі хрипи можуть зберігатися протягом 3–4 тиж і більше після перенесеної пневмонії і свідчать про природний перебіг захворювання (локальний ендобронхіт або пневмосклероз у ділянці фокуса запалення) |
| Підвищення ШОЕ | Неспецифічний показник, не є ознакою лише бактеріальної інфекції |
| Слабкість, що зберігається, підвищене потовиділення | Прояви постінфекційної астенії |
У більшості випадків наведені симптоми НП зникають самостійно або під впливом симптоматичного лікування. Водночас рентгенологічна динаміка повільніша, ніж клінічна, тому дані контрольного рентгенологічного дослідження легень не можуть бути беззаперечним критерієм для визначення тривалості антибактеріальної терапії. Слід зазначити, що лише у 60% пацієнтів віком до 50 років із НП без супутніх захворювань зворотний розвиток рентгеноморфологічних змін у легенях відбувається впродовж перших 4 тиж. У випадку тривалої клінічної, лабораторної та рентгенологічної симптоматики НП слід здійснювати диференційну діагностику з такими захворюваннями, як емпієма плеври, рак легені, туберкульоз, застійна СН тощо.
Найбільш поширені помилки щодо застосування антибактеріальної терапії наведені в табл. 3.13.
Таблиця 3.13. Найпоширеніші помилки призначення антибактеріальної терапії у хворих на НП
| Призначення | Характеристика помилки |
| За вибором препарату (легкий або середньотяжкий перебіг НП) | |
| Гентаміцин | Відсутність активності проти пневмококів і «атипових» збудників |
| Ампіцилін per os | Низька біодоступність препарату (40%) порівняно з амоксициліном (75–90%) |
| Цефазолін | Низька антипневмококова активність, відсутність клінічно значущої активності до H. іnfluenzaе |
| Ципрофлоксацин | Низька активність стосовно S. pneumoniae та М. pneumoniae |
| Респіраторні фторхінолони | Недоцільно застосовувати як препарат вибору за відсутності факторів ризику терапевтичної невдачі (супутні захворювання, попередній прийом антибактеріальних засобів) |
| За вибором препарату (тяжкий перебіг НП) | |
| Монотерапія β-лактамами | Не перекривають увесь спектр потенційних збудників, наприклад L. pneumophila, атипову флору |
| Карбапенеми (іміпенем, меропенем) | Застосування як стартової терапії економічно не виправдане, можуть призначатися лише при аспірації та інфекції, спричиненій P. aeruginosa (крім ертапенему) |
| Антисиньогнійні цефалоспорини ІІІ покоління (цефтазидим, цефоперазон) | Поступаються цефотаксиму і цефтріаксону активністю проти S. pneumoniae; використовувати слід тільки за підозри на інфекцію, спричинену P. aeruginosa |
| За вибором шляху введення препарату | |
| Відмова від ступеневої терапії | Ступенева терапія дозволяє суттєво скоротити витрати на лікування, не погіршує прогноз. У більшості випадків перехід на пероральне введення антибіотиків можливе на 2–3-й день терапії |
| В/м введення антибіотика при тяжкому перебігу НП | Недоцільне через можливе зниження швидкості та ступеня абсорбції препарату в системний кровообіг |
| За термінами початку терапії | |
| Пізній початок антибактеріальної терапії | Затримка введення першої дози антибіотика на 4 год і більше зумовлює значне підвищення ризику смерті хворих |
| За тривалістю терапії | |
| Часта зміна антибіотика в процесі лікування, що пояснюється небезпекою розвитку резистентності | Зміна антибіотика в процесі лікування, за винятком випадків клінічної неефективності і/або непереносимості, є недоцільною. Показаннями до заміни антибіотика є:
|
| Продовження антибактеріальної терапії до повного зникнення всіх клініко-лабораторних показників НП | Головним критерієм відміни антибіотика є зворотний розвиток клінічних симптомів НП:
|
3.1.2. Госпітальна (нозокоміальна) пневмонія
Визначення. Госпітальна пневмонія — захворювання, що характеризується появою рентгенологічно верифікованих нових вогнищево-інфільтративних змін в легенях через 48 год та більше після госпіталізації в поєднанні з клінічною симптоматикою, яка підтверджує їхню інфекційну природу.
Госпітальні пневмонії становлять близько 15–18% усіх нозокоміальних інфекцій; смертність від цього захворювання дуже висока (50–70% випадків). Пневмонії виникають також у випадку внутрішньолікарняного інфікування під час інтубації трахеї, при тривалому лікуванні антибіотиками, оперативних втручаннях, хірургічних, урологічних, стоматологічних маніпуляціях. При цьому хворі, ослаблені внаслідок основного захворювання, інфікуються малопатогенною для здорових людей інфекцією. Домінуючими етіологічними факторами госпітальної пневмонії є стафілокок та грамнегативні мікроорганізми (клебсієла, протей, ентеробактерії, псевдомонас, кишкова паличка), а також грибкова флора. Джерелами інфікування в стаціонарі можуть бути повітря (аспергіли), вода (легіонела), бактеріоносійство медичного персоналу (стафілокок), медичні інструменти та устаткування (катетери, бронхоскопи, ендотрахеальні трубки, лікарняне сміття).
Класифікація госпітальної пневмонії:
1. Власне госпітальна пневмонія.
2. Вентилятор-асоційована пневмонія.
3. Госпітальна пневмонія у пацієнтів із вираженими порушеннями імунітету:
а) у реципієнтів донорських органів;
б) у пацієнтів, що отримують цитостатичну терапію.
4. Госпітальна аспіраційна пневмонія.
Власне госпітальна пневмонія. Рання госпітальна пневмонія виникає протягом перших 5 днів (>48–120 год) з моменту госпіталізації і зумовлена збудниками, які були у хворого до надходження до стаціонару (S. pneumoniae, Н. influenzae, метицилінчутливий S. aureus та інші представники нормальної мікрофлори порожнини ротоглотки). Ці збудники чутливі до антимікробних препаратів, тому захворювання має сприятливий прогноз. Пізня госпітальна пневмонія розвивається не раніше 6-го дня госпіталізації (>120 год) і спричинена госпітальною мікрофлорою з ризиком високовірулентних і полірезистентних збудників (P. aeruginosa, Acinetobacter spp., Enterobacteriaceae, MRSA), тож має менш сприятливий прогноз.
Вентилятор-асоційована пневмонія — пневмонія, яка виникла через 48 год від початку штучної/допоміжної вентиляції легень за відсутності легеневої інфекції на момент інтубації.
Госпітальна пневмонія у пацієнтів з вираженими порушеннями імунітету — пневмонія, яка виникла у реципієнтів донорських органів або у пацієнтів, що отримують цитостатичну терапію.
Госпітальна аспіраційна пневмонія — це гостре ураження легень, що виникає внаслідок аспірації контамінованого вмісту носоглотки, порожнини рота або шлунка з наступним розвитком інфекційного процесу (табл. 3.14).
Таблиця 3.14. Основні фактори ризику та збудники аспіраційної пневмонії
| Фактори ризику | Збудники пневмонії |
| Порушення свідомості різного походження |
|
| Захворювання центральної та периферичної нервової системи | |
| Гастроезофагеальний рефлюкс, блювання | |
| Дисфагія через пухлини, чужорідні тіла та травми стравоходу, середостіння, трахеї, бронхів, обличчя, шиї | |
| Механічні, ятрогенні фактори (назогастральний зонд, трахеостома та ін.) | |
| Захворювання порожнини рота. Наявність патогенних мікроорганізмів у носо- та ротоглотці |
Найбільш часто госпітальна пневмонія виникає при інтубації, що підвищує ризик розвитку захворювання в 7–21 раз. Достовірне підвищення частоти госпітальної пневмонії спостерігається у хворих похилого віку (понад 70 років) за наявності порушення свідомості, хронічного захворювання легень, гіпотрофії, операцій на органах черевної порожнини, під час прийому імуносупресивних препаратів.
Діагностичними критеріями госпітальної пневмонії є поява на рентгенограмі нових вогнищево-інфільтративних змін у легенях і наявність двох із наведених нижче ознак:
1) температура тіла >38,0 °С;
2) бронхіальна гіперсекреція, гнійне мокротиння;
3) кашель, тахіпное; локальна крепітація, вологі хрипи, бронхіальне дихання;
4) розвиток артеріальної гіпоксемії; FiO2 (фракція кисню у повітрі, що вдихається) — від 0,21 (при диханні повітрям) до 1 (при диханні 100% киснем);
5) лейкопенія (<4,0•109/л) чи лейкоцитоз (>10,0•109/л), паличкоядерний зсув (>10%).
Показання до госпіталізації до відділення інтенсивної терапії хворих на госпітальну пневмонію [18, 28]
Абсолютні показання до госпіталізації/переведення до відділення інтенсивної терапії («великі» критерії тяжкості перебігу госпітальної пневмонії): потреба у застосуванні механічної вентиляції легень; септичний шок (середній АТ <65 мм рт. ст., зниження АТ >40 мм рт. ст. від вихідного рівня, ЧСС >130/хв, гіпоперфузія тканин); необхідність введення вазопресорних препаратів.
Відносні показання до госпіталізації/переведення до відділення інтенсивної терапії («малі» критерії тяжкості перебігу госпітальної пневмонії): частота дихання 30/хв та більше; порушення свідомості; сатурація артеріальної крові киснем (SaO2) <90%, РаО2 <60 мм рт. ст.; САТ <90 мм рт. ст., ДАТ <60 мм рт. ст.; двобічне або багаточасткове ураження легень, порожнини розпаду, плевральний випіт; швидке прогресування вогнищево-інфільтративних змін у легенях: збільшення розмірів інфільтрації більше ніж на 50% протягом 2 діб; гостре пошкодження нирки (кількість сечі <80 мл за 4 год або рівень креатиніну в сироватці крові >0,18 ммоль/л, або концентрація азоту сечовини >7 ммоль/л (азот сечовини = сечовина (ммоль/л) : 2,14) за відсутності ХНН.
Наявність у хворого хоча б одного «великого» або двох «малих» критеріїв є показанням до госпіталізації до відділення інтенсивної терапії. Для вирішення питання госпіталізації до відділення інтенсивної терапії, окрім наведених критеріїв, слід використовувати шкали оцінки стану CRB-65, SMART-COP, PORT, враховувати наявність декомпенсації супутніх захворювань, ускладнень госпітальної пневмонії та власний клінічний досвід лікаря.
Інтенсивна терапія хворих із тяжким перебігом госпітальної пневмонії передбачає емпіричну антибактеріальну терапію, респіраторну та гемодинамічну підтримку, застосування окремих медикаментозних препаратів за показаннями, профілактику та лікування тромбоемболічних ускладнень, жорсткий контроль глікемії, раннє ентеральне харчування.
Схему лікування різних форм госпітальних і аспіраційних пневмоній наведено в алгоритмі 3.3.
| Алгоритм 3.3. Лікування внутрішньолікарняних та аспіраційних пневмоній [8]
Крок 1. Легкий перебіг внутрішньолікарняних пневмоній:
Крок 2. Середньотяжкий перебіг внутрішньолікарняних пневмоній:
Крок 3. Тяжкий перебіг внутрішньолікарняних пневмоній:
Лікування аспіраційної пневмонії незалежно від ступеня тяжкості:
|
Традиційна антибіотикотерапія хворих на госпітальну пневмонію триває 14–21 день. Збільшення її тривалості може призвести до суперінфекції полірезистентними госпітальними збудниками.
У табл. 3.15 наведено рекомендації IDSA та ATS (2016) стосовно лікування клінічно підозрюваної вентилятор-асоційованої пневмонії емпіричним призначенням антибіотика із активністю проти Staphylococcus aureus і двох антибіотиків, активних проти синьогнійної палички/грамнегативних збудників, а також засоби протимікробної терапії при різних формах госпітальних і негоспітальних пневмоній (табл. 3.16 і 3.17) [15, 40].
Таблиця 3.15. Лікування клінічно підозрюваної вентилятор-асоційованої пневмонії (IDSA, ATS, 2016) і протимікробна терапія при різних формах госпітальних і негоспітальних пневмоній [11]
| Антибіотик з активністю проти грамнегативних патогенів, включно із MRSA | Антибіотик із активністю проти грамнегативних патогенів, включно з ß-лактамними антибіотиками | Антибіотик із активністю проти грамнегативних патогенів, окрім ß-лактамних антибіотиків |
Глікопептиди1
|
Антисиньогнійні пеніциліни2
|
Фторхінолони
|
| АБО | АБО | АБО |
Оксазолідинони
|
Цефалоспорини2
|
Аміноглікозиди1, 3
|
| АБО | АБО | |
Карбапенеми2
|
Поліміксини1, 5
|
|
| АБО | ||
|
Примітки. Слід із кожної колонки вибрати по одному антибіотику. Доза, запропонована у таблиці, може коригуватися для пацієнтів із печінковою або нирковою дисфункцією.
1Необхідне вимірювання концентрації препарату в крові з подальшим коригуванням дози та/або інтервалу між введеннями.
2Можуть бути доцільними тривалі інфузії. Див. розділ, присвячений терапії за фармакокінетичними/фармакодинамічними параметрами.
3За даними метааналізу, застосування аміноглікозидів було пов’язане з нижчим показником клінічної відповіді, але не було відмічено різниці щодо смертності.
4Може знадобитися зниження дози для пацієнтів з масою тіла <70 кг з метою запобігання судинним нападам.
5Застосування поліміксинів слід обмежити відділеннями, у яких спостерігається висока частота полірезистентних патогенів та є місцевий досвід застосування цих препаратів. Дозування базується на активності колістину у вигляді основи. Наприклад, доза 1 млн МО колістину еквівалентна приблизно 30 мг колістину у вигляді основи, що відповідає приблизно 80 мг проліків колістиметату. 1 мг поліміксину В = 10 000 одиниць.
6Якщо немає інших варіантів, додатково до іншого β-лактамного антибіотика можна використати азтреонам, оскільки він має інші мішені в клітинній стінці бактерій.
Таблиця 3.16. Рекомендована початкова антибіотикотерапія нозокоміальної пневмонії (не вентилятор-асоційованої пневмонії) (IDSA, ATS, 2016)
| Немає високого ризику смертності та факторів, які збільшують імовірність MRSA2, 3 | Немає високого ризику смертності 1, але є фактори, що збільшують імовірність MRSA2, 3 | Високий рівень смертності або введення в/в антибіотиків протягом попередніх 90 днів1, 3 |
| Один із нижченаведених | Один із нижченаведених | Два із нижченаведених; слід уникати β-лактамних антибіотиків |
| Піперацилін + тазобактам4 4,5 г в/в кожні 6 год | Піперацилін + тазобактам4 4,5 г в/в кожні 6 год | Піперацилін + тазобактам4 4,5 г в/в кожні 6 год |
| АБО | АБО | АБО |
| Цефепім4 2 г в/в кожні 8 год | Цефепім4 або цефтазидим 2 г в/в кожні 8 год | Цефепім4 або цефтазидим 2 г в/в кожні 8 год |
| АБО | АБО | АБО |
| Левофлоксацин 750 мг в/в щоденно | Левофлоксацин 750 мг в/в щоденно
Ципрофлоксацин 400 мг в/в кожні 8 год |
Левофлоксацин 750 мг в/в щоденно
Ципрофлоксацин 400 мг в/в кожні 8 год |
| АБО | АБО | АБО |
| Іміпенем4 500 мг в/в кожні 6 год
Меропенем4 1 г в/в кожні 8 год |
Іміпенем4 500 мг в/в кожні 6 год
Меропенем4 1 г в/в кожні 8 год |
Іміпенем4 500 мг в/в кожні 6 год
Меропенем4 1 г в/в кожні 8 год |
| АБО | АБО | |
| Азтреонам 2 г в/в кожні 8 год | Амікацин 15–20 мг/кг щоденно
Гентаміцин 5–7 мг/кг в/в щоденно Тобраміцин 5–7 мг/кг в/в щоденно |
|
| АБО | ||
| Азтреонам5 2 г в/в кожні 8 год | ||
| Плюс
Ванкоміцин 15 мг/кг в/в кожні 8–12 год з метою досягнення мінімального рівня 15–20 мг/мл (слід розглянути доцільність навантажувальної дози 25–30 мг/кг × 1 у разі тяжкого захворювання) |
Плюс
Ванкоміцин 15 мг/кг в/в кожні 8–12 год з метою досягнення мінімального рівня 15–20 мг/мл (слід розглянути доцільність навантажувальної дози 25–30 мг/кг × 1 у разі тяжкого захворювання) |
|
| АБО | АБО | |
| Якщо призначення антибіотика з активністю проти MRSA не передбачається, слід призначити препарат, який є активним проти MSSA.
Варіанти: піперацилін + тазобактам, цефепім, левофлоксацин, іміпенем, меропенем. Оксацилін, нафцилін і цефазолін є препаратами, яким надається перевага для лікування доведеного MSSA, але зазвичай їх не використовують для емпіричного лікування НП |
||
| Якщо пацієнт має тяжку алергію на піперацилін і передбачається призначення азтреонаму замість будь-якого β-лактамного антибіотика, слід призначити антибіотик із активністю проти MSSA | ||
Примітки. MSSA — метицилінчутливий S. аureus.
1Фактори ризику смертності включають потребу в ШВЛ з приводу НП і септичного шоку.
2Показаннями до призначення антибіотика з активністю проти MRSA є в/в введення антибіотика протягом попередніх 90 днів, перебування пацієнта у відділенні, де частота ізолятів MRSA є невідомою або >20%. Попереднє виявлення MRSA при скринінгу культуральними або некультуральними методами може також підвищувати ризик MRSA. Рівень 20% був вибраний для того, щоб знайти баланс між необхідністю ефективності початкової антибіотикотерапії та ризиком надмірного застосування антибіотиків. Цей рівень може коригуватися відповідно до місцевих цінностей і переваг. Якщо активність MRSA нехтується, антибіотикотерапія повинна включати препарат із активністю проти MRSA.
3Якщо пацієнт має фактори, які підвищують імовірність грамнегативної інфекції, або обструктивне захворювання легень, яке підвищує ризик грамнегативної інфекції (наприклад бронхоектаз або муковісцидоз), рекомендовано застосовувати два антисиньогнійні препарати. Якщо результати високоякісного забарвлення респіраторних зразків за Грамом показують значну кількість і переважання грамнегативних паличок, це підвищує ймовірність пневмонії, зумовленої грамнегативними патогенами, включаючи мікроорганізми, що ферментують і не ферментують глюкозу.
4Можуть бути доцільними тривалі інфузії.
5Якщо немає інших варіантів, додатково до іншого β-лактамного антибіотика можна використати азтреонам, оскільки він має інші мішені дії в клітинній стінці бактерії.
Таблиця 3.17. Емпірична протимікробна терапія при різних формах госпітальної та негоспітальної пневмонії [7]
| Захворювання | Збудники | Засоби І ряду | Альтернативні засоби |
| НП: легкий перебіг | S. pneumoniae, Mycoplasma, Chlamidia | Амоксицилін або макролід | 1. Цефалоспорини ІІ покоління
2. Амоксицилін/клавуланова кислота 3. Левофлоксацин або моксифлоксацин 4. Доксициклін |
| НП: середньотяжкий перебіг; госпіталізовані хворі | S. pneumoniae, H. influenzae, Mycoplasma, Chlamidia | Ампіцилін в/м, в/в чи амоксицилін перорально чи амоксицилін/клавуланова кислота | 1. Цефуроксим
2. Цефотаксим чи цефтріаксон 3. Левофлоксацин або моксифлоксацин |
| НП: тяжкий перебіг; хворі, госпіталізовані до реанімації | S. pneumoniae, Legionela, Enterobacteriaceae | Цефтріаксон чи цефотаксим, чи цефепім + макролід | 1. Левофлоксацин
2. Моксифлоксацин |
| НП на фоні ХОЗЛ | H. influenzae, S. pneumoniаe, M. catarrhalis | Амоксицилін/клавуланова кислота | 1. Цефуроксим
2. Цефотаксим чи цефтріаксон 3. Левофлоксацин або моксифлоксацин |
| НП у хворих похилого віку, з ЦД, алкоголізмом | S. pneumoniаe, H. influenzae, S. aureus, Klebsiella spp., інші грамнегативні бактерії | Цефотаксим чи цефтріаксон | 1. Амоксицилін/клавуланова кислота
2. Левофлоксацин або моксифлоксацин 3. Ципрофлоксацин |
| Госпітальна пневмонія у відділеннях загального профілю | Enterobacteriaceae, S. aureus, S. pneumoniаe | Цефотаксим чи цефтріаксон | 1. Левофлоксацин
2. Моксифлоксацин 3. Цефепім |
| Реанімація (з використанням ШВЛ) | Ті самі + P. aeruginosa, Acinetobacter spp. | Цефепім; цефтазидим + амікацин + ванкоміцин | 1. Іміпенем
2. Меропенем 3. Цефоперазон + амікацин 4. Ципрофлоксацин + амікацин + ванкоміцин |
| Аспіраційна пневмонія | Анаероби S. aureus, Enterobacteriaceae | Цефоперазон/сульбактам/тикарцилін/клавуланова кислота | 1. Цефалоспорини ІІ–ІІІ + кліндаміцин
2. Фторхінолон + кліндаміцин 3. Іміпенем чи меропенем |
При аспіраційній госпітальній пневмонії показанням до термінового початку емпіричної антибактеріальної терапії є препарат вибору — захищений амінопеніцилін (амоксицилін/клавуланова кислота); альтернативні препарати — карбапенем або фторхінолон (моксифлоксацин).
Інфекційно-токсичний шок
Тяжкий перебіг захворювання інколи спричиняє розвиток ІТШ.
Визначення. ІТШ — це невідкладний стан, що виникає внаслідок бактеріємії, зумовлений дією бактерій, біологічно активних речовин і токсинів, який супроводжується порушенням життєво важливих функцій організму (системного кровообігу, дихання, ЦНС, згортання крові, ендокринної регуляції) [5].
Основні ланки патогенезу ІТШ:
1. Патогенетичний вплив бактерій на органи кровообігу, дихання, ЦНС.
2. У результаті активації різних пошкоджувальних факторів виникає вазодилатація, підвищується судина проникність, активується агрегація тромбоцитів і надходження в кров дериватів арахідонової кислоти, активних кисневих радикалів, лізосомальних ферментів.
3. Внаслідок запуску вказаного каскаду патологічних реакцій відбувається порушення мікроциркуляції, ураження елементів крові, ендотелію судин, знижується загальний периферичний судинний опір.
4. Компенсаторно збільшується синтез адренокортикотропного гормону, кортизолу, альдостерону; це призводить до затримки Na+ та води в організмі, що забезпечує стримання зниження АТ і підвищення ХОК та загального периферичного судинного опору (це гіпердинамічна реакція циркуляції).
5. На тлі прогресуючого процесу відбувається перерозподіл системного кровотоку, збільшується робота серця, нирками затримуються вода і солі, підвищується рівень глюкози в крові і відбувається перехід інтерстиціальної рідини з тканин у судини.
6. Ці багатофакторні зміни зумовлюють розвиток сладж-синдрому і синдрому ДВЗ, а локальні гіпоксичні порушення призводять до виникнення ацидозу і накопичення тканинних метаболітів, які розширюють прекапіляри і спазмують посткапіляри. Капілярне русло розширюється і депонує 10% ОЦК [4, 24, 32].
Класифікація ІТШ за Hardaway
1. Зворотний шок, який має 3 стадії розвитку:
1.1. Ранній зворотний шок.
1.2. Пізній зворотний шок.
1.3. Стійкий зворотний шок.
2. Незворотний шок.
Клінічні прояви: АТ знижується у середньому на 20–35 мм рт. ст., а у хворих із СН — на 40–60 мм рт. ст.
Стадія 1.1. ІТШ короткочасний і не завжди діагностується. Шкіра та видимі оболонки бліднуть, виникає тахікардія. Зіниці звужені; дихання глибоке, ритмічне, дещо збільшується. Тони серця звучні (поступає мало крові). Діурез знижується (дебіт не менше 40 мл/год). У крові незначний метаболічний ацидоз, гіперкоагуляція, гіперглікемія.
Стадія 1.2. ІТШ характеризується поступовим зменшенням ХОК, УО; підвищується загальний периферичний судинний опір, знижується АТ (при критичному САТ 70–60 мм рт. ст. не відбувається ниркова фільтрація сечі і наростає гіпоксія нирок). АТ важко визначити. Відбувається психомоторне збудження, збільшується блідість шкіри (вона має мармуровий відтінок), виникає ціаноз, симптоми синдрому ДВЗ.
Стадія 1.3. ІТШ. Артеріальна гіпотензія, тахікардія, тахіпное наростають. АТ визначити не вдається. Тони серця ослаблені. Може виникати дихання Чейна — Стокса, тотальний ціаноз; вологі хрипи в легенях наростають.
Незворотний шок характеризується наростанням ціанозу та гіпотензії; АТ не вдається визначити. Поглиблюються симптоми гіпоксії головного мозку, яка поступово переходить у мозкову кому. Настає зупинка серцевої діяльності та дихання.
Трьохетапний протокол ранньої цілеспрямованої терапії хворих із септичним шоком (Early-Goal Directed Therapy — EGDT)
Протокол застосовують, якщо після інфузії (20–30 мл/кг) та початку антибіотикотерапії не відбулося стабілізації рівня показників гемодинаміки. Насамперед виконується встановлення центрального венозного катетера та артеріального катетера для прямого моніторингу АТ. Здійснюється оцінка показань до інтубації трахеї та ШВЛ, починається респіраторна підтримка.
Перший етап передбачає титроване введення кристалоїдів у дозі 20–30 мл/кг (по 500 мл рідини струминно, до 2–3 л) до досягнення значень центрального венозного тиску у межах від 8 до 12 мм вод. ст. У пацієнтів, які все ще перебувають на самостійному диханні, здійснюється повторна оцінка показань до інтубації трахеї та ШВЛ. У пацієнтів із тяжким шоком, які перебувають на ШВЛ, цільовий рівень центрального венозного тиску — 12–15 мм вод. ст.
Другий етап. За відсутності позитивної динаміки після інфузії призначають вазопресори для підтримки середнього АТ на рівні >65 мм рт. ст. Коли стан пацієнта критичний, вазопресори (препаратом вибору є норадреналін) призначають негайно, тобто 1-й та 2-й кроки поєднують. Норадреналін вводять за допомогою шприцевого насоса-дозатора; доза препарату може варіюватися у широких межах (2–20 мкг/хв).
Третій етап. Здійснюється оцінка насичення киснем крові в центральній вені (ScvO2). При ScvO2 <70% призначають інотропні препарати (добутамін, дофамін, адреналін). При рефрактерному шоку показане призначення кортикоїдів (гідрокортизон у дозі 50–75 мг кратністю до 4 разів на добу).
У розвинених країнах питання про призначення низьких доз кортикоїдів вирішується за результатами тесту зі стимуляцією кортикотропіном. З урахуванням малодоступності цього тесту, а також того факту, що приблизно 75% пацієнтів зі стійкою до вазопресорів гіпотензією мають недостатність надниркової залози, у хворих із септичним шоком обґрунтоване емпіричне використання цих препаратів. При септичному шоку з гіпотензією, резистентною до рідинної ресусцитації та терапії вазопресорами, показане введення гідрокортизону в добовій дозі 200–300 мг. У хворих із тяжким перебігом госпітальної пневмонії, в яких відсутні прояви резистентного до вазопресорів септичного шоку, рутинне використання ГК не показане.
Профілактика. Специфічна профілактика пневмонії не розроблена. Необхідно підвищувати неспецифічну резистентність організму шляхом загартовування, заняття спортом, дихальною гімнастикою, налагодження повноцінного збалансованого харчування з достатньою кількістю вітамінів, мікроелементів, особливо тих, що містять цитопротектори (вітамін А, Е, мікроелемент селен тощо).
