Хронічне обструктивне захворювання легень — дуже розповсюджена нині патологія, яка займає друге місце після ССЗ і четверте місце в структурі причин смертності. Від ХОЗЛ у світі щорічно помирають 2,75 млн пацієнтів. Експерти ВООЗ прогнозують збільшення економічного збитку від ХОЗЛ до 2020 р. і стверджують, що вони посідатимуть перше місце серед захворювань органів дихання та третє місце серед усіх причин смерті. В Україні на ХОЗЛ хворіють близько 3 млн людей, або як мінімум 7% населення.
Визначення. Хронічне обструктивне захворювання легень — це хворобливий стан, що характеризується стійким обмеженням прохідності дихальних шляхів, яке не є повністю зворотним. Обмеження повітряного потоку зазвичай прогресує і пов’язане з незвичайною відповіддю легень запального характеру на шкідливі частки або гази. Це захворювання, якому можна запобігти та яке можна лікувати (GOLD, 2018).
Етіологія. Фактори ризику ХОЗЛ поділяються на зовнішні та внутрішні [19, 21].
Зовнішні фактори ризику:
- довготривале тютюнопаління;
- промислові та побутові шкідливі викиди (повітряні полютанти, гази та пари хімічних сполук, продукти згорання пального);
- інфекційні (тяжкі дитячі інфекції, респіраторні інфекції);
- низький соціальний та економічний рівень життя (скупченість населення, шкідливі звички тощо).
Внутрішні фактори ризику:
- генетично зумовлені (спадковий дефіцит α1-антитрипсину);
- аномалії розвитку легень;
- гіперреактивність бронхів.
Найбільш вагомими причинами підвищення розповсюдженості інвалідизації та летальності при ХОЗЛ є тютюнопаління (провідний фактор ризику), старіння населення, погіршення стану довкілля, часті респіраторні та вірусні інфекції, які послаблюють імунітет і погіршують функціональний стан легень.
Патогенез. Основні ланки механізму розвитку ХОЗЛ наступні:
1) хронічне запалення бронхів, паренхіми та судин легень;
2) дисбаланс оксидантів/антиоксидантів з перевагою оксидантів;
3) дисбаланс протеаз/антипротеаз у легенях;
4) медіатори запалення: лейкотрієни В4, інтерлейкін-8, фактор некрозу пухлин альфа тощо;
5) клітинне запалення: нейтрофіли, макрофаги, Т-лімфоцити, еозинофіли, епітеліальні клітини;
6) вентиляційно-перфузійні порушення в легенях, що призводять до підвищення концентрації в крові СО2 — дуже сильного вазодилататора, який знижує загальний периферичний опір судин і збільшує ємність артеріального русла;
7) важливу роль у розвитку набряків при хронічному легеневому серці у пацієнтів з ХОЗЛ відіграє підвищення внутрішньогрудного тиску внаслідок гіперфункції легень, що призводить до екстракорпорального депонування крові, в результаті чого суттєво знижується венозне повернення крові до серця і створюються умови для її застою в системі верхньої та нижньої порожнистих вен.
Важливими патогенетичними факторами розвитку ХОЗЛ є обмеження дихального повітряного потоку, спричинене поєднанням ураження бронхів (обструктивний бронхіт) і руйнування паренхіми (емфізема легень), співвідношення яких змінюється індивідуально. Відбувається розвиток ремоделювання та звуження бронхів, руйнування альвеолярних перетинок, зменшення еластичності легень, що призводить до послаблення утримання дихальних шляхів відкритими під час видиху.
За даними досліджень переконливо доведено, що в розвитку ХОЗЛ суттєве значення мають такі патофізіологічні механізми [36, 44]:
- гіперсекреція слизу;
- дисфункція війчастого епітелію;
- обмеження повітряного потоку в бронхах;
- надмірне здуття легень;
- легенева гіпертензія (ЛГ);
- легеневе серце;
- порушення газообміну в результаті розвитку альвеолярно-капілярного блоку.
Хронічне обструктивне захворювання легень і фактори ризику коморбідних станів
Тютюнопаління є важливим фактором ризику розвитку ХОЗЛ. Визначається тісний взаємозв’язок між тютюнопалінням і запальною реакцією, оксидативним стресом і порушенням ендотеліальної функції легень.
Ожиріння має тісний взаємозв’язок зі зниженням легеневої функції і розвитком ХОЗЛ.
Зменшення маси тіла і респіраторна кахексія мають певне значення у розвитку ХОЗЛ. Прозапальна активація є одним із факторів, які пов’язують ХОЗЛ з дефіцитом маси тіла. Встановлено, що недоношеність або порушення харчування в ранній неонатальний період зумовлені затримкою «дозрівання» легень, що проявляється накопиченням еластину, розширенням альвеол та стоншенням їх стінок. Усе це може призводити до виникнення ХОЗЛ без впливу продуктів цитокінової активності на мембрани альвеолоцитів та епітелій бронхів.
СН і ФП верифікуються, за різними даними, у 20–33% пацієнтів з документованим ХОЗЛ. Зниження ОФВ1 є сильним маркером як несприятливого прогнозу, асоційованого з респіраторними причинами, так і високого ризику кардіоваскулярної смертності. Підвищення жорсткості артеріальної стінки асоціюється з тяжкістю бронхіальної обструкції і може розцінюватися як фактор кардіоваскулярного ризику у пацієнтів з ХОЗЛ. Спостерігається стійкий взаємозв’язок між СН, ФП і частотою інсультів, які серед пацієнтів з ХОЗЛ є більш вираженими, ніж у загальній популяції.
Ризик кардіоваскулярних подій як фактор можливого виживання пацієнтів з ХОЗЛ. Встановлено, що дисфункція міокарда є не тільки важливим предиктором підвищення ризику смерті в когорті пацієнтів з ХОЗЛ, але й свідчить про велике самостійне значення кардіоваскулярних факторів ризику в еволюції ХОЗЛ. Аналіз національних кадастрів США (USA National Hospital Discharge Survey) нараховує понад 47 млн випадків госпіталізації пацієнтів з ХОЗЛ за 1979–2001 рр. У них спостерігалася перевага госпітальної над негоспітальною смертністю. При цьому основними причинами смерті були пневмонія, АГ, СН і злоякісні новоутворення (переважно рак легені). Поряд з цим цереброваскулярні захворювання, ХХН, шлунково-кишкові кровотечі не були асоційовані ані з різними причинами госпіталізацій, ані з основними причинами смерті пацієнтів із ХОЗЛ. Отримані дані свідчать про те, що в осіб з документованим ХОЗЛ основними причинами госпіталізації та смерті є кардіоваскулярні захворювання, які відображають тісний взаємозв’язок між патофізіологічними механізмами цих захворювань.
Класифікація. Відповідно до сучасної класифікації (GOLD, 2018) виділяють 4 ступені захворювання (табл. 3.28). Класифікацію ХОЗЛ залежно від ризику розвитку несприятливих подій наведено в табл. 3.29.
Таблиця 3.28. Спірометрична класифікація ХОЗЛ за ступенем тяжкості та порушень ОФВ1 після прийому бронхолітика
| Ступінь тяжкості | Ознаки ХОЗЛ |
| У пацієнтів із ОФВ1/ФЖЄЛ <70% | |
| GOLD 1, легкий | ОФВ1 ≥80% від належного |
| GOLD 2, помірний | 50% ≤ ОФВ1 <80% від належного |
| GOLD 3, тяжкий | 30% ≤ ОФВ1 <50% від належного |
| GOLD 4, дуже тяжкий | ОФВ1 <30% від належного |
Таблиця 3.29. Класифікація ХОЗЛ залежно від ризику розвитку несприятливих подій
| Оцінюючи ризик, необхідно вибирати найвищий ризик несприятливих подій, виходячи зі спірометричної класифікації або анамнезу загострень | |||||
| Ризик GOLD:
класифікація обмеження прохідності дихальних шляхів, що ґрунтується на ОФВ1 |
4 | С | D | ≥2 | Ризик
Анамнез загострень за попередній рік |
| 3 | |||||
| 2 | А | В | 1 | ||
| 1 | 0 | ||||
| мМКД <2 | мМКД ≥2 | ||||
| ТОХ <10 | ТОХ ≥2 | ||||
| Симптоми | |||||
Примітки. Характеристика вказаних груп хворих:
- Хворі групи А — низький ризик несприятливих подій, мало симптомів;
- Хворі групи В — низький ризик несприятливих подій, багато симптомів;
- Хворі групи С — високий ризик несприятливих подій, мало симптомів;
- Хворі групи D — високий ризик несприятливих подій, багато симптомів.
ТОХ — тест для оцінки ХОЗЛ; мМКД — модифікована шкала задишки Медичного дослідницького консиліуму.
Загострення ХОЗЛ — це складні події, які зазвичай пов’язані із запаленням дихальних шляхів, збільшенням слизової продукції та виявленням захоплення газу. Прогресивне збільшення задишки є ключовим симптомом загострення. Інші симптоми включають збільшення гнійності та кількості мокротиння. Оcкільки у хворих на ХОЗЛ поширені супутні захворювання, загострення слід диференціювати від гострого коронарного синдрому, погіршення застійної СН, емболії легеневої артерії та пневмонії.
Загострення ХОЗЛ класифікуються таким чином:
- легке (не інфекційне) — наявність одного симптому (або збільшення задишки, або збільшення мокротиння); лікування було лише бронхолітичними засобами короткої дії;
- помірне (інфекційне) — наявність двох симптомів, один із яких обов’язковий — гнійне мокротиння; лікування бронходилататорами короткої дії плюс антибіотики та/або пероральні кортикостероїди;
- тяжке (інфекційне) — наявність усіх трьох симптомів; пацієнт потребує госпіталізації або невідкладної допомоги. Тяжкі загострення можуть бути пов’язані з гострою дихальною недостатністю.
Загострення головним чином спричиняються респіраторними вірусними інфекціями, хоча бактеріальні інфекції та фактори навколишнього середовища також можуть ініціювати та/або посилювати ці події.
Приклади формулювання діагнозу:
1. ХОЗЛ, група А, ЛН І ступеня.
2. ХОЗЛ, група В, ЛН І ступеня.
3. ХОЗЛ, група С, інфекційне тяжке загострення. ЛН ІІІ ступеня, недостатність кровообігу І стадії.
Клініка та діагностика ХОЗЛ [21, 35]
Обсяг діагностичних та лікувальних заходів на первинному рівні надання медичної допомоги: здійснюється спостереження за хворими на ХОЗЛ групи А або В (ОФВ1 >50%): збір скарг, оцінка факторів ризику, фізикальне обстеження; опитування для оцінки симптомів за модифікованою шкалою Медичної дослідницької ради (мМДР) та ТОХ; постбронходилатаційний тест; рентгенографія органів грудної порожнини; повний аналіз крові, ІМТ.
Показання до діагностичних та лікувальних заходів на вторинному рівні надання медичної допомоги: діагностична невизначеність; підозра на наявність тяжкого ХОЗЛ; пацієнт цікавиться альтернативною думкою; з’ясовуються часті загострення; кровохаркання; розвиток легеневого серця; оцінка стану для призначення кисневої терапії; оцінка стану для призначення довготривалої небулайзерної терапії; оцінка стану для призначення ГК для перорального застосування; бульозна хвороба легень (визначення показань до хірургічного лікування); різке зниження ОФВ1; початок виникнення симптомів у віці до 40 років або сімейний анамнез дефіциту α1-антитрипсину; диспропорція між симптоматикою і порушеннями функції легень; пошук інших пояснень, включаючи патологію серцево-судинної системи, ЛГ, депресію.
Додаткові методи обстеження: полісомнографічне дослідження (при синдромі обструктивного апное-гіпопное уві сні); бодиплетизмографія (для визначення бронхіального опору, легеневих об’ємів та ємностей, ознак ЛН; тести з фізичним навантаженням (толерантність до фізичного навантаження); вимірювання газів артеріальної крові (підозра на ЛН та правошлуночкову недостатність); скринінг дефіциту α1-антитрипсину (розвиток ХОЗЛ у молодому віці).
Показання до діагностичних та лікувальних заходів на третинному рівні надання медичної допомоги: тяжкий перебіг хвороби, що вимагає втручання; такі пацієнти повинні регулярно проходити огляд у фахівців. Питання про хірургічне втручання розглядається стосовно таких груп хворих:
- пацієнти із задишкою, які мають єдину велику булу, виявлену завдяки КТ, і ОФВ1 <50% від належного, повинні бути направлені до спеціалізованого стаціонару для вирішення питання щодо булектомії;
- пацієнти з тяжким ХОЗЛ, у яких зберігається задишка і спостерігається істотне обмеження повсякденної активності при адекватній медикаментозній терапії (включаючи реабілітацію), повинні направлятися до спеціалізованих центрів для вирішення питання резекції частини легень за наступних умов: ОФВ1 >20% від належного; РаСО2 <7,3 кПа; емфізема, що розповсюджується на верхню частку легень; DLCO (дифузійна здатність легень для CO) >20% від розрахункового;
- хворі з тяжкими проявами ХОЗЛ та вираженою задишкою і значним обмеженням щоденної діяльності при максимальній терапії повинні розглядатися як кандидати для пересадки легень з урахуванням супутньої патології та хірургічного втручання.
У старій термінології використовувався термін «дихальна недостатність», який мав широке значення і включав характеристику порушень вентиляції, газообміну, транспорту кисню, тканинного обміну. Наразі використовують термін «легенева недостатність».
ЛН — це нездатність легень забезпечити нормальний газовий склад артеріальної крові в стані спокою та/або за помірних фізичних навантажень.
Класифікація ЛН [21, 35, 44]:
І ступінь — хворий відзначає появу задишки, якої раніше не було, під час звичного фізичного навантаження (рівень звичного навантаження є індивідуальним для кожного пацієнта і залежить від його фізичного функціонального стану).
ІІ ступінь — задишка виникає під час незначного фізичного навантаження (ходьба по рівній місцевості).
ІІІ ступінь — задишка турбує в стані спокою.
При ХОЗЛ слід застосовувати не класифікацію ХСН за М.Д. Стражеском та В.Х. Василенком (1935), а класифікацію недостатності кровообігу, прийняту ІІІ З’їздом фтизіатрів і пульмонологів України (2003) (кардіологам та пульмонологам слід узгодити вказані класифікації, оскільки в них існують суттєві розбіжності та невідповідності).
Виділяють наступні стадії недостатності кровообігу:
- стадія недостатності кровообігу — нечітко виражені ознаки застою крові у великому колі кровообігу (набряки на ногах, збільшена печінка), які минають під впливом лікування основного захворювання або діуретиків;
- стадія недостатності кровообігу — наявність виражених набряків і порушень гемодинаміки з розвитком гепатомегалії, які потребують інтенсивного лікування діуретиками, іАПФ або БРА;
- (термінальна) стадія характеризується вторинними ураженнями інших органів та систем; єдиний засіб, що подовжує життя пацієнтів при цій стадії, — це безперервна оксигенотерапія.
Клінічна картина ХОЗЛ багатогранна. Основною скаргою хворих на ХОЗЛ є кашель, який передує задишці. Спочатку він виникає спорадично, а потім турбує щоденно, частіше вдень. Задишка при ХОЗЛ є одним з основних симптомів захворювання. Ступені її вираженості відображає шкала MRC (табл. 3.30).
Таблиця 3.30. Шкала ступенів задишки MRC
| Ступінь | Тяжкість | Характеристика |
| 0 | – | Задишка не турбує, за винятком дуже значного навантаження |
| 1 | Легка | Задишка при швидкій ходьбі або при невеликому підйомі |
| 2 | Середня | Задишка при більш повільній ходьбі у порівнянні з іншими людьми такого ж віку, що змушує пацієнта зупинятися |
| 3 | Тяжка | Задишка змушує хворого робити зупинки під час ходьби по рівній дорозі на відстань близько 100 м або через декілька хвилин |
| 4 | Дуже тяжка | Задишка не дозволяє виходити із квартири або виникає під час одягання чи роздягання |
Для оцінки симптомів у пацієнтів з ХОЗЛ існує декілька валідизованих опитувальників. GOLD пропонує застосовувати мМДР для оцінки тяжкості задишки (табл. 3.31) та тест для оцінки ХОЗЛ (ТОХ) (табл. 3.32). мМДР для оцінки тяжкості задишки відображає один симптом — задишку; ТОХ ширше відображає вплив захворювання на повсякденну активність пацієнта та його самопочуття.
Таблиця 3.31. мМДР для оцінки тяжкості задишки
| Оцінка задишки в балах |
Характеристика задишки |
| 0 | Задишка виникає лише при дуже інтенсивному навантаженні |
| 1 | Задишка під час швидкого підйому на поверх або при ходьбі в гору |
| 2 | Задишка примушує мене ходити повільніше, ніж люди мого віку, або з’являється необхідність зупинки при ходьбі в своєму темпі по рівній місцевості |
| 3 | Задишка примушує робити зупинки при ходьбі на відстань близько 100 м або через декілька хвилин ходьби по рівній місцевості |
| 4 | Задишка робить неможливим вихід за межі свого будинку або з’являється при одяганні і роздяганні |
Таблиця 3.32. TOX
|
Приклад заповнення анкети пацієнтом Я дуже щасливий(-а) |
Бали
| Я взагалі не кашляю | 0 | 1 | 2 | 3 | 4 | 5 | Я кашляю постійно |
| У мене в грудях зовсім немає мокротиння (слизу) | 0 | 1 | 2 | 3 | 4 | 5 | Мої груди повністю заповнені мокротинням (слизом) |
| Мене зовсім не тисне в грудях | 0 | 1 | 2 | 3 | 4 | 5 | Мені дуже сильно тисне в грудях |
| Коли я йду під гору або підіймаюсь сходами на один марш, я не відчуваю задишки | 0 | 1 | 2 | 3 | 4 | 5 | Коли я йду під гору або підіймаюсь сходами на один марш, я відчуваю сильну задишку |
| Я займаюсь будь-якими домашніми справами без обмежень | 0 | 1 | 2 | 3 | 4 | 5 | Я займаюсь домашніми справами з великими обмеженнями |
| Виходячи з дому, я почуваюся впевнено, незважаючи на захворювання легень | 0 | 1 | 2 | 3 | 4 | 5 | Виходячи з дому, я почуваюся невпевнено через захворювання легень |
| Я міцно сплю | 0 | 1 | 2 | 3 | 4 | 5 | Я погано сплю через захворювання легень |
| У мене багато енергії | 0 | 1 | 2 | 3 | 4 | 5 | У мене зовсім немає енергії |
| Загальний рахунок TOX визначається як сума балів відповідей на кожне з восьми запитань | |||||||
| Загальний результат ТОХ визначається як сума балів відповідей на кожне з восьми запитань. Оцінка задишки ≥2 та загальна сума балів ТОХ ≥10 свідчать про вираженість симптомів ХОЗЛ | |||||||
ТОХ містить 8 пунктів, які визначають ступінь погіршення статусу здоров’я при ХОЗЛ. Загальна сума балів може становити від 0 до 40.
У хворих на ХОЗЛ мокротиння виділяється в незначній кількості і має слизовий характер. З часом задишка прогресує, стає постійною і має експіраторний характер. Характерною ознакою ХОЗЛ є діжкоподібна форма грудної клітки; перкуторно визначається коробковий звук, що свідчить про перевагу повітря над щільними елементами легень і є ознакою емфіземи легень. При аускультації визначається ослаблене везикулярне дихання з подовженим видихом (розширені повітрям легені гірше проводять легеневі звуки), можуть визначатися сухі, свистячі, подібні до дзижчання та тріскучі хрипи (рис. 3.3).

Рис. 3.3. Спірографічні показники в нормі та при ХОЗЛ
Інші захворювання, які супроводжуються кашлем і задишкою, наведено на рис. 3.4.
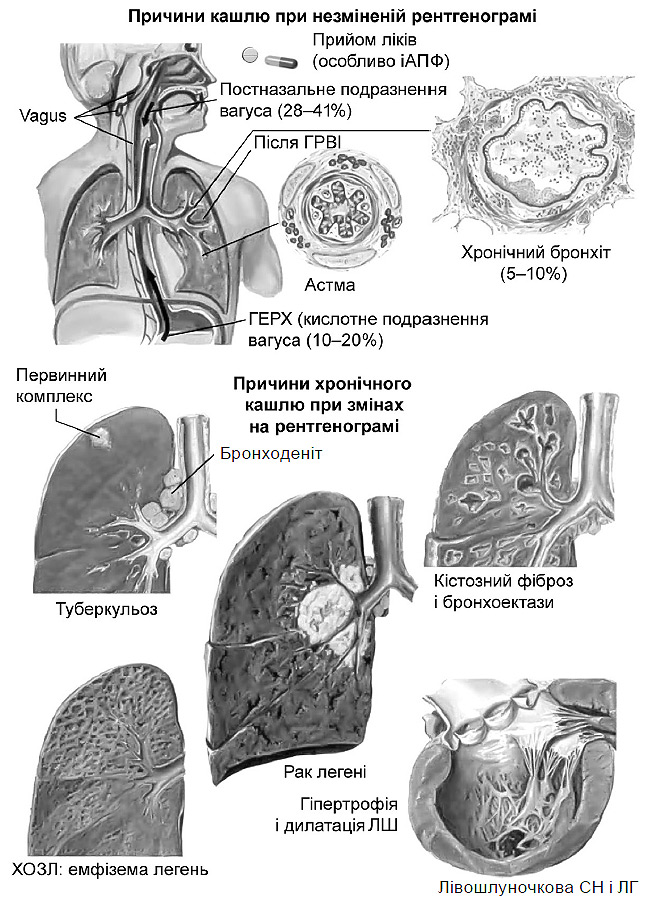
Рис. 3.4. Захворювання, що супроводжуються хаотичним кашлем і задишкою (за Ф. Неттером)
ГЕРХ — гастроезофагеальна рефлюксна хвороба; ГРВІ — гостра респіраторна вірусна інфекція.
Пульс частий, АТ може підвищуватися. Серце прикрите легенями, тож межі відносної тупості серця визначаються важче. Спостерігається зміщення відносної тупості серця вправо. Тони серця послаблені, може визначатися акцент ІІ тону над легеневою артерією.
За тривалого перебігу захворювання можуть з’являтися набряки на ногах, збільшення печінки, що свідчить про хронічну правошлуночкову недостатність.
Рентгенологічне дослідження виявляє легені великого об’єму, низьке стояння куполів діафрагми, вузьку тінь серця, збільшення ретростернального повітряного простору; інколи визначаються емфізематозні були.
За даними дослідження функції зовнішнього дихання, найбільш доступними та інформативними показниками, що свідчать про обструкцію дихальних шляхів, є ОФВ1, ФЖЄЛ, співвідношення ОФВ1/ФЖЄЛ. За допомогою проб із бронхолітиками (сальбутамол, фенотерол) визначають ступінь зворотності бронхообструкції. Якщо під впливом бронхолітика ОФВ1 та інші показники збільшуються на 12%, то проба позитивна і свідчить про зворотну бронхообструкцію. Однак якщо цього збільшення не спостерігається, то це свідчить про незворотні морфологічні зміни в бронхолегеневій системі.
ПОШвид за даними спірографії та пікфлоуметрії не є достатньо інформативним показником бронхообструкції при ХОЗЛ, на відміну від БА. Діагноз ХОЗЛ встановлюється на підставі ОФВ1/ФЖЕЛ <70%.
Лабораторні дослідження при ХОЗЛ малоінформативні. За наявності гнійного компонента мокротиння у хворого може визначатися помірне підвищення ШОЕ, лейкоцитоз, збільшення вмісту в крові серомукоїду, сіалових кислот, СРБ (+). Коли мокротиння гнійне, у ньому визначають багато нейтрофілів.
Лікування хронічного обструктивного захворювання легень
Рішення щодо призначення довготривалої кисневої терапії має базуватися на РаО2 в спокої або SаО2, вимірювання яких здійснюється двічі протягом 3 тиж у хворого в стабільному стані.
Потреба в кисневій терапії оцінюється за наступними критеріями: наявність дуже тяжкої бронхообструкції (ОФВ1 <30% від належного); наявність ціанозу; поліцитемії, периферичних набряків; підвищений тиск у яремній вені; SаО2 ≤92% при диханні повітрям. Можливість застосування довготривалої кисневої терапії повинна також розглядатися у пацієнтів з тяжкою бронхообструкцією (ОФВ1 30–49% від належного). Застосовуються такі види кисневої терапії: тривала, амбулаторна, короткоімпульсна (інтермітуюча) киснева терапія.
Пацієнти з хронічною гіперкапнічною ЛН, що одержують адекватну терапію і потребують застосування допоміжної вентиляції (інвазивної або неінвазивної) при загостренні, або пацієнти з гіперкапнією чи ацидозом при лікуванні кисневою терапією повинні направлятися до спеціалізованого центру для призначення довгострокової неінвазивної вентиляції.
Застосування препаратів у лікуванні ХОЗЛ розглянуто в табл. 3.33.
Таблиця 3.33. Форми і типові дози препаратів у лікуванні ХОЗЛ
| Препарат | Шлях введення | Тривалість дії (годин) |
| β2-Агоніст короткої дії | ||
| Сальбутамол | 100 мкг (ДАІ, АВІ); 2,5/2 мкг/мл розчин для небулайзера | 4–6 |
| Фенотерол | 100 мкг (ДАІ) | 4–6 |
| β2-Агоніст пролонгованої дії | ||
| Індакатерол | 150–300 мкг (СПІ) | 24 |
| Сальметерол | 25 мкг (ДАІ) | 12+ |
| Формотерол | 12 мкг (СПІ) | 12+ |
| Антихолінергетики | ||
| Іпратропію бромід (короткої дії) | 18 мкг (СПІ) | 6–8 |
| Тіотропію бромід (тривалої дії) | 20 мг (ДАІ) | 24+ |
| Комбінація β2-агоніста короткої дії з антихолінергетиком в одному інгаляторі | ||
| Фенотерол/іпратропію бромід | 50/20 мкг (ДАІ) 0,5/0,25 мкг/мл, флакон 20, 40 мл, розчин для небулайзера |
6–8 |
| Метилксантини | ||
| Теофілін | 200 мг, 300 мг для перорального застосування | 10–12 |
| Доксофілін | 400 мг для перорального застосування | > 6 |
| ГК | ||
| Беклометазон | 50, 250 мкг (ДАІ), 100, 200 мкг (ДАІ, АВІ) | 12 |
| Будесонід | 100, 200 мкг (СПІ); 0,25/1; 0,5/1 мг/мл, небули по 2 мл, розчин для небулайзера |
12 |
| Флутиказон | 50, 125 мкг (ДАІ); 0,5/2; 2/2 мг/мл, небули по 2 мл, розчин для небулайзера |
12 |
| Комбінація β2-агоністів тривалої дії з ГК в одному інгаляторі | ||
| Сальметерол/флутиказон | 25/50; 25/125; 25/250 мкг (ДАІ); 50/100; 50/250; 50/500 мкг (СПІ) | 12 |
| Формотерол/будесонід | 4,5/80; 4,5/160 мкг (СПІ) | 24 |
| ГК | ||
| Метилпреднізолон | 4, 8 мг у таблетках для перорального застосування;
порошок для розчину для ін’єкцій по 40, 80, 125, 500, 1000 мг |
24 |
| Преднізолон | 5 мг у таблетках для перорального застосування;
30 мг/мл, ампули для ін’єкцій (мг) по 1 мл |
24 |
| Інгібітор фосфодіестерази-4 | ||
| Рофлуміласт | 500 мкг у таблетках для перорального застосування | 24 |
| НПЗП | ||
| Фенспірид | 80 мг у таблетках для перорального застосування | 8 |
Примітки. ДАІ — дозований аерозольний інгалятор; СПІ — сухий порошковий інгалятор; АВІ — активований вдихом інгалятор.
При лікуванні ХОЗЛ поряд з β2-агоністами застосовують холінолітики (антихолінергічні) препарати — як короткої дії (іпратропію бромід), так і тривалої дії (тіотропію бромід). Холінолітичним препаратам властива тривала дія, вони не спричиняють тахіфілаксію (зниження клінічної ефективності при тривалому застосуванні), тобто мають деякі переваги порівняно з β2-агоністами.
На сьогодні доведена перевага поєднаного застосування β2-агоністів з холінолітиками (іпратропію бромід + фенотерол) порівняно з монотерапією завдяки таким властивостям комбінованих препаратів:
- діють на різні відділи бронхів, тож тривалий бронходилатуючий ефект значно більший;
- зумовлюють потенціювання ефектів, зменшують побічні дії;
- знижують дозування препаратів;
- зменшують загострення ХОЗЛ.
Фенотерол усуває бронхообструкцію в 90% випадків, тоді як комбінація іпратропію броміду і фенотеролу — в 96% випадків, що значно покращує якість життя.
При тривалому застосуванні іпратропію броміду у пацієнтів із ХОЗЛ спостерігається зменшення побічних реакцій з боку системи кровообігу та респіраторної недостатності, покращується функція легень. У 22 клінічних дослідженнях показано, що іпратропію бромід призводить до достовірного зниження смертності.
Проведене в Росії багатоцентрове популяційне дослідження ІКАР-ХОЗЛ дозволило з’ясувати, що ХОЗЛ суттєво негативно впливає на якість життя пацієнтів, перш за все на їхній фізичний статус. Вираженість відхилень залежить від ступеня тяжкості ХОЗЛ, віку пацієнтів, тривалості захворювання, індексу тютюнопаління [21, 32].
Згідно з результатами багатоцентрових досліджень і рекомендаціями доказової медицини, найбільш ефективними препаратами в лікуванні пацієнтів із ХОЗЛ є β2-агоністи, холінолітики короткої та тривалої дії, а також інгаляційні ГК (алгоритм 3.11).
| Алгоритм 3.11. Лікування ХОЗЛ [8]
Крок 1. Бронходилатаційна терапія, яка займає основне місце в симптоматичному лікуванні: 1) β2-агоністи короткої дії: сальбутамол, фенотерол по 2 інгаляції 3–4 рази на добу; 2) пролонговані β2-агоністи: сальметерол по 1–2 інгаляції 1–2 рази на добу; формотерол 1 інгаляція двічі на добу; індакатерол 150–300 мкг 1 раз на добу; 3) антихолінергічні препарати: іпратропію бромід по 2 інгаляції 4 рази на добу впродовж 1 міс; тіотропію бромід по 1 інгаляції 1 раз на добу; глікопіронію бромід 50 мкг 1 раз на добу; 4) комбіновані β2-агоністи короткої дії з антихолінергічними препаратами: іпратропію гідробромід + сальбутамол по 1 інгаляції 4 рази на добу; іпратропію бромід + фенотерол по 2 інгаляції 3–4 рази на добу; 5) метилксантини:
Крок 2. ГК застосовують у плановій базисній терапії при ХОЗЛ ІІІ–IV ступеня. Інгаляційні ГК:
За відсутності ефекту від інгаляційних ГК застосовують преднізолон — 30–40 мг/добу перорально впродовж 10–14 днів. Крок 3. Доцільна комбінація інгаляційних препаратів пролонгованої дії:
Крок 4. Відхаркувальна терапія:
Крок 5. При інфекційному загостренні призначають антибіотики (макроліди, напівсинтетичні пеніциліни, фторхінолони, цефалоспорини ІІІ покоління):
Крок 6. Протирецидивна терапія здійснюється 2 рази на рік; вона включає:
|
Терапія ХОЗЛ зі стабільним перебігом
Загальні принципи:
1. Припинення куріння пацієнтами з ХОЗЛ є одним із найважливіших заходів, оскільки уповільнює рівень зниження ОФВ1 і прогресування симптомів та сприяє підвищенню виживаності.
2. Пацієнтам із ХОЗЛ, у яких зберігається задишка або виникають загострення, незважаючи на застосування β2-агоніста тривалої дії з інгаляційним кортикостероїдом, незалежно від величини ОФВ1 необхідно запропонувати агоніст мускаринових рецепторів тривалої дії на додаток до β2-агоніста тривалої дії з ГК.
3. Пацієнтам зі стабільним ХОЗЛ, із рефрактерною задишкою або загостреннями, що виникають на фоні підтримувальної терапії з агоністами мускаринових рецепторів тривалої дії, незалежно від їх ОФВ1 необхідно розглянути використання β2-агоніста тривалої дії з ГК як доповнення до агоніста мускаринових рецепторів тривалої дії.
Схему застосування препаратів на початку лікування ХОЗЛ наведено в табл. 3.34.
Таблиця 3.34. Початкове фармакологічне лікування ХОЗЛ (GOLD, 2018)
| Характеристика пацієнтів (група) | Перший вибір | Другий вибір | Альтернативний вибір* |
| А
Низький ризик, симптоми маловиражені (мМКД <2, ТОХ <10), ступінь бронхообструкції згідно з GOLD — 1–2 |
Бронхолітики короткої дії за потребою або β2-агоніст короткої дії (сальбутамол, фенотерол), або холінолітик короткої дії (іпратропію бромід), або їх комбінація | Бронхолітики пролонгованої дії: β2-агоніст пролонгованої дії (сальметерол, формотерол) або холінолітик пролонгованої дії (тіотропію бромід) або β2-агоніст короткої дії + холінолітик короткої дії | Теофілін
Доксофілін Фенспірид |
| В
Низький ризик, симптоми більш виражені (мМКД ≥2, ТОХ ≥10), ступінь бронхообструкції згідно з GOLD — 1–2 |
Бронхолітики пролонгованої дії, β2-агоніст пролонгованої дії (сальметерол, формотерол) або холінолітик пролонгованої дії (тіотропію бромід), або холінолітик тривалої дії + ІКС | β2-Агоніст короткої дії (сальбутамол) та/або холінолітик короткої дії.
Теофілін. Доксофілін. Фенспірид |
|
| С
Високий ризик, симптоми менш виражені (мМКД <2, ТОХ <10), ступінь бронхообструкції згідно з GOLD — 3–4 |
ІКС + β2-агоніст пролонгованої дії або холінолітик пролонгованої дії (тіотропію бромід), або холінолітик тривалої дії + β2-агоніст тривалої дії, або ІКС + холінолітик тривалої дії + β2-агоніст тривалої дії | β2-Агоніст короткої дії та/або холінолітик короткої дії.
Теофілін Доксофілін Інгібітор фосфодіестерази-4 |
|
| D
Високий ризик, симптоми більше виражені (мМКД ≥2, ТОХ ≥10), ступінь бронхообструкції згідно з GOLD — 3–4 |
ІКС + β2-агоніст пролонгованої дії (сальметерол/флутиказон) або (формотерол/будесонід) або холінолітик пролонгованої дії | ІКС + комбінація β2-агоніст пролонгованої дії (сальметерол /флутиказон або формотерол/будесонід, або комбінація β2-агоніст пролонгованої дії + ІКС + холінолітик пролонгованої дії або комбінація β2-агоніст пролонгованої дії + ІКС + інгібітор фосфодіестерази-4, або β2-агоніст пролонгованої дії + холінолітик пролонгованої дії, або холінолітик пролонгованої дії + інгібітор фосфодіестерази-4) | β2-агоніст короткої дії (сальбутамол, фенотерол) та/або холінолітик короткої дії (іпратропію бромід).
Теофілін Карбоцистеїн |
Примітки. *Альтернативні препарати можуть застосовуватися окремо або додаватися до препаратів першого та другого вибору; ІКС — інгаляційні кортикостероїди.
Загострення ХОЗЛ
Загострення — це стійке посилення інтенсивності симптомів порівняно із зазвичай стабільним станом, при якому мінливість симптоматики перевищує повсякденну і особливо гостру на початку захворювання. Основні чинники загострення: інфекційні — бактерії, віруси (особливо в зимові місяці); неінфекційні (забруднення повітря).
Загострення ХОЗЛ може проявлятися такими симптомами: посилення задишки, поява гнійного мокротиння; збільшення кількості мокротиння, посилення кашлю, ураження верхніх дихальних шляхів (наприклад тонзиліт), посилення хрипів, відчуття стиснення в грудях, зниження фізичної активності, поява набряків, підвищення втоми, гостре виникнення симптомів.
Додаткові обстеження з метою оцінки тяжкості загострення:
- пульсоксиметрія для визначення потреби та моніторингу кисневої терапії, вимірювання газів в артеріальній крові; необхідна при ознаках гострої або підгострої дихальної недостатності (РаО2 <8,0 кПа (60 мм рт. ст.) на тлі або без РаСО2 >6,7 кПа (50 мм рт. ст.) під час вдихання повітря;
- рентгенографія грудної клітки, ЕКГ, загальний аналіз крові, аналіз мокротиння.
При ХОЗЛ часто виникає загострення різних інфекцій. Тактика підбору антибіотиків при ХОЗЛ залежно від збудника наведена в табл. 3.35.
Таблиця 3.35. Вибір антибіотиків для лікування ХОЗЛ
| Особливості нозологічної форми | Можливі збудники | Антибактеріальна терапія | |
| препарати вибору | альтернативні препарати | ||
| Просте (неускладнене) загострення | H. influenzaе
S. іneumoniaе M. сatarrhalis |
Амоксицилін або кларитроміцин, або азитроміцин | Амоксицилін/клавуланова кислота
Амоксицилін/сульбактам Респіраторні фторхінолони (левофлоксацин, моксифлоксацин, геміфлоксацин) |
Ускладнене загострення з факторами ризику при ОФВ1 35–50%:
|
H. influenzaе
M. сatarrhalis S. pneumoniaе Enterobacteriaceaе |
Ті самі препарати | |
Ускладнене загострення з факторами ризику інфекції P. aeruginosaе:
|
Ті самі + P. aeruginosaе | Антисиньогнійні β-лактами (цефтазидим, цефепім, іміпенем, меропенем)
Респіраторні фторхінолони |
|
У хворих на ХОЗЛ при різних етіологічних збудниках рекомендуються антибіотики, наведені в табл. 3.36.
Таблиця 3.36. Рекомендовані антибіотики при різних етіологічних збудниках у хворих на ХОЗЛ (Європейське товариство клінічної мікробіології та інфекційних захворювань, 2012)
| Патогенний мікроб | Рекомендовані антибіотики |
| Пеніцилінрезистентний S. pneumoniae (мінімальна інгібуюча концентрація >8 мг/дл) | Левофлоксацин, моксифлоксацин, ванкоміцин, тейкопланін, лінезолід |
| Метицилінчутливий золотистий стафілокок (MSSA) | Флуклоксацилін, цефалоспорин ІІ покоління, кліндаміцин, левофлоксацин, моксифлоксацин |
| Метицилінстійкий золотистий стафілокок (MRSA) | Ванкоміцин, тейкопланін + рифампіцин, лінезолід, кліндаміцин (якщо збудник чутливий) |
| Ампіцилінстійкий штам H. іnfluenzaе | Захищений амінопеніцилін, левофлоксацин, моксифлоксацин |
| Мycoplasma pneumoniae | Доксициклін, макролід, левофлоксацин, моксифлоксацин |
| Chlamydophila pneumoniae | Доксициклін, макролід, левофлоксацин, моксифлоксацин |
| Legionella spp. | Левофлоксацин, моксифлоксацин, макролід (краще азитроміцин) + рифампіцин |
| Coxiella burnetii | Доксициклін, левофлоксацин, моксифлоксацин |
| Acinobacter baumanii | Цефалоспорин ІІІ покоління + аміноглікозиди, ампіцилін/сульбактам |
Фармакологічне лікування загострення ХОЗЛ (GOLD, 2018) [44]
Для лікування загострення ХОЗЛ найчастіше застосовують бронходилататори, кортикостероїди та антибіотики.
Бронходилататори. Інгаляційні β2-агоністи короткої дії та антихолінергічні засоби короткої дії — це початкові бронходилататори, рекомендовані для невідкладної терапії загострень у будь-яких пристроях для доставки. В/в метилксантини не рекомендуються через їхні побічні ефекти.
Глюкокортикоїди. Системні ГК при загостренні ХОЗЛ скорочують час відновлення і покращують ОФВ1. Вони також поліпшують оксигенацію і знижують ризик раннього рецидиву. Рекомендована доза — 40 мг преднізолону на добу протягом 5 днів. Терапія пероральним преднізолоном однаково ефективна при в/в введенні. ГК можуть бути менш ефективними для лікування загострень у пацієнтів з низьким рівнем еозинофілів у крові.
Антибіотики. Антибіотики слід призначати пацієнтам із сильними загостреннями, які мають три кардинальні симптоми: збільшення задишки і обсягу мокротиння та гнійного мокротиння; мають два серйозні симптоми, якщо підвищена гнійність мокротиння є одним із двох симптомів, або пацієнт потребує механічної вентиляції (інвазивної чи неінвазивної). Рекомендована тривалість антибактеріальної терапії становить від 5 до 7 днів. Вибір антибіотиків має базуватися на локальній моделі стійкості до бактерій. Звичайне початкове емпіричне лікування — амінопеніцилін з клавулановою кислотою, макролід або тетрациклін.
У нових рекомендаціях запропоновано модель для ініціювання і подальшої ескалації та/або деескалації фармакологічного управління відповідно до індивідуалізованої оцінки симптомів та ризику загострення. У попередніх звітах GOLD рекомендації були надані лише для початкової терапії, однак багато пацієнтів з ХОЗЛ вже отримують лікування і повертаються з постійними симптомами після первинної терапії або, рідше, з усуненням деяких симптомів, які можуть згодом потребувати меншого обсягу терапії. Стратегії ескалації та деескалації фармакологічного управління наведено в табл. 3.37.
Таблиця 3.37. Фармакологічне лікування загострення ХОЗЛ (GOLD, 2018) [44]
| Група пацієнтів | Стратегія фармакологічного лікування |
| Група А | Всій групі пацієнтів необхідно запропонувати бронходилататор, щоб зменшити задишку. Це може бути бронходилататор або короткої, або тривалої дії |
| Група В | Початкова терапія здійснюється бронходилататором тривалої дії. За ефективністю бронходилататори тривалої дії перевершують бронходилататори короткої дії з періодичним прийомом. Немає жодних підстав віддавати перевагу конкретному класу бронходилататорів тривалої дії для зменшення вираженості симптомів; вибір повинен залежати від відповіді пацієнта на окремі препарати. Для лікування хворих із персистуючою задишкою рекомендується використовувати два бронходилататори. Для пацієнтів із сильною задишкою можна віддавати перевагу початковій терапії двома бронходилататорами |
| Група С | Початкова терапія здійснюється одним бронходилататором тривалої дії. Для порівняння холінолітик тривалої дії мав перевагу над β2-агоністом тривалої дії щодо запобігання загостренням; отже, у цій групі варто ініціювати холінолітик тривалої дії. У пацієнтів із постійними загостреннями може бути корисним додавання другого бронходилататора тривалої дії (β2-агоніста тривалої дії/холінолітика тривалої дії) або комбінування β2-агоніста тривалої дії та інгаляційного ГК. Оскільки ГК підвищують ризик розвитку пневмонії, основний вибір — β2-агоніст тривалої дії/холінолітик тривалої дії |
| Група D | Рекомендується ініціювати комбінацію β2-агоніста тривалої дії/холінолітика тривалої дії, оскільки, за результатами досліджень, комбінація β2-агоніста тривалої дії/холінолітика тривалої дії показала позитивні результати порівняно з одним бронходилататором. Комбінація β2-агоніста тривалої дії/холінолітика тривалої дії була більш ефективною для профілактики загострень у пацієнтів групи D, ніж комбінація β2-агоніста тривалої дії/інгаляційного ГК. Пацієнти групи D мають підвищений ризик розвитку пневмонії при лікуванні інгаляційними ГК. Якщо пацієнти, яких лікують β2-агоністом тривалої дії/холінолітиком тривалої дії/інгаляційним ГК, все ще мають загострення, можна розглянути наступні варіанти:
|
Доведено, що тривале застосування антибіотиків з метою профілактики загострень не впливає на частоту їх виникнення: прийом хворими антибіотиків у зимові місяці протягом 5 років дослідження не вплинув на частоту загострень.
Інші лікувальні заходи. Залежно від стану пацієнта слід передбачати підтримання належного водного балансу. Особливу увагу слід приділяти введенню діуретиків; застосуванню антикоагулянтів; лікуванню супутніх захворювань і корекції харчування. Протягом усього лікування медичні працівники повинні максимально посилити обмежувальні заходи проти активного куріння тютюну.
Необхідно пам’ятати, що при ХОЗЛ зниження тиску в легеневій артерії вазоактивними засобами нерідко збільшує ступінь гіпоксемії та сприяє негативним змінам газового складу крові, нівелюючи захисний ефект гіпоксемічної вазоконстрикції. Водночас розвиток ЛГ у пацієнтів із ХОЗЛ, як правило, не потребує медикаментозного лікування. У цих випадках доцільною є оксигенотерапія. Така тактика лікування пацієнтів із ХОЗЛ і ЛГ рекомендована конгресом Європейського респіраторного товариства.
Рекомендації доказової медицини
З-поміж усіх протизапальних засобів при ХОЗЛ найбільш ефективними є ГК, які гальмують активацію прозапальних клітин у легенях, знижують рівень протизапальних медіаторів, чинять антиоксидантну дію. Однак при ХОЗЛ вони менш ефективні, ніж при БА, і зменшують обструкцію тільки в 10–30% пацієнтів. Згідно з рекомендаціями доказової медицини, інгаляційні ГК при тривалому застосуванні у пацієнтів із ХОЗЛ зменшують загострення на 25% (РКД EUROSCOP, ISOLDE).
Найбільш ефективними у лікуванні ХОЗЛ є інгаляції β2-агоністів та/або холінолітиків (рівень доказовості А).
Згідно з останніми міжнародними і національними рекомендаціями, а також даними РКД, присвячених ХОЗЛ, тіотропію бромід є одним із основних бронходилататорів; він чинить бронхорозширювальну і протизапальну дію та сприяє нормалізації показників апарату дихання [11].
Позитивною рисою β2-агоністів є швидка дія; перевагами антихолінергічних засобів — висока безпека і добра переносимість. У таких комбінованих препаратів, як іпратропію бромід + фенотерол або іпратропію бромід + сальбутамол, перевагою є те, що вони діють на різні відділи бронхів (антихолінергічні препарати переважно діють на проксимальні, β2-агоністи — на дистальні відділи); вони більш ефективні і рідше спричиняють побічні реакції, що підтверджено доказовою медициною і даними РКД. У них доведено, що комбіноване лікування більш ефективне, ніж монотерапія. Отже, можна зробити висновок, що у хворих із тяжким перебігом ХОЗЛ інгаляційна терапія комбінацією β2-агоніст + холінолітик може розглядатися як терапія вибору, оскільки покращує функціональну здатність легень, зменшує задишку та побічні реакції на препарати [16, 33, 44].
β2-Агоністи сальбутамол і формотерол розслаблюють гладкі м’язи бронхів завдяки стимуляції β2-адренорецепторів, які підвищують рівень циклічного аденозинмонофосфату і спричиняють функціональний антагонізм. Поряд з цим лікування інгаляційними бронходилататорами тривалої дії може доповнюватися прийомом перорально пролонгованих теофілінів, що сприяють зменшенню вираженості симптомів ХОЗЛ (рівень доказовості В).
В усіх редакціях GOLD і національних стандартах багатьох країн головним засобом у лікуванні ХОЗЛ визнано бронходилататори.
Дані метааналізу та РКД BRONCUS показали, що застосування ацетилцистеїну в дозі 400–1200 мг/добу впродовж 6 міс знижує ризик загострення ХОЗЛ приблизно на 50% у результаті протизапальної, муколітичної та антиоксидантної дії препарату.
У РКД TORCH показано, що комбінація ГК і сальбутамолу при ХОЗЛ зумовлює зменшення ризику смерті на 17,5% (р<0,05) і зниження загальної смертності на 2,6%.
Однак з-поміж усіх протизапальних препаратів найбільш ефективними є ГК, які призводять до зменшення нападів ядухи та задишки на 34% при застосуванні препаратів упродовж року; при трирічному застосуванні — на 25% (SSOLDE). Усі ці дані лягли в основу рекомендації GOLD щодо застосування інгаляційних ГК при ХОЗЛ.
Виражена протизапальна дія властива препарату фенспіриду, який призначають по 80 мг 2 рази на добу упродовж 6 міс. Він пригнічує утворення простагландинів, тромбоксану та лейкотрієнів, проте цей препарат не є стероїдним гормоном.
У першому РКД INSPІRE вивчали вплив препаратів із протизапальною дією (комбінація сальметерол/флутиказону пропіонат у дозі 50/500 мкг 2 рази на добу) у порівнянні з бронхолітиком тіотропію бромідом у дозі 18 мкг 1 раз на добу. У групі хворих, які приймали сальметерол/флутиказон, було менше загострень у порівнянні з тими, хто лікувався тіотропію бромідом, але в першій групі пацієнтів частіше призначали антибактеріальну терапію. У дослідженні TORCH вказується, що при ХОЗЛ на фоні застосування комбінації сальметеролу/флутиказону пропіонату також відмічалася підвищена частота розвитку пневмонії, але вона не призводила до погіршення стану хворих у цілому і не впливала на показник смертності. Остаточна природа цих епізодів і причини їх виникнення потребують подальшого вивчення.
Водночас у РКД OPTIMAL не виявлено переваг комбінованої терапії над монотерапією.
У РКД VPLIFT (2008) показано, що 4-річне застосування тіотропію в лікуванні пацієнтів із ХОЗЛ позитивно впливало на клінічний перебіг хвороби, сприяло достовірному поліпшенню функції легень, якості життя і скороченню загострень. Протягом 4 років і 30 днів застосування тіотропію на 14% знижувало ризик розвитку загострень, зменшувало кількість випадків госпіталізацій і ЛН. При цьому ризик смерті після лікування тіотропієм зменшився на 16%.
Результати масштабних досліджень показали, що інгаляційні ГК (флутиказону пропіонат, будесонід) покращують показники після бронходилатаційного ОФВ1 та бронхіальну реактивність при стабільному ХОЗЛ, знижують частоту загострень, а також покращують якість життя у пацієнтів із тяжким перебігом захворювання.
Можливий тривалий вплив інгаляційних ГК і β2-агоністів тривалої дії на смертність вивчався у декількох фармакоепідеміологічних дослідженнях. Аналіз цих досліджень у Канаді і Великобританії показав, що флутиказону пропіонат при ХОЗЛ значно знижує рівень смертності. У дослідженні TORCH 35% смертельних випадків при ХОЗЛ були пов’язані зі станом дихальної системи, 27% — ССЗ, 21% — раком, 10% — іншими причинами.
У РКД VPLIFT вивчали ефективність тіотропію броміду при ХОЗЛ. Показано, що тіотропій забезпечує тривалу 24-годинну бронхорозширювальну дію, а постійне застосування цього препарату підвищує толерантність до фізичного навантаження, зменшує задишку, кількість загострень і покращує якість життя пацієнтів.
Останнім часом було проведено низку РКД при загостренні ХОЗЛ і визначено роль ГК у таких пацієнтів. Згідно з даними цих досліджень, системні (пероральні та в/в) ГК при ХОЗЛ покращують функціональні показники, знижують смертність, подовжують тривалість та покращують якість життя.
Застосування інгаляційних ГК протягом року зумовлює зниження тяжкості загострень ХОЗЛ на 35% (PKD TRIESTAN); трирічне застосування — на 25% (ISOLDE), а застосування великих доз тріамцинолону протягом 4 років — на 53% (Lung Health Study II). У метааналізі ISOLDE показано, що при лікуванні ХОЗЛ флутиказоном наприкінці 2-го року досягнуто кращого ефекту, ніж у групі плацебо.
У РКД TRISTAN доведено, що застосування комбінованого препарату, який містить сальметерол і флутиказон, сприяло значному покращенню бронхіальної прохідності, зниженню смертності і зменшенню кількості випадків повторної госпіталізації, ніж при монотерапії цими препаратами.
У подвійному сліпому РКД TORCH (6000 пацієнтів протягом 3 років) доведено, що при застосуванні комбінованого інгаляційного препарату (сальметерол + флутиказону пропіонат) відмічалися зниження частоти загострень ХОЗЛ на 25%, достовірне покращення якості життя (р<0,001), зниження смертності на 2,6%. Така комбінована терапія при ХОЗЛ дає наступні позитивні результати:
1) зменшення спазму гладких м’язів бронхів;
2) зменшення кількості нейтрофілів, макрофагів і Т-клітин;
3) зниження рівня маркерів запалення (IL-β, TNF-α);
4) зменшення легеневого фіброзу;
5) покращення мукоциліарного транспорту.
Кромони (кромоглікат натрію) менш ефективні, ніж β2-агоністи, які забезпечують захист на 50–60% тільки протягом 1–2 год, але мають низку переваг, оскільки їх можна застосовувати часто і тривало, а численні інгаляції не викликають побічних реакцій та толерантності. Кромони застосовують при алергічних захворюваннях, легкій формі БА, астмі фізичного навантаження. Їх можна використовувати в моно- і комбінованій терапії [35, 44].
У якості антибіотика вибору при загостренні ХОЗЛ рекомендується амінопеніцилін (амоксицилін) або макролід, або респіраторний фторхінолон для перорального застосування, який призначається у разі неефективності β-лактамів і макролідів або алергії на них.
Якщо збудниками захворювання є H. influenzaе, представники сімейства Enterobacteriасae, а також S. pneumoniae, то антибіотиками вибору є захищені амінопеніциліни або цефалоспорини ІІ покоління, або респіраторний фторхінолон для перорального застосування.
Коли збудником виступає P. аeruginosae, застосовують фторхінолони ІІ покоління (ципрофлоксацин) або респіраторний фторхінолон левофлоксацин у високій дозі, або β-лактам з антисиньогнійною активністю в комбінації з аміноглікозидом.
Препарати теофіліну при загостренні ХОЗЛ розглядаються як засоби другої чи третьої лінії і можуть бути додані тільки при регулярній інгаляційній терапії у разі недостатньої ефективності β2-агоністів і антихолінергічних препаратів [8, 9, 32].
Отож, результати масштабних досліджень свідчать про те, що застосування фіксованих комбінацій інгаляційних ГК і β2-агоністів тривалої дії має суттєві переваги над монотерапією цими препаратами.
Алгоритм ведення хворих із загостренням ХОЗЛ в амбулаторних умовах:
1) ініціювати або посилити бронхолітичну терапію (вищі доза та частота прийому, поєднання різних бронхолітиків (β2-агоністи, холінолітики), застосування небулайзера або спейсера);
2) у разі інфекційного загострення додати антибіотики;
3) повторно оцінити стан;
4) якщо спостерігається зменшення вираженості симптомів та ознак загострення, продовжувати призначене лікування; після закінчення загострення слід переглянути терапію;
5) якщо покращення симптомів не спостерігається, додати пероральні ГК (30–40 мг преднізолону на 7–10 днів);
6) повторно оцінити стан;
7) у разі погіршення симптомів загострення госпіталізувати хворого.
Діагностику та лікування ЛГ і правошлуночкової недостатності при ХОЗЛ наведено в алгоритмах 3.12, 3.13.
| Алгоритм 3.12. Діагностика ЛГ і правошлуночкової недостатності у хворих на ХОЗЛ [9]
Крок 1. З’ясування клінічної картини і аускультації серця. Клінічна картина і аускультація серця: кашель, експіраторна задишка, набряки на ногах, збільшення печінки, ослаблене дихання; сухі, свистячі, тріскучі та подібні до дзижчання хрипи. Крок 2. Інструментальні критерії діагностики ЛГ і правошлуночкової недостатності у хворих на ХОЗЛ: 1. ЕКГ-критерії: діагностуються ознаки гіпертрофії ПШ, P-pulmonale та різні (переважно суправентрикулярні) аритмії, а також БПНПГ. ЕКГ-зміни при легеневому серці:
2. ЕхоКГ-критерії: у хворих на ХОЗЛ рівень САТ в легеневій артерії перевищує 30 мм рт. ст.; визначається розширення порожнин ПШ і (рідко) правого передсердя; систолічна функція ПШ значно знижена. 3. Радіонуклідна вентрикулографія: збільшення товщини стінки ПШ і його порожнини. 4. МРТ: збільшення товщини стінки ПШ і його порожнини. |
| Алгоритм 3.13. Лікування ЛГ і правошлуночкової недостатності у хворих на ХОЗЛ [8]
Крок 1. Оксигенотерапія. Показання до тривалої оксигенотерапії при ХОЗЛ
Якщо тривала гіперкапнія призвела до пригнічення дихального центру, для стимуляції дихання доцільно використати стимулятори периферичних хеморецепторів. Крок 2. Використання бронходилататорів. Тривалість і схема призначення інгаляційних бронходилататорів
Теофілін — 500 мг в/в повільно протягом 20–40 хв. Крок 3. Використання вазодилататорів з метою зменшення бронхообструктивного синдрому або усунення суправентрикулярних аритмій. АК дилтіазем (початкова доза — 180–240 мг/добу, добова — 360–420 мг). Крок 4. Застосування препаратів для лікування правошлуночкової недостатності:
Крок 5. Флеботомія у хворих з підвищеною в’язкістю крові (гематокрит >55%). |
||||||||||||||||||||||||||
Прогноз. ХОЗЛ — частково зворотна патологія; адекватне і тривале лікування дозволяє сповільнити її прогресування. Хворі на ХОЗЛ часто помирають від ЛН (4–35% випадків), раку легені (20–33%), кардіоваскулярних ускладнень (25% випадків), яким нині приділяється велика увага. Дані літератури та власний досвід авторів стосовно кардіоваскулярних ускладнень узагальнено в табл. 3.38.
Таблиця 3.38. Фактори ризику кардіоваскуляторних ускладнень при ХОЗЛ
| Загальні фактори ризику | Кардіальні фактори ризику | Кардіоваскуляторні ускладнення |
|
|
|
Чим більше кардіальних факторів ризику у хворого на ХОЗЛ, тим частіше виникають кардіоваскулярні ускладнення. За даними міжнародної статистики, госпітальна смертність хворих із загостренням ХОЗЛ становить 8%, а через рік після загострення — 23%.
Попри те що ХОЗЛ є прогресуючим захворюванням, правильно підібрані і вчасно призначені препарати та реабілітація можуть значно уповільнити розвиток, запобігти виникненню ускладнень і покращити якість життя пацієнтів.
Профілактика. Первинна профілактика включає заходи щодо екологічного оздоровлення зовнішнього середовища і загартування організму людини. Вторинна профілактика ХОЗЛ передбачає проведення протирецидивного лікування в осінні та зимові місяці, коли підвищується ризик респіраторно-вірусних захворювань органів дихання. Припинення паління є найбільш ефективним і економічно обґрунтованим засобом, що дозволяє знизити ризик розвитку ХОЗЛ і запобігти прогресуванню ХОЗЛ (рівень доказовості А).