Мідіана (Midiana)
Мідіана інструкція із застосування
Склад
Допоміжні речовини: лактози моногідрат, крохмаль кукурудзяний, крохмаль прежелатинізований, повідон К-25, магнію стеарат; оболонка: Опадрай ІІ білий (спирт полівініловий, титану діоксид (Е171), макрогол, тальк, лецитин (соєвий)).
Дроспіренон - 3 мг
Етинілестрадіол - 0,03 мг
Фармакологічні властивості
фармакодинаміка. Контрацептивний ефект таблеток Мідіана ґрунтується на взаємодії різних факторів, найважливішими з яких є гальмування овуляції і зміна ендометрію.
Мідіана, таблетки, вкриті плівковою оболонкою, — це комбінований пероральний контрацептив (КПК), що містить етинілестрадіол і прогестоген дроспіренон. У терапевтичній дозі дроспіренон також володіє антиандрогенними і легкими антимінералокортикоїдними властивостями. Він позбавлений будь-якої естрогенної, глюкокортикоїдної та антиглюкокортикоїдної активності. Це забезпечує дроспіренону фармакологічний профіль, дуже схожий на природний натуральний гормон прогестерон.
Легкі антимінералокортикоїдні властивості таблеток Мідіана призводять до легкого антимінералокортикоїдного ефекту.
Індекс Перля контрацептивних невдач для препарату становить 0,09 (верхній двосторонній 95% довірчий інтервал (ДІ) — 0,32).
Загальний індекс Перля (контрацептивні невдачі + помилки з боку пацієнток) для препарату становить 0,57 (верхній двосторонній 95% ДІ — 0,90).
Фармакокінетика
Дроспіренон
Всмоктування. При пероральному прийомі дроспіренон швидко і майже повністю абсорбується. Cmax активної речовини в сироватці крові, що дорівнює 38 нг/мл, досягається через 1–2 год після одноразового прийому. Біодоступність дроспіренону коливається в діапазоні 76–85%. Одночасне вживання їжі не впливає на біодоступність дроспіренону.
Розподіл. Після перорального прийому спостерігається зниження рівня дроспіренону в сироватці крові, яке характеризується Т1/2 тривалістю 31 год. Дроспіренон зв’язується зі сироватковим альбуміном та не зв’язується з глобуліном, що зв’язує статеві гормони (ГЗСГ), або кортикостероїдзв’язувальним глобуліном (КЗГ).
Тільки 3–5 % від загальної сироваткової концентрації активної речовини являє собою вільний гормон. Індуковане етинілестрадіолом підвищення ГЗСГ не впливає на зв’язування дроспіренону білками сироватки крові. Середній уявний об’єм розподілу становить 3,7±1,2 л/кг.
Біотрансформація. Після перорального прийому дроспіренон екстенсивно метаболізується. Більшість метаболітів у плазмі крові представлені кислотними формами дроспіренону, отриманими при відкритті лактонового кільця, та 4,5-дигідро-дроспіренон-3-сульфатом, утворюваним шляхом відновлення і наступного сульфатування. Дроспіренон також піддається окисному метаболізму, що каталізується за допомогою CYP 3A4. В умовах in vitro була відзначена здатність лікарського засобу пригнічувати активність даного ізоферменту, а також ізоферментів системи цитохрому P450 1A1, 2C9 і 2C19.
Виведення. Швидкість метаболічного кліренсу дроспіренону в сироватці крові становить 1,5±0,2 мл/хв/кг. Дроспіренон виділяється лише у слідових кількостях у незміненому стані. Метаболіти дроспіренону екскретуються з калом і сечею у співвідношенні приблизно 1,2:1,4. Т½ для виведення метаболітів із сечею та калом становить приблизно 40 год.
Рівноважна концентрація. Під час одного циклу лікування максимальна рівноважна концентрація дроспіренону в сироватці крові (приблизно 70 нг/мл) досягається через 8 днів застосування. Концентрація дроспіренону в сироватці крові збільшується приблизно у 3 рази внаслідок існуючого співвідношення кінцевого Т½ та інтервалу дозування, що використовується.
Етинілестрадіол
Всмоктування. Етинілестрадіол після перорального прийому швидко і повністю абсорбується. Cmax в сироватці крові після одноразового перорального прийому досягається через 1–2 год і становить приблизно 33 пг/мл. Абсолютна біодоступність у результаті пресистемної кон’югації та ефекту першого проходження через печінку становить приблизно 60%. Одночасне вживання їжі знижувало біодоступність етинілестрадіолу приблизно на 25% у досліджуваних жінок, при цьому в інших не спостерігали жодних змін.
Розподіл. Після перорального прийому спостерігається двофазне зниження рівня етинілестрадіолу в сироватці крові, яке характеризується Т½ тривалістю приблизно 24 год. Етинілестрадіол сильно, але неспецифічно зв’язується з білками плазми крові (приблизно 98,5%) та індукує підвищення рівня ГЗСГ і КЗГ у сироватці крові. Очікуваний об’єм розподілу етинілестрадіолу становить приблизно 5 л/кг.
Біотрансформація. Етинілестрадіол піддається значному метаболізму в кишечнику та первинному метаболізму в печінці. Етинілестрадіол метаболізується насамперед ароматичним гідроксилюванням, але утворюється широкий спектр гідроксильних і метильних метаболітів, які наявні у вигляді вільних метаболітів та кон’югатів з глюкуронідами та сульфатами. Рівень метаболічного кліренсу етинілестрадіолу становить приблизно 5 мл/хв/кг. In vitro етинілестрадіол є оборотним інгібітором CYP 2C19, CYP 1A1 та CYP 1A2, а також інгібітором CYP 3A4/5, CYP 2C8 і CYP 2J2.
Виведення. Етинілестрадіол майже не виводиться в незміненому стані. Метаболіти етинілестрадіолу виводяться з сечею і жовчю у співвідношенні 4:6. Т½ для метаболітів становить приблизно 1 добу.
Рівноважна концентрація. Стан рівноважної концентрації досягається протягом другої половини циклу лікування, причому рівень етинілестрадіолу в сироватці крові акумулюється з кратністю приблизно 1,4–2,1.
Окремі категорії населення.
Вплив на функцію нирок. Рівноважний рівень дроспіренону в сироватці крові у жінок з легким ступенем ниркової недостатності (кліренс креатиніну 50–80 мл/хв) був порівнянний з таким у жінок з нормальною функцією нирок (>80 мл/хв). Рівень дроспіренону в сироватці крові в середньому був на 37% вищим у жінок із середнім ступенем ниркової недостатності (CLcr = 30–50 мл/хв) порівняно з таким у жінок з нормальною функцією нирок. Лікування дроспіреноном добре переносилося жінками і з легким, і з середнім ступенем ниркової недостатності.
Лікування дроспіреноном не мало клінічно значущого впливу на концентрацію калію в сироватці крові.
Вплив на функцію печінки. Кліренс після перорального прийому у добровольців з помірною печінковою недостатністю був знижений приблизно на 50% порівняно з людьми з нормальною функцією печінки.
Зазначене зменшення кліренсу дроспіренону в добровольців з помірною нирковою недостатністю не призводить до будь-яких значущих розходжень щодо концентрації калію в сироватці крові.
Навіть при цукровому діабеті та одночасному лікуванні спіронолактоном (два чинники, які можуть спровокувати гіперкаліємію у пацієнта) не відзначалося збільшення концентрації калію в сироватці крові вище верхньої межі норми.
Можна зробити висновок, що комбінація дроспіренон/етинілестрадіол добре переноситься пацієнтами з помірною печінковою недостатністю (клас В за класифікацією Чайлда — П’ю).
Етнічні групи. Клінічно значущих відмінностей у фармакокінетиці дроспіренону або етинілестрадіолу між жінками європейської та азіатської рас відзначено не було.
Показання Мідіана
пероральна контрацепція
Застосування Мідіана
перорально.
Дозування. Таблетки необхідно приймати щодня приблизно в один і той же час, у разі необхідності запиваючи невеликою кількістю рідини, у послідовності, зазначеній на блістерній упаковці. Необхідно приймати по 1 таблетці на добу протягом 21-го дня поспіль. Кожну наступну упаковку слід починати після 7-денної перерви у прийомі таблеток, протягом якої зазвичай настає менструальноподібна кровотеча. Вона зазвичай починається через 2–3 дні після прийому останньої таблетки і може не закінчитися до початку прийому таблеток з наступної упаковки.
Як розпочати застосування препарату Мідіана
Якщо гормональні контрацептиви у попередній період (минулий місяць) не застосовували. Прийом лікарського засобу Мідіана слід розпочинати у перший день природного циклу жінки (тобто у перший день менструальної кровотечі).
Перехід з іншого комбінованого гормонального контрацептива (КПК, вагінальне кільце або трансдермальний пластир). Бажано, щоб жінка почала прийом таблеток Мідіана на наступний день після прийому останньої активної таблетки попереднього КПК; у таких випадках прийом Мідіани не слід починати пізніше наступного дня після звичної перерви у прийомі таблеток або прийому неактивних таблеток попереднього КПК. При переході з вагінального кільця або трансдермального пластиру прийом препарату Мідіана бажано розпочинати в день видалення попереднього засобу; у таких випадках прийом препарату Мідіана слід розпочинати не пізніше запланованої процедури переходу.
Перехід з методу, який базується на застосуванні лише прогестогену (таблетки, що містять тільки прогестоген, ін’єкції, імплант) або внутрішньоматкової системи з прогестагеном. Жінка може розпочати приймати препарат Мідіана у будь-який день після припинення прийому таблеток, що містять тільки прогестоген (у разі імпланта або внутрішньоматкової системи — у день їх видалення, у випадку ін’єкції — замість наступної ін’єкції). Однак у всіх випадках рекомендується додатково використовувати бар’єрний метод контрацепції протягом перших 7 днів прийому препарату.
Після аборту в І триместрі вагітності. Прийом препарату слід розпочати негайно в той же день після операції. У такому випадку немає необхідності застосовувати додаткові засоби контрацепції.
Після пологів або аборту у ІІ триместрі вагітності. У випадку годування грудьми див. Застосування у період вагітності або годування грудьми.
Жінкам необхідно рекомендувати розпочинати прийом препарату Мідіана з 21–28-го дня після пологів або аборту у ІІ триместрі вагітності. Якщо жінка пізніше починає прийом таблеток, слід рекомендувати додатково використовувати бар’єрний метод контрацепції протягом перших 7 днів прийому таблеток. Однак, якщо статевий акт уже відбувся, то перед початком застосування КПК слід виключити можливу вагітність або жінці слід дочекатися першої менструації.
Що робити у випадку пропуску прийому таблетки.
Якщо запізнення у прийомі будь-якої таблетки не перевищує 12 год, контрацептивна дія препарату не знижується. Пропущену таблетку треба прийняти одразу, як тільки це з’ясувалося. Наступну таблетку з цієї упаковки слід приймати у звичний час.
Якщо запізнення з прийомом забутої таблетки перевищує 12 год, контрацептивний захист може зменшитися.
У випадку пропуску прийому таблетки необхідно керуватися двома основними правилами:
1. Перерва у прийомі таблеток ніколи не може становити більше 7 днів.
2. Адекватне пригнічення системи гіпоталамус-гіпофіз-яєчники досягається безперервним прийомом таблеток протягом 7 днів.
Відповідно до цього у повсякденному житті слід керуватися такими рекомендаціями:
1-й тиждень. Жінка повинна прийняти останню пропущену таблетку якомога швидше, навіть якщо доведеться прийняти 2 таблетки одночасно. Після цього вона продовжує приймати таблетки у звичайний час. Крім того, протягом наступних 7 днів слід використовувати бар’єрний метод контрацепції, наприклад, презерватив. У разі, якщо у попередні 7 днів відбувся статевий акт, слід враховувати можливість настання вагітності. Чим більше таблеток пропущено і чим ближче перерва у прийомі препарату, тим вищий ризик вагітності.
2-й тиждень. Жінка повинна прийняти останню пропущену таблетку якомога швидше, як тільки згадає про пропуск, навіть якщо доведеться прийняти 2 таблетки одночасно. Після цього вона продовжує приймати таблетки у звичайний час. За умови, що жінка правильно приймала таблетки протягом 7 днів перед пропуском, немає необхідності застосовувати додаткові протизаплідні засоби. В іншому разі або якщо пропущено більше 1 таблетки, рекомендується додатково використовувати бар’єрний метод контрацепції протягом 7 днів.
3-й тиждень. Вірогідність зниження контрацептивного ефекту значна через майбутню перерву прийому таблеток у 7 днів. Однак при дотриманні нижчезазначеної схеми прийому таблеток можна уникнути зниження контрацептивного захисту. Якщо дотримуватися одного з наступних варіантів, то не виникне необхідності застосовувати додаткові контрацептивні засоби за умови правильного прийому таблеток протягом 7 днів до пропуску. В іншому випадку рекомендується дотримуватися першого з наступних варіантів і використовувати додаткові методи протягом наступних 7 днів.
1. Жінка повинна прийняти останню пропущену таблетку якомога швидше, як тільки згадає про пропуск, навіть якщо доведеться прийняти 2 таблетки одночасно. Після цього вона продовжує приймати таблетки у звичайний час. Таблетки з нової упаковки слід почати приймати одразу ж після закінчення попередньої, тобто не повинно бути перерви між прийомом таблеток з обох упаковок. Малоймовірно, що у жінки розпочнеться менструальноподібна кровотеча до закінчення прийому таблеток з другої упаковки, хоча під час прийому таблеток можуть спостерігатися мажучі кров’янисті виділення або проривна кровотеча.
2. Жінці можна також порадити припинити прийом таблеток з поточної упаковки. У такому випадку перерва в прийомі препарату повинна становити до 7 днів, включаючи дні пропуску таблеток; прийом таблеток слід почати з наступної нової упаковки.
Якщо жінка пропустила приймання таблеток і у неї відсутня менструальноподібна кровотеча під час першої звичайної перерви у прийманні препарату, слід розглянути імовірність вагітності.
Рекомендації у випадку порушень з боку ШКТ. У разі тяжких порушень з боку ШКТ (блювання, діарея) можливе неповне всмоктування препарату; у такому разі слід застосовувати додаткові засоби контрацепції.
Якщо протягом 3–4 год після прийому таблетки сталося блювання, необхідно якомога швидше прийняти нову таблетку, що заміняє попередню. Нову таблетку, якщо можливо, необхідно прийняти впродовж 12 год після звичайного часу прийому. Якщо пройшло більше 12 год, необхідно дотримуватися правил прийому препарату, зазначених у розділі Що робити у випадку пропуску прийому таблетки. Якщо жінка не хоче змінювати свою звичайну схему прийому препарату, їй необхідно прийняти додаткову (і) таблетку(и) з іншої упаковки.
Як змінити час виникнення кровотечі відміни. Щоб затримати день початку менструації, жінці слід продовжувати приймати таблетки Мідіана з нової упаковки і не робити перерви у застосуванні препарату. При бажанні термін прийому можна продовжити аж до закінчення таблеток із другої упаковки. При цьому можуть спостерігатися проривна кровотеча або мажучі кров’янисті виділення. Звичайний прийом препарату Мідіана відновлюється після 7-денної перерви у прийомі таблеток.
Щоб змістити час настання менструації на інший день тижня, рекомендується скоротити перерву в прийомі таблеток на стільки днів, на скільки бажано. Слід зазначити, що чим коротшою буде перерва, тим частіше спостерігається відсутність менструальноподібної кровотечі та проривної кровотечі або мажучих кров’янистих виділень протягом прийому таблеток з другої упаковки (як у випадку затримки настання кровотечі відміни). Окремі категорії пацієнтів
Пацієнтки літнього віку. Не застосовувати. Препарат Мідіана не показаний після настання менопаузи.
Пацієнтки з порушеннями функції печінки. Препарат Мідіана протипоказаний жінкам з порушенням функції печінки (див. ПРОТИПОКАЗАННЯ).
Пацієнтки з порушенням функції нирок. Препарат Мідіана, таблетки, вкриті плівковою оболонкою, протипоказаний жінкам з тяжкою ХНН або ГНН (див. ПРОТИПОКАЗАННЯ).
Діти. Препарат Мідіана показаний для застосування тільки після настання першої менструації. На основі епідеміологічних даних, зібраних більше ніж у 2000 підлітків віком до 18 років, немає даних, що демонструють різницю у безпеці та ефективності застосування у цієї групи пацієнток порівняно з жінками віком від 18 років.
Протипоказання
КПК не можна застосовувати у разі наявності хоча б одного з нижчезазначених станів. У разі, якщо будь-який із цих станів виникає вперше під час застосування КПК, прийом препарату слід негайно припинити.
КПК не слід застосовувати за наявності таких станів:
– підвищена чутливість до діючих речовин або до будь-якої з допоміжних речовин лікарського засобу (див. СКЛАД);
– підвищена чутливість до арахісу або сої;
– наявність або ризик виникнення венозної тромбоемболії (ВТЕ):
• венозна тромбоемболія — наявна ВТЕ, зокрема внаслідок терапії антикоагулянтами або в анамнезі (наприклад, тромбоз глибоких вен (ТГВ) або тромбоемболія легеневої артерії (ТЕЛА));
• відома спадкова або набута схильність до ВТЕ, наприклад резистентність до активованого протеїну С (у тому числі мутація фактора V Лейдена), дефіцит антитромбіну III, дефіцит протеїну С, дефіцит протеїну S;
• велике оперативне втручання із тривалою іммобілізацією (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ);
• високий ризик ВТЕ внаслідок наявності множинних факторів ризику (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ);
– наявність або ризик розвитку артеріальної тромбоемболії (АТЕ):
• артеріальна тромбоемболія — наявність АТЕ на даний час або в анамнезі (наприклад інфаркт міокарда), або продромальний стан (наприклад стенокардія);
• порушення мозкового кровообігу — інсульт на даний час або в анамнезі, наявність продромального стану (наприклад транзиторна ішемічна атака (ТІА));
• відома спадкова або набута схильність до розвитку АТЕ, така як гіпергомоцистеїнемія та наявність антифосфоліпідних антитіл (антикардіоліпінові антитіла, вовчаковий антикоагулянт);
• мігрень із вогнищевими неврологічними симптомами в анамнезі;
• високий ризик АТЕ внаслідок наявності численних факторів ризику (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ) або внаслідок наявності одного з таких серйозних факторів ризику, як цукровий діабет із судинними ускладненнями; тяжка АГ; тяжка дисліпопротеїнемія.
– наявність тяжкого захворювання печінки на даний час або в анамнезі, поки показники функції печінки не повернулися в межі норми;
– ниркова недостатність тяжкого ступеня або ГНН;
– наявність пухлин печінки (доброякісних або злоякісних) на даний час або в анамнезі;
– відомі або підозрювані злоякісні пухлини (наприклад статевих органів або молочних залоз), залежні від статевих гормонів;
– вагінальна кровотеча нез’ясованої етіології;
– підозрювана або підтверджена вагітність.
Протипоказано одночасне застосування лікарського засобу Мідіана з лікарськими засобами, що містять омбітасвір/паритапревір/ритонавір, дасабувір, глекапревір/пібрентасвір та софосбувір/велпатасвір/воксилапревір (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ та ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
Побічна дія
серйозні побічні ефекти, пов’язані із застосуванням КПК, див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ.
Під час застосування препарату Мідіана повідомляли про наступні побічні реакції.
У таблиці нижче наведені побічні реакції за класами систем органів MedDRA (КСО) та частотою відповідно до рекомендацій ВООЗ (табл. 1):
Таблиця 1.
| Класи систем органів | Побічні реакції за частотою | ||
| Часто (≥1/100 та <1/10) | Нечасто (≥1/1000 та <1/100) | Поодинокі (≥1/10 000 та <1/1000) | |
| Розлади імунної системи | – | – | Гіперчутливість, БА |
| Психічні порушення | Депресія | Підвищення лібідо, зниження лібідо | _ |
| Розлади нервової системи | Головний біль | _ | _ |
| Розлади органів слуху та лабіринту | _ | _ | Гіпоакузія |
| Судинні розлади | Мігрень | АГ, артеріальна гіпотензія | ВТЕ, АТЕ |
| Розлади ШКТ | Біль у животі, нудота | Блювання, діарея | – |
| Розлади шкіри та підшкірної клітковини | Акне | Екзема, свербіж, алопеція | Вузликова еритема, мультиформна еритема |
| Розлади репродуктивної системи та молочних залоз | Менструальні розлади, метрорагія, біль у молочних залозах, болючість молочних залоз, лейкорея, вульвовагінальний кандидоз | Збільшення молочних залоз, вагініт | Виділення з молочних залоз |
| Загальні розлади та розлади в місці введення | – | Затримка рідини, збільшення маси тіла, зменшення маси тіла | – |
Опис окремих небажаних реакцій. У жінок, які приймали КПК, спостерігався підвищений ризик розвитку артеріальних або венозних тромботичних/тромбоемболічних ускладнень, у тому числі інфаркту міокарда, інсульту, транзиторних ішемічних атак, венозного тромбозу та тромбоемболії легеневої артерії. Більш детальна інформація представлена у розділі ОСОБЛИВОСТІ ЗАСТОСУВАННЯ.
Нижчезазначені серйозні побічні реакції були зареєстровані у жінок, які застосовують КПК, що також описані в розділі ОСОБЛИВОСТІ ЗАСТОСУВАННЯ:
– венозні тромбоемболічні розлади;
– артеріальні тромбоемболічні розлади;
– АГ;
– пухлини печінки;
– поява або загострення захворювань, зв’язок яких із прийомом пероральних контрацептивів не з’ясований остаточно: хвороба Крона, неспецифічний виразковий коліт, епілепсія, міома матки, порфірія, системний червоний вовчак, герпес вагітних, хорея Сиденгама, гемолітико-уремічний синдром, холестатична жовтяниця;
– хлоазма;
– гострі або хронічні порушення функції печінки, що можуть потребувати скасування застосування КПК до нормалізації показників функції печінки;
– екзогенні естрогени можуть індукувати або посилювати симптоми спадкового та набутого ангіоневротичного набряку.
Частота діагностування раку молочної залози серед жінок, які приймають КПК, дещо підвищена. Оскільки рак молочної залози у жінок віком до 40 років зустрічається зрідка, збільшення кількості випадків діагностування раку молочної залози у жінок, які застосовують нині або нещодавно застосовували КПК, є незначним щодо рівня загального ризику раку молочної залози. Взаємозв’язок із застосуванням КПК невідомий. Докладну інформацію — див. ПРОТИПОКАЗАННЯ та ОСОБЛИВОСТІ ЗАСТОСУВАННЯ.
Взаємодії. Проривні кровотечі та/або зниження контрацептивної дії може виникнути внаслідок взаємодії інших лікарських засобів (індукторів ферментів) із пероральними контрацептивами (див. ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
Особливості застосування
рішення про призначення препарату Мідіана слід приймати з урахуванням індивідуальних факторів ризику жінки, існуючих на даний момент, у тому числі факторів ризику розвитку ВТЕ, а також ризику виникнення ВТЕ, пов’язаного з прийомом препарату Мідіана, порівняно з іншими комбінованими гормональними контрацептивами (КГК) (див. ПРОТИПОКАЗАННЯ та ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
Попередження. За наявності будь-яких станів або факторів ризику, зазначених нижче, слід обговорити з жінкою доцільність застосування препарату Мідіана.
У разі загострення або при перших проявах будь-яких із вказаних станів або факторів ризику жінкам рекомендується звернутися до лікаря та визначити необхідність припинення прийому препарату Мідіана.
У разі підозрюваного або підтвердженого артеріального або венозного тромбозу слід припинити застосування КГК. Якщо розпочата антикоагулянтна терапія, слід забезпечити альтернативну адекватну контрацепцію через тератогенний вплив антикоагулянтів (кумарини).
Циркуляторні розлади
Ризик виникнення ВТЕ. На тлі застосування будь-якого КГК підвищується ризик розвитку ВТЕ порівняно з відсутністю застосування.
Застосування препаратів, що містять левоноргестрел, норгестимат або норетистерон, асоціюються з нижчим ризиком ВТЕ. Застосування інших лікарських засобів, таких як Мідіана, може призводити до підвищення ризику удвічі. Рішення про застосування препарату, який не належить до групи препаратів з найменшим ризиком розвитку ВТЕ, має бути прийняте тільки після обговорення з жінкою. Необхідно переконатися, що вона усвідомлює ризик розвитку ВТЕ, пов’язаний із застосуванням препарату Мідіана, ступінь впливу наявних у неї факторів ризику на рівень вищезазначеного ризику і той факт, що ризик ВТЕ є найвищим протягом першого року застосування препарату. За деякими даними, ризик ВТЕ може зростати при відновленні застосування КПК після перерви тривалістю ≥4 тиж.
Серед жінок, які не застосовують КПК і не є вагітними, частота виникнення ВТЕ становить приблизно 2 випадки на 10000 жінок на рік. Однак у будь-якої окремо взятої жінки рівень ризику може бути значно вищим, залежно від наявних у неї основних факторів ризику (див. нижче).
Встановлено1, що з 10000 жінок, які застосовують КГК, що містять дроспіренон, у 9–12 жінок розвинеться ВТЕ протягом 1 року. Це порівнюється з показником приблизно 62 у жінок, які застосовують КГК, що містять левоноргестрел.
В обох випадках кількість випадків ВТЕ за рік була меншою, ніж зазвичай очікується у період вагітності або у післяпологовий період.
ВТЕ може призводити до летальних наслідків у 1–2% випадків.
Кількість випадків ВТЕ на 10000 жінок за 1 рік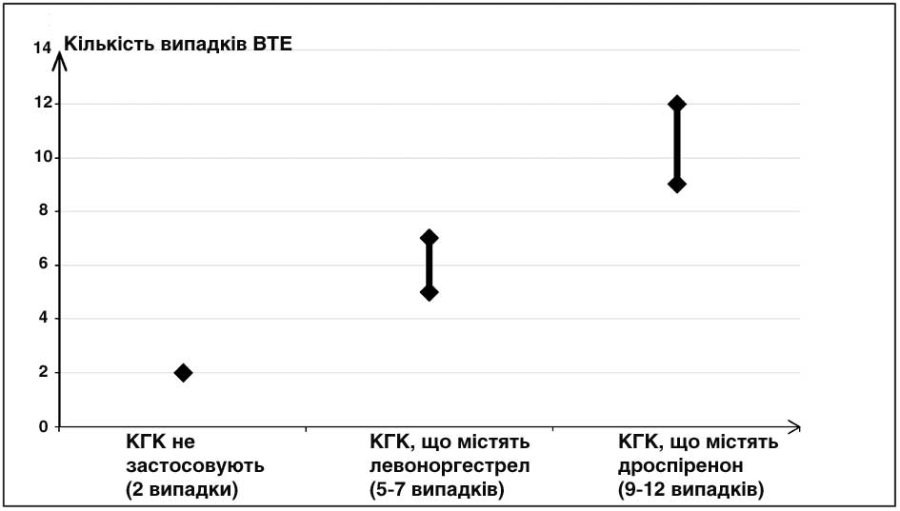
1 Ці показники отримано на основі всіх даних епідеміологічних досліджень з урахуванням відносних ризиків, пов’язаних із прийомом різних КГК, порівняно із застосуванням КГК, що містять левоноргестрел.
2 У середньому 5–7 випадків на 10000 жінко-років на основі розрахунку відносного ризику застосування КГК, що містять левоноргестрел, порівняно з таким у жінок, які не отримують КГК (приблизно 2,3–3,6 випадка).
Надзвичайно рідко повідомлялося про виникнення тромбозу в інших кровоносних судинах, наприклад артеріях і венах печінки, нирок, сітківки або мезентеріальних судинах, у жінок, які застосовували КГК.
Фактори ризику розвитку ВТЕ . На тлі застосування КГК ризик розвитку венозних тромбоемболічних ускладнень може значно збільшуватися у жінок з додатковими факторами ризику, особливо при наявності множинних факторів ризику (табл. 2).
Препарат Мідіана протипоказаний жінкам з наявністю множинних факторів ризику, на підставі яких їх можна віднести до групи високого ризику розвитку венозного тромбозу (див. ПРОТИПОКАЗАННЯ). Якщо жінка має більше одного фактора ризику, зростання ризику може бути більшим, ніж сума ризиків, асоційованих із кожним окремим фактором, тому слід брати до уваги загальний ризик розвитку ВТЕ. КГК не слід призначати, якщо співвідношення користь/ризик є несприятливим (див. ПРОТИПОКАЗАННЯ).
Таблиця 2
Фактори ризику розвитку ВТЕ
| Фактор ризику | Примітка |
| Ожиріння (індекс маси тіла >30 кг/м2) | Ризик значно підвищується при збільшенні індексу маси тіла. Особливо потребує уваги при наявності у жінок інших факторів ризику |
| Тривала іммобілізація (у тому числі повітряний переліт більше 4 год), велике оперативне втручання, будь-яка операція на ногах або на органах малого таза, нейрохірургічні втручання або обширна травма. Примітка: тимчасова іммобілізація, у тому числі повітряний переліт >4 год, також може бути фактором ризику ВТЕ, особливо для жінок з іншими факторами ризику | У таких випадках рекомендується припинити застосування препарату (у разі планового оперативного втручання щонайменше за 4 тиж) та не відновлювати застосування раніше ніж через 2 тиж після повного відновлення рухової активності. Щоб уникнути неочікуваної вагітності, слід використовувати інший метод контрацепції. Потрібно розглянути доцільність антитромботичної терапії, якщо застосування препарату Мідіана не було припинено заздалегідь |
| Сімейний анамнез (ВТЕ у рідного брата/сестри або батьків, особливо у відносно молодому віці, наприклад <50 років) | У разі наявності спадкової схильності перед застосуванням будь-яких КГК жінкам рекомендується порадитися зі спеціалістом |
| Інші стани, пов’язані з ВТЕ | Рак, системний червоний вовчак, гемолітико-уремічний синдром, хронічне запальне захворювання кишечнику (хвороба Крона або виразковий коліт) та серпоподібноклітинна анемія |
| Старший вік | Особливо >35 років |
Немає єдиної думки щодо можливого впливу варикозного розширення вен або поверхневого тромбофлебіту на розвиток та прогресування венозного тромбозу.
Необхідно звернути увагу на підвищений ризик розвитку тромбоемболії у період вагітності, особливо протягом перших 6 тиж після пологів (див. Застосування у період вагітності або годування грудьми).
Симптоми ВТЕ (тромбоз глибоких вен і тромбоемболія легеневої артерії)
У разі виникнення нижчезазначених симптомів жінці слід терміново звернутися за медичною допомогою та повідомити лікаря про те, що вона приймає КПК.
Симптоми тромбозу глибоких вен (ТГВ) можуть включати:
– однобічний набряк ноги та/або стопи або ділянки уздовж вени на нозі;
– біль або підвищену чутливість у нозі, що може відчуватися тільки при стоянні або ходьбі;
– відчуття жару в ураженій нозі;
– почервоніння або зміну кольору шкіри на нозі.
Симптоми тромбоемболії легеневої артерії (ТЕЛА) можуть включати:
– раптову задишку нез’ясованої етіології або прискорене дихання;
– раптовий початок кашлю, який може супроводжуватися кровохарканням;
– раптовий біль у грудній клітці;
– переднепритомний стан або запаморочення;
– швидке або нерегулярне серцебиття.
Деякі із цих симптомів (наприклад задишка, кашель) є неспецифічними і можуть бути неправильно оцінені як більш поширені або менш тяжкі явища (наприклад інфекції дихальних шляхів).
Інші ознаки оклюзії судин можуть включати раптовий біль, набряк та незначне посиніння кінцівки.
При оклюзії судин ока початковою симптоматикою може бути нечіткість зору, що не супроводжується больовими відчуттями і яка може прогресувати до втрати зору. Іноді втрата зору розвивається майже миттєво.
Ризик розвитку ATE. Епідеміологічні дослідження виявили, що застосування будь-яких КГК асоціюється з підвищеним ризиком АТЕ (інфаркт міокарда) або цереброваскулярних подій (наприклад транзиторна ішемічна атака, інсульт). Артеріальні тромбоемболічні явища можуть призводити до летального наслідку.
Фактори ризику розвитку АТЕ. При застосуванні КГК ризик розвитку артеріальних тромбоемболічних ускладнень або цереброваскулярних подій зростає у жінок із факторами ризику (табл. 3). Препарат Мідіана протипоказаний, якщо у жінки є один серйозний або множинні фактори ризику розвитку ATE, які можуть підвищити ризик розвитку артеріального тромбозу (див. ПРОТИПОКАЗАННЯ). Якщо жінка має більше одного фактора ризику, зростання ризику може бути більшим, ніж сума ризиків, асоційованих із кожним окремим фактором, тому слід брати до уваги загальний ризик розвитку АТЕ. КГК не слід призначати, якщо співвідношення користь/ризик є несприятливим (див. ПРОТИПОКАЗАННЯ).
Таблиця 3
Фактори ризику розвитку АТЕ
| Фактор ризику | Примітка |
| Старший вік | Особливо ≥35 років |
| Паління | Жінкам, які бажають застосовувати КГК, слід рекомендувати відмовитися від паління. Жінкам віком від 35 років, які продовжують палити, слід наполегливо рекомендувати інший метод контрацепції |
| АГ | |
| Ожиріння (індекс маси тіла >30 кг/м2) | Ризик значно підвищується при збільшенні індексу маси тіла. Особливо потребує уваги при наявності у жінок інших факторів ризику |
| Сімейний анамнез (АТЕ у рідного брата/сестри або батьків, особливо у відносно молодому віці, наприклад до 50 років) | У разі наявності спадкової схильності перед застосуванням будь-яких КГК жінкам рекомендується порадитися зі спеціалістом |
| Мігрень | Зростання частоти виникнення або тяжкості мігрені під час застосування КГК (може бути продромальним станом перед розвитком цереброваскулярних подій) може стати причиною негайного припинення прийому КГК |
| Інші стани, пов’язані з небажаними реакціями з боку судин | Цукровий діабет, гіпергомоцистеїнемія, вади клапанів серця, фібриляція передсердь, дисліпопротеїнемія та системний червоний вовчак |
Симптоми ATE . У разі виникнення нижчезазначених симптомів жінці слід терміново звернутися за медичною допомогою та повідомити лікаря, що вона приймає КГК.
Симптомами цереброваскулярного розладу можуть бути:
– раптове оніміння або слабкість обличчя, рук або ніг, особливо однобічне;
– раптове порушення ходи, запаморочення, втрата рівноваги або координації;
– раптова сплутаність свідомості, порушення мовлення або розуміння;
– раптове погіршення зору на одне або обидва ока;
– раптовий сильний або тривалий головний біль без визначеної причини;
– втрата свідомості або непритомність із судомами або без них.
Тимчасовість симптомів може свідчити про транзиторну ішемічну атаку (ТІА).
Симптомами інфаркту міокарда (ІМ) можуть бути:
– біль, дискомфорт, тиск, тяжкість, відчуття стискування або розпирання у грудях, руці або за грудиною;
– дискомфорт з іррадіацією у спину, щелепу, горло, руку, шлунок;
– відчуття переповненості шлунка, порушення травлення або ядуха;
– посилене потовиділення, нудота, блювання або запаморочення;
– надзвичайна слабкість, неспокій або задишка;
– швидке або нерегулярне серцебиття.
Пухлини. Результати деяких епідеміологічних досліджень вказують на додаткове підвищення ризику розвитку раку шийки матки при тривалому застосуванні КПК (>5 років), проте це твердження залишається суперечливим, оскільки остаточно не з’ясовано, наскільки результати досліджень враховують супутні фактори ризику, наприклад статеву поведінку та інші фактори, наприклад інфікування вірусом папіломи людини (ВПЛ).
Метааналіз даних 54 епідеміологічних досліджень вказує на незначне підвищення відносного ризику (1,24) розвитку раку молочної залози у жінок, які застосовують КПК. Цей підвищений ризик поступово зникає протягом 10 років після закінчення застосування КПК. Оскільки рак молочної залози у жінок віком до 40 років зустрічається рідко, збільшення кількості випадків діагностування раку молочної залози у жінок, які застосовують нині або нещодавно застосовували КПК, є незначним щодо рівня загального ризику виникнення раку молочної залози. Результати цих досліджень не надають доказів існування причинного взаємозв’язку. Підвищення ризику може бути зумовлене як більш ранньою діагностикою раку молочної залози у жінок, які застосовують КПК, так і біологічною дією КПК або поєднанням обох факторів. Відзначено тенденцію, що рак молочної залози, виявлений у жінок, які коли-небудь приймали КПК, клінічно менш виражений, ніж у тих, хто ніколи не приймав КПК.
У поодиноких випадках у жінок, які застосовували КПК, спостерігалися доброякісні, а ще рідше — злоякісні пухлини печінки. В окремих випадках ці пухлини спричиняли небезпечну для життя внутрішньочеревну кровотечу. У разі виникнення скарг на сильний біль в епігастральній ділянці, збільшення печінки або наявність ознак внутрішньочеревної кровотечі при диференціальній діагностиці слід враховувати можливість наявності пухлини печінки у жінок, які приймають КПК.
Застосування КПК у високих дозах (50 мкг етинілестрадіолу) знижує ризик раку ендометрія та яєчника. Залишається підтвердити, чи ці дані можуть стосуватися і низькодозових КПК.
Злоякісні пухлини можуть бути небезпечними для життя або призводити до летального наслідку.
Інші стани. Депресивний настрій і депресія є частими побічними реакціями при застосуванні гормональних контрацептивів (див. ПОБІЧНА ДІЯ). Депресія може бути тяжкою і є відомим фактором ризику суїцидальної поведінки та самогубства. Жінок слід інформувати про необхідність звернутися до лікаря у разі перепадів настрою і симптомів депресії, навіть якщо вони виникають невдовзі після початку лікування.
Прогестогенний компонент препарату Мідіана є антагоністом альдостерону із калійзберігаючими властивостями. У більшості випадків застосування не очікується підвищення рівня калію в сироватці крові. Однак, у клінічному дослідженні у деяких пацієнтів із легкими та помірними порушеннями функції нирок і супутнім застосуванням калійзберігаючих лікарських засобів рівень калію в сироватці крові дещо, але не суттєво, підвищувався під час застосування дроспіренону. Тому рекомендується контролювати рівень калію в сироватці крові у першому циклі прийому препарату у пацієнтів з нирковою недостатністю та перед початком застосування препарату утримувати рівень калію сироватки крові не вище верхньої межі норми, особливо при одночасному застосуванні калійзберігаючих лікарських засобів (див. ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
Жінки з гіпертригліцеридемією або сімейним анамнезом щодо цього порушення належать до групи ризику розвитку панкреатиту при застосуванні КПК.
Хоча незначне підвищення АТ описане у багатьох жінок, які приймали КПК, клінічно значуще підвищення АТ є поодиноким явищем. Лише в цих рідкісних випадках необхідне негайне припинення прийому КПК.
У разі існуючої до початку лікування АГ або неможливості належним чином контролювати показники АТ за допомогою антигіпертензивних засобів, жінкам, які приймають КПК, слід припинити їх застосування. Якщо це доцільно, застосування КПК можна відновити після досягнення нормотонії за допомогою антигіпертензивної терапії.
Повідомлялося про виникнення або загострення зазначених нижче захворювань у період вагітності та при застосуванні КПК, але їх взаємозв’язок із застосуванням КПК не є остаточно з’ясованим: жовтяниця та/або свербіж, пов’язаний із холестазом; утворення жовчних каменів; порфірія; системний червоний вовчак; гемолітико-уремічний синдром; хорея Сиденгама; герпес вагітних; втрата слуху, пов’язана з отосклерозом.
Екзогенні естрогени можуть індукувати або посилювати симптоми спадкового та набутого ангіоневротичного набряку.
Гострі або хронічні розлади функції печінки можуть потребувати припинення застосування КПК, поки показники функції печінки не повернуться в межі норми.
При рецидиві холестатичної жовтяниці та/або свербежу, який спричинений холестазом, що раніше виникали у період вагітності або попереднього застосування статевих гормонів, прийом КПК слід припинити.
Хоча КГК можуть впливати на периферичну інсулінорезистентність і толерантність до глюкози, немає даних щодо потреби змінювати терапевтичний режим у жінок із цукровим діабетом, які приймають низькодозовані КПК (що містять <0,05 мг етинілестрадіолу). Проте жінки із цукровим діабетом повинні ретельно обстежуватися протягом застосування КПК, особливо на початку лікування.
Випадки загострення ендогенної депресії, епілепсії, хвороби Крона та виразкового коліту також спостерігалися під час застосування КПК.
Іноді може виникати хлоазма, особливо у жінок із хлоазмою вагітних в анамнезі. Жінки, схильні до виникнення хлоазми, мають уникати дії прямих сонячних променів або ультрафіолетового опромінювання під час прийому КПК.
Допоміжні речовини. Цей лікарський засіб містить 48,17 мг лактози моногідрату в одній таблетці.
За наявності рідкісних спадкових станів непереносимості галактози, повної лактазної недостатності або мальабсорбції глюкози-галактози не слід застосовувати цей лікарський засіб.
1 таблетка цього лікарського засобу містить 0,07 мг соєвого лецитину. Даний препарат не слід приймати пацієнткам із гіперчутливістю до арахісу або сої.
Медичне обстеження/консультація. Перед початком або відновленням прийому препарату Мідіана рекомендується зібрати повний медичний анамнез (включаючи сімейний анамнез), пройти медичне обстеження і виключити вагітність. Слід виміряти АТ, провести об’єктивне дослідження, беручи до уваги протипоказання (див. ПРОТИПОКАЗАННЯ), та особливі вказівки і запобіжні заходи (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ). Важливо звернути увагу жінок на ризик виникнення венозного і артеріального тромбозу, включаючи ризик застосування препарату Мідіана, порівняно з іншими КПК, щодо симптомів ВТЕ і АТЕ, а також на відомі фактори ризику та дії у разі підозри на тромбоз.
Необхідно, щоб пацієнтка уважно прочитала інструкцію для медичного застосування та дотримувалася зазначених у ній рекомендацій. Частота і характер оглядів повинні ґрунтуватися на існуючих нормах медичної практики з урахуванням індивідуальних особливостей кожної жінки.
Слід попередити, що пероральні контрацептиви не захищають від ВІЛ-інфекції (СНІД) та інших захворювань, що передаються статевим шляхом.
Зниження ефективності. Ефективність КПК може знижуватися у випадку пропуску прийому таблетки (див. ЗАСТОСУВАННЯ), розладів ШКТ (див. ЗАСТОСУВАННЯ) або одночасного прийому інших лікарських засобів (див. ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
Контроль циклу. При застосуванні КПК можуть спостерігатися нерегулярні кровотечі (кровомазання або проривні кровотечі), особливо протягом перших місяців застосування препарату. Тому оцінка нерегулярних кровотеч може мати значення лише після 3 циклів адаптації.
Якщо нерегулярні кровотечі продовжуються або трапляються після декількох нормальних циклів, необхідно розглянути питання про негормональні причини і провести відповідні діагностичні заходи (при необхідності — кюретаж) для виключення злоякісних новоутворень або вагітності.
У деяких жінок може не настати кровотеча відміни під час перерви у прийомі препарату. Якщо прийом КПК відбувався згідно з вказівками, описаними у розділі ЗАСТОСУВАННЯ, вагітність малоймовірна. Проте, якщо прийом КПК відбувався нерегулярно до відсутності першої кровотечі відміни або якщо кровотечі відміни відсутні протягом 2 циклів, перед продовженням застосування КПК необхідно виключити вагітність.
Підвищення рівня АлАТ. Під час клінічних досліджень за участю пацієнтів, які проходили курс лікування вірусного гепатиту С (ВГС), за допомогою лікарських засобів, що містять омбітасвір/паритапревір/ритонавір та дасабувір, з рибавірином або без нього, було зафіксовано значне підвищення рівня АлАТ, що перевищувало верхню межу норми у 5 разів. Це відбувалося зі значно більшою частотою у жінок, які застосовували лікарські засоби, що містять етинілестрадіол, такі як КГК. Підвищення рівня АлАТ спостерігалося також при застосуванні противірусних лікарських засобів, що містять глекапревір/пібрентасвір та софосбувір/велпатасвір/воксилапревір (див. ПРОТИПОКАЗАННЯ та ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
Застосування у період вагітності або годування грудьми.
Вагітність. Препарат Мідіана протипоказаний до застосування у період вагітності.
У разі настання вагітності під час застосування препарату Мідіана, його прийом необхідно припинити негайно. Однак результати епідеміологічних досліджень не вказують на підвищення ризику появи вроджених вад у дітей, народжених жінками, які приймали КПК до вагітності, так само, як і на існування тератогенної дії при ненавмисному прийомі КПК у період вагітності.
У дослідженнях на тваринах були виявлені побічні ефекти у період вагітності та лактації (див. ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ). Ґрунтуючись на цих даних, не можна виключити побічних ефектів, пов’язаних із гормональним впливом поєднаних діючих речовин. Однак загальний досвід застосування КПК у період вагітності не свідчить про існування небажаного впливу у людини.
Відомі дані щодо застосування препарату Мідіана у період вагітності занадто обмежені для того, щоб можна було зробити висновки щодо негативного впливу препарату Мідіана на перебіг вагітності, здоров’я плода або новонародженого. Дотепер немає жодних відповідних епідеміологічних даних.
При відновленні застосування препарату Мідіана слід враховувати підвищення ризику розвитку ВТЕ у післяпологовому періоді (див. ЗАСТОСУВАННЯ, ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
Період годування грудьми. КПК можуть впливати на годування грудьми, оскільки під їх впливом може зменшуватись кількість грудного молока, а також змінюватися його склад. Зважаючи на це, КПК не рекомендується приймати в період годування грудьми. Невеликі кількості контрацептивних стероїдів та/або їх метаболіти можуть проникати у грудне молоко під час застосування КПК. Ці кількості можуть вплинути на дитину.
Здатність впливати на швидкість реакції при керуванні транспортними засобами або роботі з іншими механізмами. Не проводили досліджень щодо впливу лікарського засобу на здатність керувати транспортними засобами або працювати з іншими механізмами. У жінок, які приймають комбіновані пероральні контрацептиви, не повідомлялося про вплив на здатність керувати транспортними засобами або працювати з іншими механізмами.
Взаємодія з іншими лікарськими засобами
слід ознайомитися з інформацією щодо лікарського засобу, що застосовується одночасно, для виявлення потенційних взаємодій.
Фармакодинамічні взаємодії. Одночасне застосування з лікарськими засобами, що містять омбітасвір/паритапревір/ритонавір та дасабувір, з рибавірином або без нього, глекапревір/пібрентасвір і софосбувір/велпатасвір/воксилапревір, може збільшити ризик підвищення рівня АлАТ (див. ПРОТИПОКАЗАННЯ та ОСОБЛИВОСТІ ЗАСТОСУВАННЯ). Тому, перш ніж розпочати застосування цих лікарських засобів, пацієнти, які застосовують лікарський засіб Мідіана, повинні перейти на альтернативний метод контрацепції (наприклад, контрацепція за допомогою препаратів, що містять тільки прогестаген або використовувати негормональні методи). Застосування лікарського засобу Мідіана можна відновити через 2 тиж після завершення лікування за допомогою цих лікарських засобів.
Фармакокінетичні взаємодії
Вплив інших лікарських засобів на препарат Мідіана
Взаємодії можливі з лікарськими засобами, що індукують мікросомальні ферменти. Це може призвести до збільшення кліренсу статевих гормонів, що, зі свого боку, може спричинити проривну кровотечу та/або втрату ефективності контрацептиву.
Терапія. Індукція ензимів може бути виявлена вже через декілька днів лікування. Максимальна індукція ферментів загалом спостерігається через декілька тижнів. Після відміни лікування індукція ферментів може тривати приблизно 4 тиж.
Короткострокове лікування. Жінки, які приймають лікарські засоби, що індукують ферменти, мають тимчасово використовувати бар’єрний метод або інший метод контрацепції додатково до КПК. Бар’єрний метод слід використовувати протягом усього терміну лікування відповідним препаратом і ще протягом 28 днів після припинення його застосування.
Якщо терапія розпочинається у період застосування останніх таблеток КПК з упаковки, то прийом таблеток з наступної упаковки КПК слід розпочати одразу після попередньої без звичного інтервалу без застосування таблеток.
Довгострокове лікування. Жінкам при довгостроковій терапії діючими речовинами, що індукують ферменти печінки, рекомендується бар’єрний або інший відповідний негормональний метод контрацепції.
Нижчезазначені взаємодії були зафіксовані згідно з опублікованими даними.
Діючі речовини, що збільшують кліренс КПК (зниження ефективності КПК через індукцію ферментів), наприклад барбітурати, бозентан, карбамазепін, фенітоїн, примідон, рифампіцин; препарати, що застосовуються при ВІЛ-інфекції: ритонавір, невірапін та ефавіренц; також, можливо, фелбамат, гризеофульвін, окскарбазепін, топірамат і препарати, до складу яких входить рослинний лікарський засіб звіробій (Hypericum perforatum).
Діючі речовини з непостійним впливом на кліренс КПК. При одночасному застосуванні з КПК велика кількість комбінацій інгібіторів ВІЛ-протеази та ненуклеозидних інгібіторів зворотної транскриптази, включаючи комбінації з інгібіторами вірусу гепатиту С (ВГС), можуть підвищувати або знижувати концентрацію естрогену або прогестинів у плазмі крові. Сукупний вплив таких змін може бути клінічно значущим у деяких випадках.
Тому для виявлення потенційних взаємодій та будь-яких інших рекомендацій слід ознайомитися з інформацією щодо медичного застосування лікарського засобу для лікування ВІЛ/вірусу гепатиту С, що приймається одночасно. При наявності будь-яких сумнівів жінкам додатково слід використовувати бар’єрний метод контрацепції при терапії інгібіторами протеази або інгібіторами ненуклеозидної зворотної транскриптази.
Діючі речовини, що знижують кліренс КПК (інгібітори ферментів). Клінічна значущість потенційної взаємодії з інгібіторами ферментів залишається невідомою.
Одночасне застосування сильних інгібіторів CYP 3A4 може підвищити концентрації в плазмі крові естрогену або прогестину, або обох компонентів.
У дослідженні багаторазових доз комбінації дроспіренон (3 мг/добу)/етинілестрадіол (0,02 мг/добу) та сильного інгібітора CYP 3A4 кетоконазолу, що застосовувався одночасно, протягом 10 днів збільшувалося значення AUC0–24 дроспіренону та етинілестрадіолу у 2,7 та 1,4 раза відповідно.
Еторикоксиб у дозах від 60 до 120 мг/добу продемонстрував підвищення концентрацій етинілестрадіолу в плазмі крові у 1,4–1,6 раза відповідно при одночасному застосуванні з КПК, що містить 0,035 мг етинілестрадіолу.
Вплив препарату Мідіана на інші лікарські засоби. КПК можуть впливати на метаболізм інших препаратів. З огляду на це можуть змінюватися концентрації діючих речовин у плазмі крові та тканинах — як підвищуватися (наприклад циклоспорин), так і знижуватися (наприклад ламотриджин).
На підставі досліджень взаємодії in vivo у жінок-добровольців, які застосовували омепразол, симвастатин або мідазолам як субстрати-маркери, встановлено, що клінічно значуща взаємодія дроспіренону в дозі 3 мг з іншими діючими речовинами, що індукуються цитохромом Р450, є малоймовірною.
Клінічні дані свідчать про те, що етинілестрадіол пригнічує кліренс субстратів CYP 1A2, що, зі свого боку, спричиняє слабке (наприклад теофілін) або помірне (наприклад тизанідин) підвищення їх концентрацій у плазмі крові.
Інші форми взаємодії. У пацієнтів із нормальною функцією нирок одночасне застосування дроспіренону та інгібіторів АПФ або НПЗП не показало значущого впливу на рівень калію в сироватці крові. Однак одночасне застосування Мідіани та антагоністів альдостерону або калійзберігаючих діуретиків не досліджувалося. У цьому випадку необхідне дослідження рівня калію в сироватці крові протягом першого циклу прийому препарату (див. також ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
Лабораторні дослідження. Застосування контрацептивних стероїдів може впливати на результати деяких лабораторних аналізів, таких як біохімічні показники функції печінки, щитовидної залози, надниркових залоз і нирок, а також рівень транспортних білків плазми крові, таких як КЗГ і фракції ліпідів/ліпопротеїнів, показники вуглеводного обміну, коагуляції та фібринолізу. Зміни зазвичай перебувають у межах нормальних значень.
Дроспіренон збільшує активність реніну та альдостерону в плазмі крові, що викликано його легкою антимінералокортикоїдною активністю.
Передозування
дотепер немає жодних даних про комбіноване передозування дроспіренону та етинілестрадіолу.
На підставі загальних даних про застосування КПК виділяють симптоми, які можуть спостерігатися у такому випадку: нудота, блювання та кровотеча відміни. Кровотеча відміни може виникнути навіть у дівчат перед настанням першої менструації, якщо вони випадково прийняли лікарський засіб. Ніяких антидотів не існує, подальше лікування повинно бути симптоматичним.
Умови зберігання
при температурі не вище 25 °С в оригінальній упаковці для захисту від впливу світла. Препарат зберігати в недоступному для дітей місці.

