Визначення. Подагра — хронічне захворювання, зумовлене порушенням пуринового обміну і накопиченням сечової кислоти в організмі, що клінічно проявляється рецидивами гострого артриту, синовіту та відкладенням уратів у тканинах. У західних країнах подагру відзначають у 1% чоловіків.
Етіологія. При подагрі визначається порушення пуринового обміну і розвивається гіперурикемія. Причинами накопичення сечової кислоти та уратів є недостатнє виведення їх нирками (нирковий чи ретенційний тип) та надмірне утворення уратів (метаболічний чи продуктивний тип).
Підвищене утворення сечової кислоти відбувається в результаті надмірного надходження її з їжею, збільшеного синтезу пуринів, посиленого катаболізму нуклеотидів. Велике значення має генетичне порушення ферментних реакцій пуринового обміну, що спричинияє їх появу, а також екзогенні фактори: переїдання; надмірне вживання білків, жирів, алкоголю; переохолодження.
Патогенез. У розвитку подагри мають значення 3 патогенетичні фактори:
- гіперурикемія та накопичення уратів в організмі;
- відкладання уратів у тканинах;
- гостре подагричне запалення.
При гострому подагричному запаленні відбувається відкладання в порожнині суглоба уратових мікрокристалів, які активують фактор Хагемана, компоненти комплементу, кініни, що зумовлює підвищення судинної проникності, хемотаксис нейтрофілів. При цьому фагоцитоз кристалів спричиняє вивільнення лізосомальних ферментів, у результаті чого розвивається запалення. Відкладання мікрокристалів в інтерстиції нирок призводить до розвитку подагричної нефропатії.
Гіперурикемія спричиняє підвищенню АТ, активації РААС.
Предиктори розвитку подагри:
- гіперурикемія, АГ, дисліпідемії, атеросклероз, ІХС;
- застосування тіазидних і петльових діуретиків, ожиріння, часте вживання спиртних напоїв;
- підвищена експресія уратів;
- нефропатія;
- інсулінорезистентність (підвищує реабсорбцію уратів у нирках).
Фактори, що провокують загострення подагри:
- алкоголь, переохолодження;
- мікротравма (тривала ходьба, тривале перебування за кермом);
- операція, медикаментозні засоби (вітамін В12, інсулін, діуретики, пеніцилін тощо);
- раптова зміна концентрації уратів у крові (у результаті гіповолемії при значному потовиділенні);
- зміна харчування (споживання м’яса, жирів тощо).
Класифікація подагри [6]
За етіопатогенетичними ознаками:
- первинна (ідіопатична) подагра;
- вторинна подагра, зумовлена іншими захворюваннями чи застосуванням медикаментів.
За механізмом накопичення сечової кислоти:
- метаболічний тип;
- гіпоекскреторний (нирковий) тип;
- змішаний тип.
За клінічним перебігом (ACR):
- безсимптомна гіперурикемія;
- гострий подагричний артрит;
- подагра з розвитком тофусів;
- сечокам’яний уролітіаз, асоційований з подагрою, патологія нирок.
Періоди перебігу суглобового синдрому:
1. Преморбідний — є лише гіперурикемія, її перебіг безсимптомний.
2. Інтермітуючий — чергування гострих нападів подагричного артриту з тривалими періодами ремісії.
3. Хронічна подагра — характерні тофуси, хронічний подагричний артрит, з позасуглобових проявів — ураження нирок (у 50–75% хворих).
Стадії подагри:
1) легка — напади артриту 1–2 рази на рік, охоплює не більше 2 суглобів, на рентгенограмах немає ознак суглобової деструкції, уражень нирок, тофуси відсутні чи поодинокі й дрібні;
2) середньотяжка — частота нападів артриту 3–4 рази на рік при ураженні 2–4 суглобів, суглобова деструкція виражена помірно, множинні тофуси та нефролітіаз;
3) тяжка — частота нападів 5 на рік і більше, множинне ураження суглобів, різко виражена суглобово-кісткова деструкція, множинні великі тофуси, наявність вираженої нефропатії та ХНН.
Клінічна класифікація подагри (Асоціація ревматологів України, 2013; EULAR, 2016)
1. Клінічні стадії:
а) гострий подагричний артрит;
б) міжприступна (інтервальна) подагра;
в) хронічний подагричний артрит: загострення, ремісія;
г) хронічний тофусний артрит.
2. Рентгенологічні стадії:
І — великі кісти (тофуси, симптом «пробійника») в субхондральній кістці і більш глибоких шарах, звуження суглобової щілини, іноді ущільнення м’яких тканин;
II — великі кісти поблизу суглобової поверхні з незначним (<1/3 суглобової поверхні) ерозуванням суглобового хряща, ущільнення навколосуглобових м’яких тканин, іноді з кальцифікатами;
ІІІ — великі ерозії не менше ніж 1/3 суглобової поверхні, остеоліз епіфізу, значне ущільнення м’яких тканин з вапнуванням.
3. Ступінь функціональної недостатності суглобів:
І — професійна здатність збережена;
ІІ — професійна здатність втрачена;
ІІІ — втрачена здатність до самообслуговування.
4. Типи нефропатії:
а) уролітіаз; б) інтерстиційний нефрит; в) гломерулонефрит; г) артеріолосклероз.
Патогенетично прийнято виділяти метаболічну, ниркову та змішану форми подагри. При метаболічній формі основним механізмом гіперурикемії є збільшення синтезу сечової кислоти. В основі ниркової форми подагри лежить зниження видалення уратів нирками. При змішаній формі має місце помірно збільшений синтез сечової кислоти і знижена її екскреція нирками [5, 14].
Приклади формулювання діагнозу:
1. Первинна подагра, змішаний тип, тяжкий перебіг, хронічний подагричний артрит, ХХН ІІ ст., подагрична нефропатія, функціональна недостатність суглобів ІІ ст.
2. Вторинна подагра, метаболічний тип, середньотяжкий перебіг, гострий подагричний артрит, функціональна недостатність суглобів І ст.
Критерії діагностики різних варіантів подагри наведені в алгоритмі 6.9.
| Алгоритм 6.9. Критеріїв діагностики різних клінічних варіантів подагри [11, 19]
Клінічні критерії: 1. Типовий (класичний) гострий напад розвивається через декілька років від початку безсимптомної гіперурикемії, частіше виникає вночі після вживання жирної їжі, алкоголю, травм, переохолодження, фізичного перевантаження, носіння тісного взуття, застосування гіпоурикемічних ліків. Виникає різкий біль в І плеснофаланговому суглобі та стопі; шкіра червона, поступово стає бузково-багряною, гарячою на дотик, блищить (потім лущиться). Напад триває 3–10 днів. 2. Підгостра форма перебігає у вигляді моноартриту з типовою локалізацією, супроводжується незначним болем і помірною ексудацією. 3. «Мігруюча» форма характеризується виникненням гострих нападів подагричного артриту в нетипових суглобах. 4. Ревматоїдноподібна форма характеризується ураженням дрібних суглобів кистей, променезап’ясткових суглобів. 5. Псевдофлегмонозна форма супроводжується розвитком моноартриту будь-якої локалізації з різко вираженими запальними явищами і значним лейкоцитозом; клінічна картина нагадує флегмону. 6. Абортивна форма більш притаманна жінкам; напад гострого артриту починається і регресує впродовж 2–3 год. 7. Малосимптомна форма характеризується незначним болем, іноді зі змінами шкіри над суглобом; підтверджується підвищенням рівня сечової кислоти в крові. 8. Тофус — макроскопічний конгломерат кристалів моноурату натрію, який формується через декілька років після дебюту подагри. Тофуси часто локалізуються підшкірно, внутрішньосуглобово, в ділянці сухожилля, у суглобових сумках м’яких тканин у нирках; тривають до утворення уратового нефрону, а в кісткових структурах виникає симптом «пробійника». Лабораторні критерії:
Рентгенологічні критерії: І стадія — великі кісти (тофуси, симптом «пробійника») в субхондральній кістці і глибших шарах, звуження суглобової щілини, іноді ущільнення м’яких тканин; ІІ стадія — великі кісти поблизу суглобової поверхні з незначним (менше 1/3 суглобової поверхні) ерозуванням суглобового хряща, ущільненням навколосуглобових м’яких тканин, іноді з кальцифікатами; ІІІ стадія — великі ерозії не менше ніж 1/3 суглобової поверхні, остеоліз епіфізу, значне ущільнення м’яких тканин з вапнуванням. |
Результати досліджень свідчать про те, що гіперурикемія — сильний незалежний модифікований предиктор серцево-судинної смертності з високим і дуже високим серцево-судинним ризиком (АГ, ІХС, ХСН, метаболічний синдром, ЦД).
Для діагностики подагри застосовуються критерії EULAR, 2016 (табл. 6.39).
Таблиця 6.39. Критерії встановлення діагнозу подагри (EULAR, 2016)
| Критерії | Кількість балів |
| Чоловіча стать | 2 бали |
| Одна і більше гострих атак артриту в анамнезі | 2 бали |
| Максимальне запалення суглоба уже в першу добу | 0,5 бала |
| Почервоніння шкіри над суглобом | 1 бал |
| Ураження І плеснофалангового суглоба | 2,5 бала |
| АГ | 1,5 бала |
| Гіперурикемія | 3,5 бала |
| За підозри на подагру показник повинен бути не менше 2 балів. Діагноз подагри верифікований при сумі 8 балів | |
Примітка. Діагноз подагри вважається визначеним при сумі 8 балів, вірогідним — 5–7 балів, подагра заперечується — 4 бали.
Для діагностики подагри широко застосовують Римські та Американські критерії.
Римські критерії діагностики подагри:
1. Вміст сечової кислоти в крові перевищує 0,36 ммоль/л.
2. Наявність тофусів (рис. 6.9).
3. Наявність кристалів сечокислого натрію в синовіальній рідині чи відкладення солей сечової кислоти в тканинах, що визначаються при хімічному та мікроскопічному дослідженні.
4. Чіткі анамнестичні дані про пошкодження суглобів (напад болю та припухлість) через 1–2 тиж.
5. Діагноз вважається доведеним, якщо визначаються два будь-які позитивні критерії.
Слід зауважити, що наведені дані не враховують той факт, що в 40% випадків камені в нирках утворюються ще до першого нападу подагричного артриту на фоні нормальної кількості сечової кислоти в крові.
Критерії діагностики подагри ACR:
I. Наявність характерних кристалічних уратів у суглобовій рідині.
II. Наявність доведених тофусів, які вміщують кристалічні урати, підтверджуються хімічною чи поляризаційною мікроскопією.
III. Наявність 6 із 12 ознак:
- більш ніж одна гостра атака артриту в анамнезі;
- максимум запалення суглоба в першу добу;
- моноартикулярний характер артриту;
- гіперемія шкіри над ураженим суглобом;
- припухлість або біль в І плеснофаланговому суглобі;
- одностороннє ураження суглоба стопи;
- вузликові утворення, які нагадують тофуси;
- гіперурикемія;
- одностороннє ураження І плеснофалангового суглоба;
- асиметрична припухлість ураженого суглоба;
- виявлені на рентгенограмах субкортальні кісти без ерозій;
- відсутність флори в суглобовій рідині.
Існує бальна діагностика подагричного артриту, яка наведена в табл. 6.40.
Таблиця 6.40. Діагностичні критерії подагричного артриту
| Критерії | Бали | |
| Наявність в анамнезі або спостереження 2 атак та набряків і/або почервоніння та сильного болю в суглобі кінцівок з ремісією через 1–2 тиж | 2 | |
| Гострий артрит плеснофалангового суглоба великого пальця стопи в анамнезі або в статусі | 4 | |
| Тофуси | 4 | |
| Підвищення рівня сечової кислоти в сироватці крові ( >0,36 ммоль/л (6 мг%)) | 1 | |
| Симптом «пробійника» або великі кісти на рентгенограмі | 2 | |
| Діагноз | Діагностична гранична сума балів | |
| Подагра достовірна | ≥8 | |
| Подагра імовірна | 5–7 | |
| Подагра відсутня | ≤4 | |
Локалізацію тофусів при подагрі характеризує рис. 6.9.
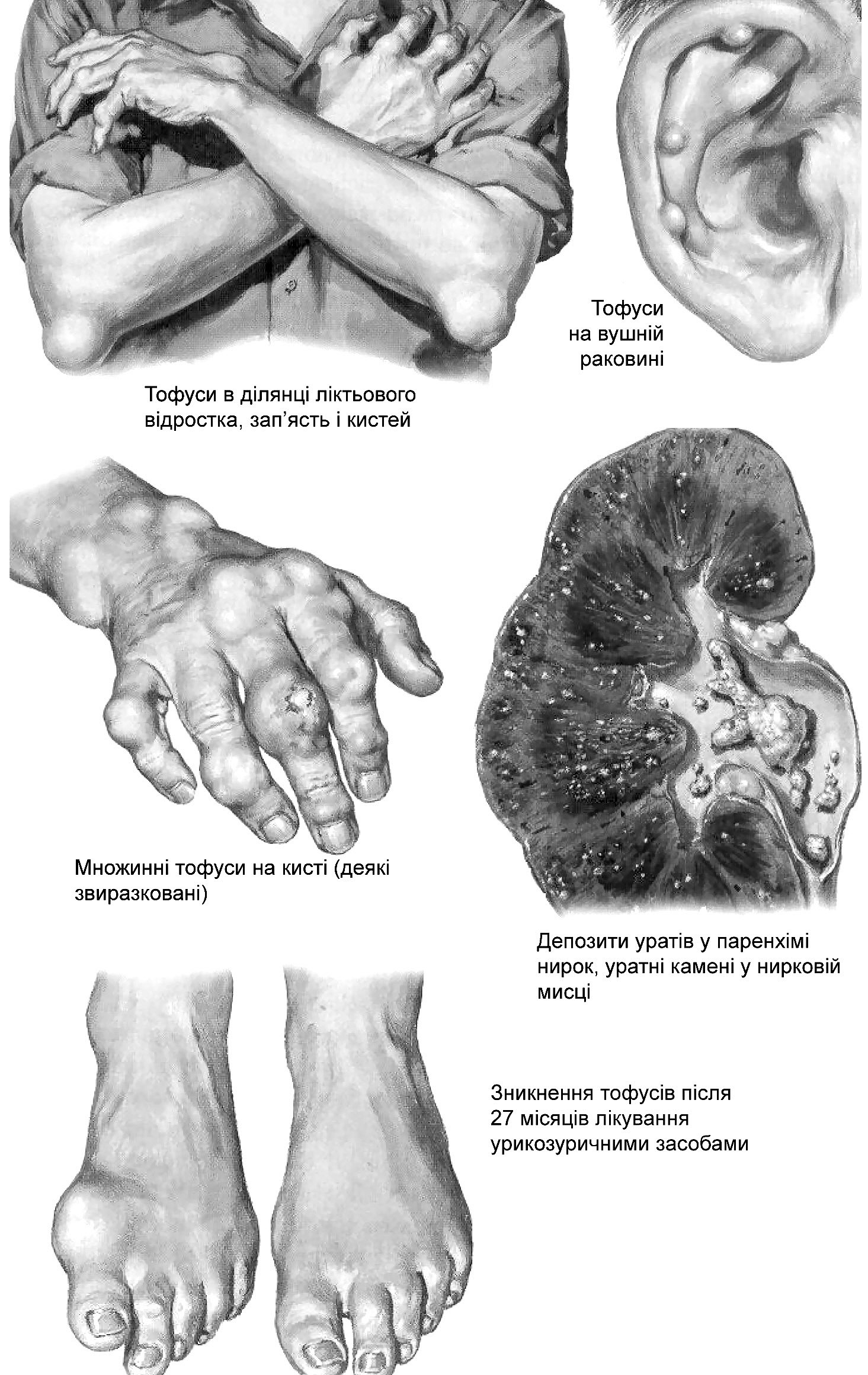
Рис. 6.9. Локалізація тофусів при подагрі (за Ф. Неттером)
Характер болю при подагричному артриті ілюструє рис. 19. (див. кольорову вкл.).
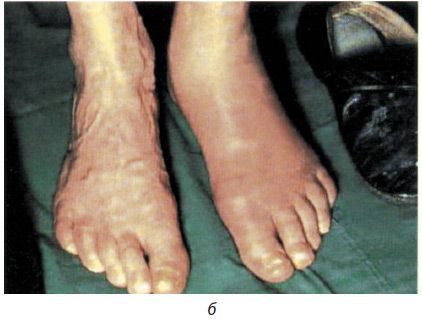
Природний перебіг подагри у різному віці наведений на рис. 6.10.

Рис. 6.10. Природний перебіг подагри (за Ф. Неттером)
У 2016 р. EULAR представила оновлені рекомендації щодо лікування подагри.
Основні принципи лікування подагри:
1. Кожному хворому на подагру слід надати вичерпну інформацію про патофізіологію захворювання та ефективні способи лікування, принципи терапії гострих подагричних атак і елімінації уратних кристалів за допомогою контролю сироваткової концентрації сечової кислоти (КСК) нижче цільових значень.
2. Кожному хворому на подагру слід дати рекомендації щодо зміни способу життя: зменшення маси тіла (за необхідності), відмови від вживання алкоголю (особливо пива, міцних спиртних напоїв), солодких напоїв, жирної їжі, надлишкового споживання м’яса та морепродуктів. Рекомендоване введення до раціону молочних продуктів з низьким вмістом жирів, а також регулярні фізичні вправи.
3. Кожного хворого на подагру слід систематично обстежувати для виявлення супутніх захворювань і кардіоваскулярних факторів ризику (погіршення функції нирок, ІХС, інсульт, захворювання периферичних артерій, ожиріння, гіперліпідемія, АГ, ЦД і паління), що має розглядатися в якості обов’язкової складової лікування подагри.
Остаточні рекомендації з лікування хворих на подагру [10, 14]:
1. Лікування гострого нападу подагри необхідно розпочинати якомога раніше. Пацієнтів слід навчити самостійно приймати медикаменти за перших ознак загострення.
2. Рекомендованою терапією першої лінії гострого нападу подагри є колхіцин (протягом 12 год з моменту загострення) з навантажувальної дози 1 мг, через 1 год — наступний прийом в дозі 0,5 мг, за необхідності — разом з ІПП, пероральні ГК (преднізолон у дозі 30–35 мг/добу протягом 3–5 днів) або аспірація вмісту суглоба з ін’єкцією кортикостероїду. Слід уникати призначення колхіцину і НПЗЗ пацієнтам з тяжкими порушеннями функції нирок. Колхіцин недоцільно застосовувати у лікуванні хворих, які отримують інгібітори Р-глікопротеїну і/або CYP ЗА4, такі як циклоспорин або кларитроміцин.
3. Доцільно розглянути призначення НПЗП, ГК (пероральних та ін’єкційних форм), блокаторів інтерлейкіну-1 для лікування гострих подагричних атак у пацієнтів з частими загостреннями захворювання, що мають протипоказання до призначення колхіцину. Поточне інфекційне захворювання є протипоказанням для призначення блокаторів інтерлейкіну-1; урикостабілізувальну терапію (УСТ) слід коригувати до досягнення цільових значень урикемії після терапії загострення блокатором інтерлейкіну-1. Доведено, що інтерлейкін-1-бета відіграє важливу роль у розвитку запалення. У двох РКД встановлено, що антагоніст інтерлейкіну-1-бета моноклональне антитіло канакінумаб (150 мг п/ш, 1 доза) перевершує тріамцинолону ацетонід (40 мг п/ш, одна доза) в зменшенні вираженості больового синдрому в пацієнтів із загостренням захворювання. Ці дані сприяли схваленню зазначеного препарату в країнах Європи для лікування пацієнтів, що мають протипоказання до призначення колхіцину, НПЗП або стероїдів.
4. Профілактичну терапію рекомендується здійснювати протягом перших 6 міс УСТ. З цією метою застосовується колхіцин у дозі 0,5–1 мг/добу (у хворих із порушеннями функції нирок слід знизити дозу препарату) (!). При порушенні функції нирок або застосуванні статинотерапії пацієнтам і лікарям необхідно враховувати потенційну нейрональну і/або м’язову токсичність колхіцину. Слід уникати одночасного призначення з колхіцином інгібіторів Р-глікопротеїну і/або CYP ЗА4. Якщо пацієнт не переносить колхіцин або є протипоказання до його призначення, необхідно розглянути доцільність профілактичного застосування низьких доз НПЗП. Було доведено, що профілактика загострень низькими дозами колхіцину (0,6 мг/добу) або НПЗП (напроксен 250 мг 2 рази на добу) протягом 6 міс є більш ефективною, ніж 8-тижнева профілактика.
5. УСТ показана всім хворим з частими рецидивами (≥2 на рік), що мають тофуси, уратну артропатію і/або конкременти в нирках. УСТ розпочинається безпосередньо після початкового підтвердження діагнозу в пацієнтів молодого віку (<40 років) або при дуже високій КСК (>8 мг/дл, 480 мкмоль/л) і/або за наявності супутніх захворювань (порушення функції нирок, АГ, ІХС, СН). УСТ дозволяє розчинити кристалічні відкладення і нівелювати прояви подагри за умови підтримання цільових значень урикемії. Ефективна УСТ зменшує розміри і кількість тофусів, полегшує їх зникнення, покращує якість життя хворих на подагру. У деяких дослідженнях встановлено, що подагра є фактором ризику летального результату, особливо асоційованого з кардіоваскулярними порушеннями, а також погіршення функції нирок. Зволікання з призначенням УСТ до другої або третьої атаки може призвести до більш значного навантаження кристалами, що ускладнює їх розчинення і продовжує існування гіперурикемії, яка здатна чинити руйнівний вплив на серцево-судинну систему і нирки.
6. У пацієнтів, які отримують УСТ, слід підтримувати КСК на рівні <6 мг/дл (360 мкмоль/л). Підтримання більш низьких цільових значень КСК з метою полегшення розчинення кристалів рекомендується пацієнтам з тяжким перебігом подагри (тофуси, хронічна артропатія, часті атаки) аж до повного розчинення кристалів. Не рекомендується зберігати КСК <3 мг/дл протягом тривалого часу. Рекомендовано знижувати КСК до <5 мг/дл при тяжкій подагрі, яка характеризується високим кристалічним навантаженням, аж до повного розчинення кристалів. Після повного їх розчинення КСК слід підтримувати на рівні <6 мг/дл за допомогою зниження дози УСТ для запобігання утворенню нових уратних кристалів.
7. Усі препарати, що використовуються для УСТ, слід починати приймати в найнижчій дозі, а потім титрувати аж до досягнення цільових значень КСК. Необхідно довічно підтримувати КСК <6 мг/дл (360 мкомоль/л).
8. Хворим зі збереженою функцією нирок в якості препарату першої лінії для проведення УСТ рекомендується алопуринол (100 мг/добу), дозу якого слід підвищувати на 100 мг кожні 2–4 тиж до досягнення цільових значень урикемії. Якщо цільові значення КСК не можуть бути досягнуті на тлі застосування відповідної дози алопуринолу, останній слід замінити на фебуксостат або інші урикозуричні препарати чи застосувати їх комбінацію. Застосування алопуринолу слід починати з низьких доз (100 мг/добу) з метою зниження ризику раннього загострення. Найчастіше алопуринол призначається у дозі 300 мг/добу — це дозволяє досягти цільових значень КСК <6 мг/дл (360 мкмоль/л) у 30–50% пацієнтів зі збереженою функцією нирок. У таких випадках група експертів рекомендує використовувати стратегію підвищення дози для досягнення визначених цільових значень КСК. Лікування алопуринолом у дозі 600–800 мг/добу в 75–80% випадків є успішним і дозволяє досягти КСК <6 мг/дл (360 мкмоль/л). Фебуксостат вважається потужним непуриновим селективним інгібітором ксантиноксидази. Препарат дозволений для застосування в Європі в добових дозах 80 і 120 мг. Фебуксостат метаболізується в печінці; ниркова екскреція не є основним шляхом елімінації, що дозволяє використовувати препарат у пацієнтів з легкою/середньотяжкою нирковою недостатністю. У широкомасштабних РКД доведено перевагу фебуксостату (80 або 120 мг) над алопуринолом (300 мг) стосовно зниження рівня урикемії (!). У фундаментальному дослідженні з фебуксостатом були зареєстровані побічні ефекти з боку шкірних покривів. Урикозуричні препарати у вигляді монотерапії або в поєднанні з алопуринолом рекомендується призначати у тих випадках, коли застосування тільки алопуринолу виявилося недостатньо ефективним. Бензбромарон (50–200 мг/добу) є більш потужним урикозуричним препаратом у порівнянні з пробенецидом (1–2 г/добу). У РКД за участю пацієнтів, у яких терапія алопуринолом (300 мг/добу) не сприяла належному контролю урикемії, 65% хворих досягли цільових значень КСК ≤5 мг/дл (300 мкмоль/л) після призначення 200 мг бензбромарону або 2 г/добу пробенециду. Рекомендації EULAR (2016) з лікування гіперурикемії у хворих на подагру представлені схемою 6.3.

Схема 6.3. Рекомендації EULAR (2016)з лікування гіперурикемії у хворих з подагрою
9. У пацієнтів з порушеною функцією нирок необхідно коригувати максимальну дозу алопуринолу залежно від КК. У тому разі, якщо цільова КСК не може бути досягнута на тлі прийому цієї дози препарату, хворому слід призначити фебуксостат або бензбромарон з/без алопуринолу, за винятком пацієнтів з ШКФ <30 мл/хв.
10. Пацієнтам з тяжким виснажливим перебігом хронічної тофусної подагри і низькою якістю життя показане призначення пеглотикази за умови неможливості досягнення цільових значень КСК за допомогою будь-яких інших препаратів у максимальній дозі (у тому числі комбінації лікарських засобів).
11. Пеглотиказа визнана потужним уратзнижувальним препаратом для лікування рефрактерної подагри. Рекомендується використовувати цей лікарський засіб тільки у лікуванні пацієнтів з тяжкою подагрою за підтвердженої наявності кристалів, які не можуть бути вилікувані за допомогою традиційної УСТ, зокрема комбінації інгібітора ксантиноксидази і урикозуричного препарату. Наразі немає даних про рекомендовану тривалість лікування пеглотиказою.
12. Якщо подагра розвивається у хворого, який приймає петльові або тіазидні діуретики, слід замінити діуретик (за можливості); якщо має місце АГ, необхідно призначати БРА лосартан або АК амлодипін (!). За наявності гіперліпідемії слід рекомендувати статини або фенофібрат, які мають урикозуричні властивості.
В алгоритмі 6.10 представлено узагальнену схему лікування подагри з урахуванням рекомендацій ACR, 2012, та EULAR, 2014.
| Алгоритм 6.10. Принципи лікування подагри [11, 19]
Крок 1. Нефармакологічні методи лікування: 1. Використання тепла або холоду місцево слід розглядати як доповнення до основної терапії. 2. Лікувальна фізкультура повинна бути основним методом лікування пацієнтів з подагрою, незалежно від віку, супутніх захворювань, вираженості болю або непрацездатності. Фізичні вправи повинні включати місцеве зміцнення м’язів і загальний аеробний фітнес. 3. Медичні працівники повинні розглядати питання про використання черезшкірної електричної стимуляції нервів як доповнення до основного лікування щодо зменшення вираженості болю. 4. Доцільно давати поради щодо відповідного взуття (зокрема взуття з амортизацією), що є частиною основного лікування пацієнтів з остеоартрозом нижніх кінцівок. У пацієнтів з остеоартрозом, які мають біохімічний біль у суглобах або нестабільність, необхідно розглядати питання про скоби/устілки/опори на додаток до основного лікування. Допоміжні пристрої (наприклад тростини та ін.) слід розглядати як доповнення до основного лікування для пацієнтів з остеоартрозом, які мають специфічні проблеми в повсякденній діяльності. 5. Зміни способу життя: здорова дієта, зменшення надлишкової маси тіла, регулярне виконання фізичних навантажень, відмова від паління та надмірного вживання алкоголю призводить до часткового зниження рівня сечової кислоти. Однак дотримання дієти дозволяє знизити його лише на 10%, тому пацієнтам з високим рівнем сечової кислоти обов’язково призначається гіпоуремічна терапія. Крок 2. Лікування гострого нападу подагри: колхіцин по 2 мг/добу, НПЗП або ГК (внутрішньосуглобово, перорально чи в/м залежно від наявності супутніх захворювань і ризику негативних реакцій). При тяжких загостреннях рекомендується застосування комбінації ГК і колхіцин перорально та внутрішньосуглобово. Крок 3. Патогенетична корекція гіперурикемії. З-поміж препаратів І лінії гіпоуремічної терапії рекомендуються інгібітори ксантиноксидази (алопуринол або фебуксостат), які перешкоджають перетворенню гіпоксантану в ксантан. У якості альтернативи можна використовувати урикозуричні препарати (бензбромарон, пробенецид). Застосування рекомендованої PEG урокінази доцільне тільки при тяжкій формі подагри, коли інші препарати неефективні. Крок 4. Лікування резистентної форми подагри. У випадку відсутності покращення (зменшення вираженості симптоматики за візуально-аналоговою шкалою <20% протягом 24 год або <50% в період понад 24 год) необхідно перейти на інший препарат — інгібітор інтерлейкіну-1 (анакінра в дозі 40 мг п/ш). Крок 5. Профілактична терапія в період між нападами, спрямована на зниження загострення. Профілактика здійснюється за допомогою колхіцину (до 1,2 мг/добу), а за наявності протипоказань або у випадку поганої переносимості використовуються НПЗП або низькі дози ГК (тривалість терапії — не менше 3 міс за умови досягнення рівня сечової кислоти 360 мкмоль/л і відсутності тофусів; за їх наявності — 6 міс). Крок 6. Лікування за наявності тофусів. Необхідно досягти стійкого зниження сироваткового рівня сечової кислоти за допомогою підтримувальних доз гіпоуремічних препаратів. За легкого та помірного порушення ниркової функції (КК >30 мл/хв.) алопуринол може застосовуватися тільки за умови ретельного моніторингу стосовно негативних реакцій (препарат призначають у низьких дозах для досягнення нормального рівня вмісту сечової кислоти). У пацієнтів з нормальним рівнем сечової кислоти застосовують алопуринол у дозі 300 мг/добу. Фебуксостат — селективний інгібітор ксантиноксидази, що метаболізується в печінці, застосовують при легкому і серйозному перебігу подагри без зниження дози. |
Помірною урикозуричною дією характеризуються лозартан і фенофібрат (!). Діуретики хворим з подагрою призначають тільки за життєвими показаннями (ХСН, набряк легень). Як правило, діуретики при подагрі не застосовують.
Лікування гострого подагричного артриту розглянуто в табл. 6.41.
Таблиця 6.41. Системна терапія при гострому подагричному артриті (Terkeltaub R.A., 2006)
| Препарати | Схема лікування | Примітки |
| Неселективні інгібітори ЦОГ-2 | ||
| Напроксен | Перорально 750–1000 мг/добу 3 дні, потім 50–750 мг/добу (розділити на 2 прийоми) 4–7 днів | Не рекомендується хворим з нирковою, печінковою недостатністю та захворюваннях ШКТ |
| Селективні інгібітори ЦОГ-2 | ||
| Целекоксиб | Перорально 400 мг в 1-й день, потім 200 мг/добу (розділити на 2 прийоми) 6–10 днів | Обережно застосовувати при захворюваннях ШКТ (включаючи пептичну виразку). Можливий кардіоваскулярний ризик |
| Системні кортикостероїди | ||
| Преднізолон | 40–60 мг/добу, потім кожні 3 дні знижувати дозу на 10–15 мг/добу | Не рекомендується при септичному ураженні суглобів |
| Метилпреднізолон | 100–150 мг/добу | |
| Колхіцин | При гострому епізоді подагри протягом декількох годин — перорально 0,6 мг через кожну годину протягом 3 год (максимальна доза — 3 таблетки), потім по 0,6 мг 2 рази на добу при КК >50 мл/хв; 0,6 мг — при КК 35–49 мл/хв; 0,6 мг через кожні 2–3 дні — при КК 10–34 мл/хв. Не рекомендується при КК <10 мл/хв проведення гемодіалізу в осіб з клінічними проявами печінкової та ниркової недостатності. Слід знизити вказані дози вдвічі для осіб віком ≥70 років | Більш тривалі схеми лікування не рекомендуються у зв’язку з можливим виникненням нудоти, блювання, діареї, зневоднення. Через 1 добу ефективність колхіцину знижується. При тривалому застосуванні колхіцину необхідно контролювати рівень КФК, кровотворення в кістковому мозку. Еритроміцин, симвастатин і циклоспорин підвищують токсичний ефект колхіцину. Не рекомендується вводити колхіцин в/в |
Особливості взаємодії ліків з протиподагричними препаратами наведені в табл. 6.42.
Таблиця 6.42. Взаємодія ліків з протиподагричними препаратами
| Лікарський засіб | Препарати, з якими можлива взаємодія | Потенційний побічний ефект | Корекція дози/контроль |
| НПЗП | Варфарин | Підвищується ризик гастроінтестинальних кровотеч | Зниження дози НПЗП або варфарину |
| Інгібітори АПФ | Гіпертензія і потенційне погіршення функції нирок | Зниження дози НПЗП або варфарину | |
| Колхіцин | Інгібітори CYP PA4 і Р-глікопротеїну | Підвищення ризику колхіцин-індукованих токсичних ефектів | Зниження дози колхіцину |
| Алопуринол | Фуросемід | Підвищення плазмової концентрації оксипуринолу | Можуть знадобитися більш високі дози алопуринолу |
| Азатіоприн | Підвищення концентрації 6-меркаптопурину, що призводить до мієлосупресії | Зниження дози азатіоприну на 50–75% і використання більш низької дози алопуринолу; контроль рівня лейкоцитів, тромбоцитів, еритроцитів | |
| Пробенецид | Зниження оксипуринолу в плазмі | ||
| Варфарин | Може підвищувати антикоагулянтний ефект | Моніторинг МНВ | |
| Інгібітори АПФ | Можуть підвищувати ризик алергічних реакцій на алопуринол | ||
| Теофілін | Збільшення часу напівжиття теофіліну в сироватці крові | ||
| Пеніцилін | Підвищується ризик шкірних висипів | ||
| Лікарський засіб | Препарати, з якими можлива взаємодія | Потенційний побічний ефект | Корекція дози/контроль |
| Фебуксостат | Азатіоприн | Формально не підтверджено, але існують докази збільшення концентрації 6-меркаптопурину, що пов’язано з гальмуванням ксантиноксидази внаслідок мієлосупресії | Уникати поєднання |
| Пеглотиказа | Інші уратзнижувальні препарати | Можуть маскувати відсутність реакції на пеглотиказу і тим самим підвищити ризик побічної реакції | Уникати поєднання |
Тактика лікування подагри наведена в алгоритмі 6.11.
| Алгоритм 6.11. Тактика раціонального застосування антиподагричних засобів
1. При легкому перебігу подагри (кризи виникають 1–2 рази на рік, відсутність тофусів, нефропатії) і невисокій гіперурикемії (не вище 0,5 ммоль/л) призначають дієту № 6, лужні мінеральні води до 2 л/добу; курсове лікування менш активними антиподагричними препаратами (оротова кислота, етамід). 2. При середньотяжкому та тяжкому перебігу подагри (наявний рівень гіперурикемії при метаболічному типі гіперурикемії з високим рівнем сечової кислоти) застосовують урикодепресанти (алопуринол, тіопуринол, комбінований препарат, що містить алопуринол і бензобромарон); при нирковому типі гіперурекемії з недостатнім виділенням сечовини з сечею (менше 3,5 ммоль/добу), але за відсутності ХНН, нирковокам’яної хвороби, захворювань печінки, ШКТ застосовують тільки урикодепресанти (алопуринол, фебуксостат, бензбромарон). 3. При змішаному типі гіперурикемії (висока гіперурикемія і зменшення виділення сечової кислоти нирками — менше 3,56 ммоль/добу) здійснюють лікування комбінованим препаратом, що містить алопуринол і бензобромарон чи комбінацією урикодепресантів і урикоелімінаторів в оптимальних дозах залежно від кількості сечової кислоти в крові та в добовій сечі. 4. При розвитку подагричного суглобового кризу застосовують колхіцин чи інші протизапальні препарати на тлі лікування основного захворювання. Хворим з частими та тяжкими кризами показані тривалі курси лікування колхіцином. |
Критерії ефективності лікування подагри [5, 10, 11, 14, 19]:
1. Нормалізація чи зниження клініко-лабораторних показників активності захворювання.
2. Нормалізація чи зниження рівня сечової кислоти в крові.
3. Зниження частоти подагричних атак, які призводять до втрати працездатності.
4. Зниження потреби в застосуванні НПЗП, колхіцину та ГК.
Прогноз при подагричному артриті у цілому сприятливий, але в 20–50% хворих виникає уролітіаз. Причиною смерті в 18–25% хворих на подагру є ХНН.
Профілактика подагри передбачає наступні заходи:
1) обстеження членів сім’ї хворого на виключення латентної гіперурикемії;
2) у разі виявлення гіперурикемії показане обмеження вживання алкоголю, жирної та білкової їжі та раціональне лікування урикодепресивними та урикозуричними засобами;
3) малокалорійна та низьковуглеводна дієта з включенням ПНЖК (призводить до зниження рівня сечової кислоти);
4) заняття фізкультурою та спортом, що сприяє видаленню уратів з організму.
5) для профілактики гострого нападу при подагрі застосовують колхіцин у низьких дозах або НПЗП.
Результати доказової медицини при подагрі:
1. Дієтотерапії при подагрі присвячене єдине РКД, яке показало, що споживання деяких харчових продуктів, збагачених глікомакропептидом і екстрактом молочного жиру, знижувало ризик виникнення нападу артриту в порівнянні з плацебо. Декілька масштабних досліджень показали дозозалежний ефект регулярного вживання кави незалежно від наявності кофеїну. Зовсім незначне зниження рівня сечової кислоти спричиняє вживання екстракту зеленого чаю. Безпечним є вживання невеликої кількості сухого вина при порушеннях жирового, вуглеводного обміну та зниженні АТ. Однак вплив дієти на зниження рівня сечової кислоти у переважній більшості випадків є недостатнім, тому застосовують урикознижувальні препарати. Водночас їх ефективність повинна бути оцінена після купірування гострого артриту.
2. НПВП та ГК складають конкуренцію колхіцину в купіруванні больового синдрому при подагрі. Чим раніше призначаються НПЗП, тим більшою є вірогідність досягнення швидкого анальгезивного ефекту. При подагрі найчастіше застосовують НПЗП німесулід по 200 мг/добу. Більше 2/3 пацієнтів відзначали, що німесулід ефективно зменшував вираженість болю в суглобах у порівнянні з іншими НПЗП. Відсутність анальгезивної дії німесуліду при подагрі у деяких хворих протягом 3 міс пояснюють поліартикулярним пошкодженням [14].
3. Внутрішньосуглобове введення ГК при подагричному артриті не рекомендоване, оскільки преднізолон у дозі 30–35 мг/добу протягом 3–5 днів не є ефективнішим за НПЗП. У РКД введення при подагрі 7 мг бетаметазону або інфузії метилпреднізолону (500 мг) спричиняли численні побічні реакції (підвищення АТ, ознаки ішемії міокарда за даними ЕКГ тощо). За наявності протипоказань до НПЗП та ГК можливе призначення інтерлейкіну-1.
4. Алопуринол необхідно призначати не раніше ніж через 2 тиж після купірування нападу артриту в стартовій дозі 100 мг та доведення дози навіть до 900 мг/добу. Дуже обережно призначають препарат при розвитку ХХН.
5. Колхіцин — один з найдавніших препаратів з-поміж тих, що застосовуються в лікуванні подагри. Протизапальний ефект колхіцину зумовлений дезінтеграцією мікротубул нейтрофілів і пригніченням їх міграції. Екскреція колхіцину триває кілька днів, оскільки він залишається у зв’язаному стані. Близько 20% колхіцину екскретується нирками. Препарат піддається інтенсивному метаболізму в печінці. У 2010 р. опубліковано результати РКД AGREE, в якому вивчалась ефективність різних доз препарату. При гострому подагричному артриті порівнювалася доза 1,8 мг колхіцину, прийнята за 1 год. Низькі дози препарату продемонстрували профіль небажаних явищ, аналогічний профілю плацебо. Високі дози колхіцину спричиняють значну діарею у 76,9% випадків; низькі дози — у 23% пацієнтів. Колишні схеми лікування гострого нападу подагри, коли колхіцин призначали по 0,6 мг щогодини до повного купірування нападу, є надто токсичними, а за дієвістю не відрізняються від використання низьких доз. В іншому дослідженні використання колхіцину в лікуванні хворих на подагру при стабільній стенокардії в дозі 0,5 мг/добу у комбінації зі статинами призводило до зниження частоти ГКС, позалікарняної зупинки серця та кардіоваскулярного ішемічного інсульту. Традиційна схема застосування колхіцину передбачає старт із дози 1,2 мг з подальшим прийомом у дозі 0,6 мг через 1 год. При комбінованому застосуванні колхіцину з Р-глікопротеїном дозу необхідно знижувати: 0,6 мг з подальшим прийомом через 1 год у дозі 0,3 мг.
6. Інгібітори інтерлейкіну-1. Стимулюють кристали сечової кислоти інтерлейкін-1 бета, що може сприяти розвитку хронічного запалення й деструктивного процесу. Інтерлейкіни-1-бета при гострому нападі подагри більш ефективні, ніж при застосуванні НПЗП [10].
7. Перспективним засобом лікування хворих на подагру є канакінумаб. У РКД СANTOS заплановано вивчення застосування канакінумабу у дозі 50/150/300 мг протягом 4 років.
8. Фебуксостат — це непуриновий інгібітор ксантиноксидази, формула якого відрізняється від алопуринолу. У РКД FACT фебуксостат і алопуринол застосовували у різних дозах при подагрі. Клінічні дослідження показали, що фебуксостат є більш ефективним засобом для зниження рівня сечової кислоти в дозі 80 мг/добу порівняно з алопуринолом у дозі 300 мг/добу. Переносимість препарату була доброю в усіх дослідженнях.
9. Пеглотиказа знижує концентрацію уратів унаслідок ферментативної деградації сечової кислоти. Незначну кількість серйозних серцево-судинних побічних реакцій під час застосування препарату зафіксовано у пацієнтів з наявністю факторів ризику кардіальних подій та тривалим анамнезом кардіоваскулярних захворювань.