Перикардит — запалення вісцерального і парієтального листків перикарда інфекційного або неінфекційного генезу, що проявляється фіброзними змінами і/або накопиченням рідини в порожнині перикарда.
Епідеміологія
У клініці перикардит діагностується не часто — у 0,1% випадків, його частота за даними аутопсії становить 3–6%. Чоловіки хворіють в 1,5 раза частіше, ніж жінки.
Етіологія
Перикардит найчастіше є проявом або ускладненням загального інфекційного захворювання, пневмонії, ІХС, некоронарогенних хвороб серця, системних захворювань сполучної тканини, алергічної реакції, пухлинного або аутоімунного процесу.
Етіологічними факторами гострого перикардиту можуть бути:
- інфекції;
- віруси (30–50%): Коксакі, ECHO, Епштейна — Барр, епідемічного паротиту, вітряної віспи, краснухи, імунодефіциту людини, цитомегаловірус, парвовірус В19;
- бактерії (5–10%): пневмокок, стафілокок, менінгокок, трепонема, боррелія, хламідія, мікобактерії туберкульозу;
- гриби: кандида, гістоплазма;
- паразити: амеба, ехінокок;
- гострий ІМ (епістенокардичний перикардит) (5–20%);
- міокардит (30%);
- метаболічні порушення: уремія, ниркова недостатність, мікседема (30%), холестериновий перикардит;
- новоутворення;
- травми: при прямому або непрямому ушкодженні перикарда;
- системні аутоімунні захворювання: гостра ревматична лихоманка (20–50%); колагенози: ревматоїдний артрит (30%), склеродермія (>50%), системний червоний вовчак (30%);
- аутоімунні процеси (ушкодження): постінфарктний синдром Дресслера (1–5%), постперикардіотомний синдром (через 10–14 діб після операції) (<20%), перфорація катетером;
- ідіопатичний (вірусна етіологія не встановлена) (3–50%).
Класифікація
На сьогодні в Україні прийнята класифікація перикардиту, затверджена на VI Конгресі кардіологів України (Київ, 2000):
I. Етіологічна характеристика:
- перикардит при бактеріальних інфекціях I32.0;
- перикардит при інфекційних і паразитарних хворобах I32.1;
- перикардит при інших хворобах I32.8;
- перикардит неуточнений I31.9.
II. Патогенетичні і морфологічні варіанти:
- хронічний адгезивний I31.0;
- хронічний констриктивний I31.0, у тому числі кальциноз перикарда;
- гемоперикард I31.2;
- перикардіальний випіт (незапальний) — гідроперикард (I31.3), у тому числі хілоперикард.
III. Характер перебігу: гострий (I30), хронічний, прогресуючий.
IV. Оцінка ступеня вираженості перикардіального випоту за даними ультразвукових та інших методів дослідження (незначна, помірна, виражена).
V. СН (0–III стадія, I–IV ФК).
Гострий перикардит триває <6 тиж, хронічний >6 тиж.
Патологічна анатомія
Виникнення перикардиту супроводжується посиленням ексудації рідких і дрібнодисперсних компонентів крові в порожнину перикарда. Вільно рухаючись у порожнині, ексудат інтенсивно резорбується не ураженими запальним процесом ділянками перикарда. Внаслідок зміни проникності судинної стінки, пропотівання грубодисперсних білків плазми крові, зокрема фібриногену, і випадіння його в осад у вигляді нашарувань фібрину, утворюється запальний інфільтрат і формується фібринозний (сухий) перикардит, який може бути обмеженим або розповсюдженим.
Нагромадження в порожнині значної кількості рідкого ексудату свідчить про порушення ефективного всмоктування і про поширення запального процесу на значну площу перикарда. В залежності від характеру ексудату розрізняють серозний, фібринозний, геморагічний, гнійний та гнильний перикардит. За характером незапального випоту розрізняють гідроперикард, гемоперикард, хілоперикард і холестериновий перикардит. Результатом гострого ексудативного перикардиту може бути часткова або повна організація випоту з утворенням перикардіальних зрощень. Локальний перикардит до накопичення в порожнині перикарда рідкого випоту не призводить.
При перикардиті, що здавлює (констриктивному перикардиті), фіброзне рубцювання і адгезія обох листків перикарда призводять до облітерації порожнини перикарда, в результаті чого утворюється тверда оболонка навколо серця; при тривалому перебігу процесу формується виражена кальцинація перикарда, в окремих випадках утворюється суцільне кільце навколо серця («панцирне» серце). На пізніх стадіях перебігу констриктивного перикардиту відбувається глибоке ураження міокарда шлуночків, локальні зміни поєднуються з міокардіофіброзом. М’язові волокна стають більш тонкими, відбувається їх жирове переродження і атрофія у зв’язку зі зниженням робочого навантаження на шлуночки. Маса серця (без капсули, що здавлює) у хворих, померлих від констриктивного перикардиту, не перевищує 300 г.
Патологічна фізіологія
Гострий фібринозний (сухий) перикардит не супроводжується порушенням гемодинаміки, оскільки повільне збільшення кількості рідини викликає поступове розтягнення зовнішнього листка перикарда. При швидкій ексудації реалізується «опорна» функція перикарда, що обмежує діастолічне розширення камер серця. Тканина перикарда еластична при невеликому розтягненні (діастола шлуночків), але швидко втрачає еластичні властивості при більшому ступені розтягнення.
Порушення кровообігу (зниження АТ, венозний застій) виникають, якщо тиск всередині перикардіальної порожнини досягає 50–60 мм вод. ст. При цьому венозний тиск підвищується, перевищуючи на 20–30 мм вод. ст. внутрішньоперикардіальний і цим забезпечує у нових умовах діастолічне наповнення камер серця. Якщо об’єм ексудату досягає критичного рівня, що викликає значне здавлення серця, виникає тампонада серця, розвиток якої залежить від швидкості накопичення ексудату (при швидкому накопиченні 200 мл випоту).
При злипливому (адгезивному, спайковому) перикардиті розрізняють два механізми здавлення серця — первинний і вторинний. При первинному відбувається справжня ретракція рубцьової капсули, порушення гемодинаміки настають швидко, частіше через кілька тижнів після початку захворювання. При вторинному здавленні істотного зменшення об’єму перикардіального мішка не відзначають, але він втрачає свою еластичність, граничний розмір серця жорстко обмежений, порушення гемодинаміки розвиваються протягом декількох років.
Клінічна картина і діагностика
Гострий сухий перикардит
Проявляється тріадою клінічних симптомів — болем у грудній клітці, шумом тертя перикарда та змінами на ЕКГ.
Біль у ділянці серця виникає раптово, має різну інтенсивність, постійний характер, не купірується прийомом нітрогліцерину, посилюється під час кашлю, чхання, ковтання, дихання, триває кілька годин, тимчасово зменшується під дією анальгетиків. Біль локалізується, як правило, в центрі грудної клітки з іррадіацією в спину, а також у ділянку верхівки серця, можливе поширення болю в шию, спину, ліве плече. Інтенсивність болю залежить від дихання, руху, зміни положення тіла, зменшується у положенні сидячи з нахиленим вперед тулубом, а також у колінно-ліктьовому положенні.
Частими скаргами є напади серцебиття, сухий кашель, задишка, загальна слабкість, озноб. У результаті подразнення діафрагмального нерва можуть з’являтися гикавка і блювання. У деяких випадках хворі скаржаться на підвищену пітливість, субфебрильну температуру тіла, зниження АТ.
Патогномонічним симптомом є шум тертя перикарда, що носить непостійний характер, може зникати протягом декількох годин і з’являтися наступного дня; частіше шум поступово поширюється і посилюється. За характером шум такий, що шкребе (нагадує хрускіт снігу), мінливий, прослуховується в систолу і/або діастолу, краще вислуховується в зоні абсолютної тупості серця, як правило, нікуди не проводиться, іноді може виявлятися тільки при значному натисненні стетоскопом на стінку грудної клітки. Звичайно шум тертя перикарда має три фази: систолічний і ранній діастолічний компоненти у більш пізній фазі діастоли супроводжуються третім компонентом, пов’язаним із передсердним скороченням. Шум трифазний у 50%, двофазний — у 33% і монофазний — у 10% хворих.
ЕКГ-зміни визначають при гострій формі перикардиту, особливо інфекційної етіології, коли превалює супутнє запалення поверхневого шару міокарда. Запалення субепікардіального шару міокарда пов’язують із механізмом, що призводить до змін сегмента ST і зубця T, тоді як запалення у передсерді призводить до змін сегмента PR, які можуть передувати змінам сегмента ST. Виділяють 4 фази змін ЕКГ: 1-ша стадія — елевація сегмента ST у стандартних і грудних відведеннях з переходом у високий позитивний зубець Т — 90%; 2-га — сегмент ST знижується до ізолінії і ЕКГ-крива не має відхилень від норми, 3-тя — зубець Т поступово сплощується і через 10–15 днів стає двофазним або негативним у тих відведеннях, у яких відбувалася динаміка сегмента SТ, 4-та — ЕКГ нормалізується. У більшості пацієнтів зберігається синусовий ритм.
При рентгенологічному дослідженні збільшення серця не відзначають.
При ехоКГ-дослідженні можна визначити потовщення листків перикарда, наявність незначного випоту.
Радіонуклідне сканування з індієм-111 і галієм-67 дозволяє встановити діагноз перикардиту, виявити ділянки перикарда з вираженим запальним процесом.
Обсяг лабораторного обстеження визначається основним захворюванням, відзначається помірне підвищення ШОЕ, рівня ЛДГ і СРБ у сироватці крові, помірний лейкоцитоз і зсув лейкоцитарної формули вліво. Можуть визначатися маркери ушкодження міокарда: підвищення рівня тропоніну I і Т, МВ-фракції КФК. Рівень тропоніну I у сироватці крові підвищується у хворих із елевацією сегмента ST і гострим перикардитом, відображаючи ступінь ушкодження епікарда і міокарда, але при цьому не є негативним прогностичним маркером.
Про супутній периміокардит свідчать загальна або локальна дисфункція міокарда, підвищення в крові рівня тропонінів I і Т, МВ-фракції КФК, міоглобіну і ФНП-α.
Специфічні діагностичні тести повинні включати шкірні туберкулінові проби, визначення ревматоїдного фактора і титру антинуклеарних антитіл, дослідження на віруси, при необхідності — отримання гемокультури.
Перебіг гострого перикардиту доброякісний. Прогноз у більшості пацієнтів сприятливий. Повне одужання відбувається навіть без лікування, проте можливі рецидиви, зумовлені аутоімунним механізмом, і прогресування захворювання у подальшому з розвитком ексудативного перикардиту.
Ексудативний перикардит
Найбільш часто є наслідком інфекційного, а в ряді випадків — алергічного запалення, зазвичай ускладнює перебіг ревматизму, туберкульозу, стафілококової і стрептококової інфекції. Слід враховувати, що крім ексудату, рідина в порожнині перикарда може являти собою транссудат (гідроперикард), гній (піоперикард), кров (гемоперикард).
Клінічна картина гострого ексудативного перикардиту залежить від об’єму ексудату в порожнині перикарду і тяжкості інфекційного процесу, частіше безсимптомна, проте можуть визначатися наступні клінічні симптоми:
- синусова тахікардія;
- субфебрильна лихоманка;
- виражена постійна задишка;
- вимушене положення хворого — сидячи з нахилом тулуба вперед, нерідко хворий стає на коліна й притискається обличчям до подушки;
- при стисненні ексудатом нижньої порожнистої вени збільшується і стає болючою печінка, швидко наростають явища асциту, з’являються набряки на ногах;
- вибухання грудної клітки в ділянці проекції серця;
- послаблення або зникнення верхівкового поштовху;
- зниження АТ.
При фізикальному обстеженні визначається розширення площі серцевої тупості в усі сторони, а також збільшення ширини судинного пучка в другому міжребер’ї, конфігурація серця нагадує дах з трубою. Границі абсолютної серцевої тупості стають розширеними і їх межі співпадають з границями відносної тупості. У положенні на спині ділянка серцевої тупості заокруглюється, у вертикальному положенні нагадує неправильний трикутник у зв’язку з переміщенням рідини під дією сили ваги донизу.
Аускультативно визначається глухість тонів серця, іноді ритм галопу, мають місце часті порушення ритму серця.
При перкусії легень у нижніх відділах зліва можливе притуплення перкуторного тону, при аускультації з’являються бронхофонія, бронхіальний відтінок дихання у зв’язку із здавленням легеневої тканини збільшеним перикардом; притуплення перкуторного звуку зменшується при нахилі тіла вперед.
За даними лабораторних досліджень виявляють прискорення ШОЕ і збільшення кількості лейкоцитів, зсув лейкоцитарної формули вліво, підвищення рівня альфа-глобулінів, фібриногену, гаптоглобіну в сироватці крові.
При рентгенологічному дослідженні виявляють наступні зміни:
- кардіомегалія при накопиченні в порожнині перикарда 200–300 мл рідини;
- перехід гострого печінково-серцевого кута в тупий, зникнення талії серця;
- різке зниження амплітуди пульсації контурів серця аж до повного її зникнення при збереженні пульсації великих судин.
На ЕКГ виявляють зменшення вольтажу комплексу QRS і зубця T.
ЕхоКГ-обстеження є методом вибору, що дозволяє визначити кількість (навіть невелику — 50–100 мл) і характер випоту, включаючи наявність фібрину, повітря, пухлини, відкладення солей кальцію. За об’ємом випіт може бути незначним (<10 мм еховільного простору в систолу і діастолу), помірним (≥10 мм), значним (≥20 мм) і дуже значним (компресія серця).
При ехоКГ також можуть бути виявлені:
- ехонегативний простір між стінками ЛШ і зміщеним назад парієтальним листком перикарда; при великій кількості випоту ширина цього простору досягає 20 мм і більше (рис. 5.1а, б);
- гіперкінезія всього контуру серця та міжшлуночкової перегородки;
- порушення руху передсердно-шлуночкових клапанів;
- феномен «плаваючого», або «того, що хитається» серця при двомірній ехоКГ.
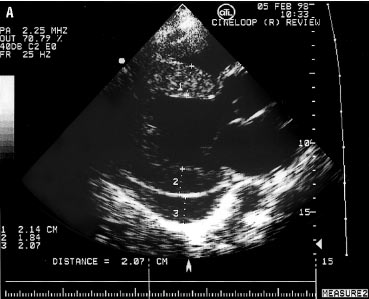
a

б
Рис. 5.1. Ексудативний перикардит. В-режим: а) парастернальна позиція, довга вісь; б) апікальна чотирикамерна позиція
Методи КТ і МРТ можуть застосовуватися для оцінки розміру і поширеності випоту, які дещо більші порівняно з тими, що визначаються при ехоКГ (рис. 5.2).
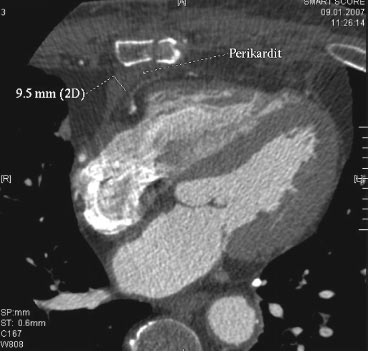
Рис. 5.2. Ексудативний перикардит. Метод мультиспіральної КТ, апікальний зріз
Перикардіоцентез проводять при підозрі на наявність гною в порожнині, туберкульозний або пухлинний генез ураження перикарда. Результатом ексудативного перикардиту може бути розсмоктування або організація випоту з утворенням перикардіальних спайок, зрощень, частковою або повною облітерацією серцевої сорочки. При хронічному ексудативному перикардиті найбільш ефективним є субтотальна перикардектомія, більшість хворих, що були прооперовані, видужують.
Тампонада серця
Виникає внаслідок накопичення випоту в перикардіальному просторі і підвищення тиску в порожнині перикарда, що призводить до здавлення серця і порушення кровообігу внаслідок зменшення серцевого викиду і системного венозного застою. Тампонада розвивається протягом декількох хвилин при розриві, травмі серця, проте частіше розвивається поступово. При швидкому накопиченні випоту в порожнині перикарда тампонада може виникнути при об’ємі випоту до 200–250 мл, при повільному накопиченні >1000 мл. Об’єм рідини, що призводить до розвитку тампонади, перебуває в прямій залежності від товщини міокарда та у зворотній залежності від товщини парієтального листка перикарда.
Клінічні ознаки тампонади варіюють від задишки і периферичних набряків до циркуляторного колапсу. Ранніми проявами тампонади є тахікардія, різко виражена задишка, набряки, підвищення венозного тиску з набряканням яремних вен, розширення меж абсолютної і відносної тупості серця. Можливе зниження АТ аж до розвитку колапса. При підгострому розвитку тампонади виявляють ознаки правошлуночкової недостатності з гепатомегалією, асцитом і плевральним випотом. Аускультативно визначається глухість тонів серця. Найважливішою ознакою тампонади серця є парадоксальний пульс — значне (>10 мм рт. ст.) зниження САТ під час фази вдиху.
ЕхоКГ дозволяє встановити точний діагноз шляхом виявлення перикардіального випоту і його локалізації. Якщо обсяг перикардіального випоту при ехоКГ-дослідженні становить 15–35 мл, листки перикарда при дослідженні визначаються окремо від епікарда.
Найбільш істотною ознакою тампонади серця при ехоКГ-дослідженні є зменшення діастолічного розміру ЛШ у фазу вдиху (рис. 5.3а, б), а також виражені зміни швидкості потоку через мітральний і трикуспідальний клапани або зміни викиду ЛШ під час дихання, що виявляються при імпульсно-хвильовій допплєрографії.
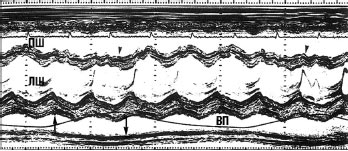
а
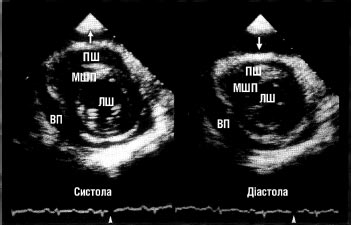
б
Рис. 5.3. Тампонада серця: а) М-режим (ВП — випіт у перикард). Стрілка вгору позначає початок вдиху, стрілка вниз — початок видиху; б) B-режим, парастернальна позиція, коротка вісь
За допомогою допплєрівського дослідження можна кількісно визначити кровотік через мітральний і тристулковий клапани, ЛА і вени. Дихальні коливання амплітуди трансмітрального піка Е >25% і транстрикуспідального піка Е >40% дають підставу запідозрити наявність тампонади серця.
Катетеризація порожнин серця історично була діагностичним стандартом при тампонаді серця і залишається важливим діагностичним методом, особливо у випадках недостатньої інформативності неінвазивних методів дослідження. Катетеризацію правих відділів серця часто проводять одночасно з перикардіоцентезом для моніторування видалення випоту.
Констриктивний перикардит
Це найбільш тяжке захворювання перикарда, розвивається найчастіше в результаті туберкульозного, ревматичного або гнійного запалення перикарда. При цьому після перенесеного гострого фібринозного або серозно-фібринозного перикардиту виникає облітерація порожнини перикарда з утворенням грануляційної тканини, яка утворює щільний рубець, іноді з відкладенням солей кальцію, що порушує наповнення шлуночків. До констриктивного (стискаючого) перикардиту відносять випадки:
- циркулярного стиснення міокарда потовщеним склерозованим і непідатливим перикардом;
- хронічного значного випоту в порожнину перикарда, що стискає міокард;
- стиснення рубцями або кальцинованими ділянками певних відділів серця, його коронарних і магістральних судин із порушенням гемодинаміки.
Констриктивний перикардит тяжко діагностувати. Клінічний діагноз залежить від виявлення підвищеного венозного тиску у пацієнта, без будь-яких інших клінічних проявів хвороби серця. При значній констрикції виявляють ознаки застійної СН, включаючи набряки, асцит, анасарку, явища застою в печінці, спленомегалію, зниження толерантності до фізичних навантажень, кахексію. Часто визначають ознаки вираженого хронічного системного венозного застою, зумовленого малим хвилинним об’ємом серця: набрякання і пульсацію яремних вен, артеріальну гіпотензію з низьким пульсовим тиском. Симптоми прогресують і не піддаються консервативній медикаментозній терапії.
На ЕКГ може визначатися зниження амплітуди комплексу QRS, зменшення амплітуди або інверсія зубця Т, фібриляція передсердь, AV- блокада, порушення внутрішньошлуночкової провідності.
При рентгенологічному дослідженні можна виявити зменшення серцевої пульсації («тихе» серце), кальцинацію перикарда («панцирне» серце), плевральний випіт.
При ехоКГ-дослідженні виявляється потовщення перикарда і його кальцинація, прекардіальні зрощення, а також непрямі ознаки констрикції: збільшення лівого і правого передсердь при незміненій конфігурації шлуночків і систолічній функції, ранній парадоксальний рух міжшлуночкової перегородки — вбік ЛШ під час вдиху і вбік ПШ під час видиху внаслідок змін розміру шлуночка під час дихання, сплощення задньої стінки ЛШ унаслідок обмеженого діастолічного наповнення (рис. 5.4).
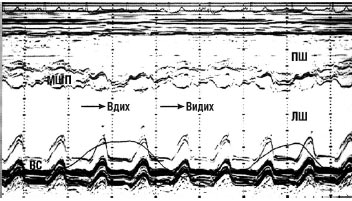
Рис. 5.4. Констриктивний перикардит. М-режим
При допплєрівській ехоКГ визначається обмеження наповнення ЛШ і ПШ, при оцінці трансклапанних AV-потоків розходження рівня наповнення в фазу вдиху і видиху перевищують 25%.
КТ грудної клітки і/або МРТ більш вірогідно допомагають встановити діагноз при виявленні перикардіального ущільнення: визначають потовщення і кальцинацію перикарда, звуження AV-борозен, застій у порожнистих венах, збільшення передсердь.
Із метою підтвердження діагнозу проводять перикардіоцентез і катетеризацію серця. При катетеризації серця виявляють характерні зміни: підвищення ЦВТ, ПШ і ЛШ нерозширені і нормально скорочуються, в них визначається майже повне вирівнювання кінцево-діастолічного тиску.
При ангіографії визначають зменшення розмірів ПШ і ЛШ, збільшення розмірів правого і лівого передсердь.
Лікування і профілактика
Відповідно до протоколу надання медичної допомоги хворим із гострим перикардитом, хронічним констриктивним перикардитом (наказ МОЗ України № 436 від 03.07.2006 р.) у перелік медичних послуг обов’язкового асортименту входить етіопатогенетичне лікування основного захворювання: застосування антибіотиків, НПЗП, ГКС, проведення перикардіоцентезу при значній кількості випоту та оперативного лікування при констриктивному перикардиті.
Хворих із гострим перикардитом слід госпіталізувати для визначення етіології, динамічної оцінки ефективності лікування та виключення тампонади серця.
Зниження частоти розвитку перикардиту при пневмонії та інших інфекційних захворюваннях досягнуто завдяки широкому застосуванню антибіотиків, що має вирішальне значення в профілактиці окремих видів перикардиту. Специфічний перикардит при різних інфекційних захворюваннях лікують антибіотиками після визначення чутливості виділених збудників. Якщо етіологія перикардиту не зясована, від проведення антибактеріальної терапії слід утриматися з огляду на зростаючу кількість неінфекційних форм, зумовлених сенсибілізацією організму.
При неспецифічному бактеріальному перикардиті застосовують бензилпеніцилін або його напівсинтетичні похідні, іноді у поєднанні з аміноглікозидами (гентаміцин, канаміцин, амікацин, стрептоміцин). При підвищеній чутливості до пеніциліну призначають цефалоспорини.
При інфекційному перикардиті неспецифічну терапію застосовують паралельно з ефективною антибіотикотерапією, оскільки етіотропна протимікробна терапія не має безпосереднього впливу на ексудативний і проліферативний компоненти запального процесу.
Основою терапії гострого перикардиту є застосування НПЗП протягом декількох днів або тижнів до зникнення перикардіального випоту. Хворим похилого віку не слід призначати індометацин, оскільки препарат знижує кровоток у коронарних артеріях. Відповідно до Європейських рекомендацій по лікуванню перикардиту (2004) кращим препаратом є ібупрофен, який сприятливо впливає на коронарний кровоток і має широкий діапазон терапевтичних доз. Початкова доза становить 300–800 мг кожні 6–8 год, таке лікування можна призначати протягом кількох тижнів до резорбції перикардіального випоту. При необхідності призначають гастропротекторні засоби для профілактики НПЗП-асоційованої гастропатії.
Для лікування гострого перикардиту та профілактики його ускладнень можна призначати колхіцин по 0,5 мг 2 рази на добу (як монотерапію, так і додатково до лікування НПЗП).
При алергічних і аутоімунних формах перикардиту неспецифічна протизапальна терапія відіграє провідну роль.
Системне застосування ГКС показано лише при захворюваннях сполучної тканини, аутоімунних процесах або уремії. Висока ефективність відзначається при внутрішньоперикардіальному введенні ГКС із метою запобігання розвитку системних побічних ефектів.
Преднізолон у низьких дозах (10–15 мг) застосовують також при перикардиті аутоімунної етіології у хворих з ІМ або після оперативного втручання на серці. Висока ефективність терапії ГКС хоча і дозволяє припустити аутоімунну природу перикардиту, проте не виключає його інфекційного генеза.
Тампонаду серця помірного ступеня тяжкості у деяких випадках можна лікувати консервативно, призначаючи сечогінні засоби з одночасною терапією основного захворювання. Діуретики зменшують вираженість симптомів застою. При фібриляції передсердь призначають антиаритмічні препарати.
При підвищеному ЦВТ у більшості випадків слід проводити видалення рідини з перикарда. Перикардіальний випіт може бути видалений за допомогою пункції (перикардіоцентез) або інших хірургічних методик (підмечовидна перикардіостомія, торакоскопічна перикардіостомія, торакотомія). Найбільш гострі форми тампонади серця типу гемоперикарда, зумовленого розшаруванням аорти, проникаючої травми серця або розриву стінки серця при гострому ІМ потребують проведення негайного хірургічного втручання.
Перикардіоцентез ефективний при більшості підгострих форм тампонади, наприклад зумовлених ідіопатичним або вірусним гострим перикардитом, ревматизмом, діалізом і новоутворенням. Торакоскопію і торакотомію, як правило, застосовують у пацієнтів із рецидивуючою тампонадою серця, яким спочатку було проведено перикардіоцентез або підмечовидну перикардіостомію, зазвичай при пухлинних процесах.
Показанням для перикардіоцентезу є тампонада серця, наявність ексудату об’ємом >20 мм у діастолу за даним ехоКГ, підозра на туберкульозний або гнійний випіт. Клінічне покращання звичайно наступає після видалення 100–200 мл рідини.
Проведення перикардіоцентезу протипоказано при дисекції аорти, а також у ситуаціях, коли діагноз може бути встановлений іншим методом або випіт невеликого об’єму і розсмоктується в результаті протизапального лікування. Відносні протипоказання включають некориговану коагулопатію, одночасне проведення терапії антикоагулянтами, тромбоцитопенію (<50 000/мм3), наявність невеликого ізольованого ексудату.
При констриктивному перикардиті консервативне лікування неефективно.
Верифікований діагноз є абсолютним показанням до перикардектомії — видалення обох листків спаяного перикарда.
При вираженій кальцинованій адгезії перикарда хірургічне втручання часто призводить лише до покращання стану і може супроводжуватися тяжким ушкодженням перикарда, ризиком крововиливу в результаті перфорації стінки серця. Альтернативним підходом може служити застосування ексимерного лазера. Після проведення перикардектомії повна нормалізація внутрішньосерцевої гемодинаміки досягається лише у 60% хворих. У ранній післяопераційний період ЦВТ може залишитися підвищеним, проте нормалізується протягом 3 міс після операції. Неадекватна тривалість періоду реконвалесценції після хірургічного видалення перикарда може вказувати на наявність супутньої патології міокарда.
Перелік і обсяг медичних послуг додаткового асортименту (наказ МОЗ України № 436) включає наступні підходи до лікування хворих із перикардитом:
- Симптоматичне лікування СН;
- Аміодарон призначають хворим з симптоматичними або тяжкими шлуночковими аритміями, а також при тахісистолічній формі фібриляції передсердь у випадку недостатньої ефективності інших препаратів;
- Антикоагулянти (непрямі) застосовують у пацієнтів з постійною формою фібриляції передсердь, тромбоемболічними ускладненнями в анамнезі, при наявності тромбів у порожнинах серця. Обов’язковий контроль показника МНО. При неможливості його визначення — визначення протромбінового індексу.
ЛІТЕРАТУРА
- Оганов Р.Г., Фомина И.Г. (ред.) (2006) Болезни сердца: руководство для врачей. Литтерра, Москва, 1328 с.
- Коваленко В.Н., Несукай Е.Г. (2001) Некоронарогенные болезни сердца. Практ. руководство. Морион, Киев, 480 с.
- Коваленко В.М., Лутай М.І., Сіренко Ю.М. (ред.) (2007) Серцево-судинні захворювання. Класифікація, стандарти діагностики та лікування кардіологічних хворих. Київ, 122 с.
- Коваленко В.Н. (ред.) (2008) Руководство по кардиологии. Морион, Киев, 1424 с.
- Наказ № 436 Міністерства охорони здоров’я України від 03.07.2006 р. «Про затвердження протоколів надання медичної допомоги за спеціальністю «Кардіологія» (2006). Укр. кардіол. журн., 6: 89–115.
- Шиллер Н., Осипов М.А. (2005) Клиническая эхокардиография. 2-е изд. Практика, Москва, 344 с.
- Bertog S.C., Thambidorai S.K., Parakh K. et al. (2004) Constrictive pericarditis: etiology and cause-specific survival after pericardiectomy. J. Amer. Coll. Cardiol., 43: 1445–1452.
- Bonnefoy E., Godon P., Kirkorian G. et al. (2000) Serum cardiac troponin I and ST-segment elevation in patients with acute pericarditis. Eur. Heart J., 21: 832–836.
- Brucato A., Cimaz R., Balla E. (2000) Prevention of recurrences of corticosteroid-dependent idiopathic pericarditis by colchicine in an adolescent patient. Pediatr. Cardiol., 21: 395–396.
- Frank H., Globits S. (1999) Magnetic resonance imaging evaluation of myocardial and pericardial disease. J. Magn. Reson. Imaging., 10: 617–626.
- Glockner J.F. (2003) Imaging of pericardial disease. Magn. Reson. Imaging Clin. North. Amer., 11: 149–162.
- Haley J.H., Tajik A.J., Danielson G.K. et al. (2004) Transient constrictive pericarditis: causes and natural history. J. Amer. Coll. Cardiol., 43: 271–275.
- Imazio M., Demichelis B., Cecchi E. et al. (2003) Cardiac troponin I in acute pericarditis. J. Amer. Coll. Cardiol., 42: 2144–2148.
- Imazio M., Bobbio M., Cecchi E. et al. (2005) Colchicine in addition to conventional therapy for acute pericarditis: results of the COlchicine for acute PEricarditis (COPE) trial. Circulation., 112: 2012–2016.
- Ling L.H., Oh J.K., Breen J.F. et al. (2000) Calcific constrictive pericarditis: is it still with us? Ann. Intern. Med., 132: 444–450.
- Maisch B., Seferovic P.M., Ristic A.D. et al. (2004) Guidelines on the diagnosis and management of pericardial disease. Eur. Heart J., 25: 587–610.
- Maron B.J., Towbin J.A., Thiene G. et al. (2006) Contemporary definitions and classification of the cardiomyopathies: An American Heart Association Scientific Statement from the Council on Clinical Cardiology, Heart Failure and Transplantation Committee; Quality of Care and Outcomes Research and Functional Genomics and Translational Biology Interdisciplinary Working Groups; and Council on Epidemiology and Prevention. Circulation., 113: 1807–1816.
- Myers R.B., Spodick D.H. (1999) Constrictive pericarditis: clinical and pathophysiologic characteristics. Amer. Heart J., 138(1): 219–232.
- Newby L.K., Ohman E.M. (2000) Troponins in pericarditis: implications for diagnosis and management of chest pains patients. Eur. Heart J., 21: 798–800.
- Notomi Y., Setser R.M., Shiota T. et al. (2005) Assessment of left ventricular torsional deformation by Doppler tissue imaging: validation study with tagged magnetic resonance imaging. Circulation., 111: 1141–1147.
- Oh J.K., Hatle L.K., Seward J.B. et al. (1994) Diagnostic role of Doppler echocardiography in constrictive pericarditis. J. Amer. Coll. Cardiol., 23: 154–162.
- Seferovic M., Spodick D.H., Maisch B. (Eds.) (2000) Pericardiology. Contempopary answers to continuing challenges. SCIENCE, Belgrade, 475 p.
- Sagrista-Sauleda J. et al. (1999) Long-term follow-up of idiopathic chronic pericardial effusion. N. Engl. J. Med., 341: 2054–2059.
- Sagrista-Sauleda J., Angel J., Sanchez A. et al. (2004) Effusive-constrictive pericarditis. N. Engl. J. Med., 350: 469–475.
- Salem K., Mulji A., Lonn E. (1999) Echocardiographically guided pericardiocentesis — the gold standard for the management of pericardial effusion and cardiac tamponade. Can. J. Cardiol., 15: 1251–1255.
- Seferovic P.M., Ristic A.D., Maksimovic R. et al. (2003) Diagnostic value of pericardial biopsy: improvement with extensive sampling enabled by pericardioscopy. Circulation., 107: 978–983.
- Tabata T., Kabbani S.S., Murray R.D. et al. (2000) Difference in the respiratory variation between mitral inflow and pulmonary venous flow Doppler velocities in patients with constrictive pericarditis. J. Amer. Soc. Echocardiogr., 13: 435–438.
- Topol E.J. (Ed.) (2007) Textbook of cardiovascular medicine. 3th ed. Lippincott Williams&Wilkins, 1628 p.
- Troughton R.W., Asher C.R., Klein A.L. (2004) Pericarditis. Lancet, 363: 717–727.
- Van der Merwe S., Dens J., Daenen W. et al. (2000) Pericardial disease is often not recognised as a cause of chronic severe ascites. J. Hepatol., 32: 164–169.
- Von Sohsten R., Kopistansky C., Cohen M. et al. (2000) Cardiac tamponade in the «new device» era: evaluation of 6999 consecutive percutaneous coronary interventions. Amer. Heart J., 140: 279–283.