Дацептон®/Набір Евер Фарма Ді-Майн Пен (Dacepton®/Ever Pharma D-Mine® Pen Set)
Дацептон /Набір Евер Фарма Ді-Майн Пен інструкція із застосування
Склад
Апоморфіну гідрохлорид - 10 мг/мл
Фармакологічні властивості
фармакодинаміка. Апоморфін є прямим стимулятором дофамінових рецепторів типів D1 та D2. Транспортні та метаболічні шляхи апоморфіну і леводопи різні.
Хоча в інтактних експериментальних тварин введення апоморфіну зменшує швидкість збудження клітин нігростріатної системи, а у низьких дозах апоморфін знижує рухову активність (вважають, що це є наслідком пресинаптичного інгібування вивільнення ендогенного дофаміну), його дія на розлади моторики при хворобі Паркінсона, ймовірно, опосередковується постсинаптичними рецепторами. Цей двофазний ефект виявляється також у людини.
Фармакокінетика. Фармакокінетика апоморфіну при п/ш введенні описується двокамерною моделлю, період напіврозподілу становить 5±1,1 хв, а T½ — 33±3,9 хв. Клінічний ефект залежить від концентрації апоморфіну у цереброспінальній рідині; розподіл діючої речовини найкраще описується двокамерною моделлю. Апоморфін швидко і повністю всмоктується з підшкірних тканин; клінічна дія препарату починається швидко (через 4–12 хв) і продовжується недовго (приблизно протягом 1 год), що пояснюється швидким кліренсом. Апоморфін метаболізується шляхом глюкуронізації і сульфування до щонайменше 10% від загальної дози; інші шляхи метаболізму не описані.
Показання Дацептон /Набір Евер Фарма Ді-Майн Пен
лікування моторних флуктуацій (феномен «включення-виключення») у пацієнтів із хворобою Паркінсона, стан яких недостатньо контролюється пероральними протипаркінсонічними препаратами.
Рекомендації по використанню
спосіб застосування та дози. Відбір пацієнтів, яким доцільно призначати препарат Дацептон, р-н для ін ‘єкцій 10 мг/мл у картриджах. Пацієнти, відібрані для лікування препаратом Дацептон, повинні мати можливість розпізнавати початок своїх симптомів «виключення» і бути в змозі самостійно зробити собі ін’єкцію або мати відповідального опікуна, який зможе зробити їм ін’єкцію при необхідності.
Пацієнти, яким призначено апоморфін, зазвичай повинні почати приймати домперидон щонайменше за 2 доби до початку терапії. Дозу домперидону слід титрувати до найнижчої ефективної дози і припинити застосування якомога швидше. Перед прийняттям рішення про початок лікування домперидоном і апоморфіном слід ретельно оцінити фактори ризику подовження інтервалу Q–T у кожного пацієнта, щоб переконатися, що користь переважує ризик (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
Лікування апоморфіном слід розпочинати під контролем в умовах спеціалізованої клініки. Пацієнт повинен перебувати під наглядом лікаря, який має досвід лікування хвороби Паркінсона (наприклад невропатолога). Перед початком лікування препаратом Дацептон слід оптимізувати лікування пацієнта леводопою, з агоністами дофаміну або без них.
Дорослі
Спосіб застосування. Препарат Дацептон, р-н для ін’єкцій у картриджах, призначений для мультидозового застосування шляхом періодичних п/ш болюсних ін’єкцій з використанням лише спеціально призначеного пристрою Ді-майн-Пен.
Пацієнтам і опікунам необхідно надати докладні інструкції щодо приготування та ін’єкційного введення препарату, приділяючи особливу увагу правильному застосуванню необхідного дозувального шприца-ручки (див. інструкцію для застосування, що докладається до дозувального шприца-ручки). Існують певні відмінності дозувального шприца-ручки цього препарату та інших препаратів апоморфіну, наявних на ринку. Тому коли пацієнт раніше отримав певний шприц-ручку і навчився його використовувати, перехід на застосування іншого препарату потребує нового навчання під наглядом медичного працівника.
Перед використанням слід видалити будь-які залишки повітря в картриджі (див. інструкцію для застосування дозувального шприца-ручки).
Апоморфін не можна вводити внутрішньовенно!
Не можна використовувати р-н, якщо він набув зеленого кольору. Перед введенням слід перевірити р-н візуально. Слід використовувати винятково прозорий, безбарвний або жовтуватого кольору р-н без механічних включень.
Визначення порогової дози. Відповідну дозу для кожного пацієнта слід підбирати з використанням графіків поступового підвищення дози. Рекомендується нижчезазначений графік: 1 мг апоморфіну гідрохлориду гемігідрату (0,1 мл препарату), що приблизно відповідає 15–20 мкг/кг маси тіла, вводити п/ш у період гіпокінезії або «виключення», після чого спостерігати за проявами рухової активності пацієнта протягом 30 хв.
Якщо відповіді не виявлено або вона була неадекватною, вводити п/ш другу дозу 2 мг апоморфіну гідрохлориду гемігідрату (0,2 мл препарату) і спостерігати за станом пацієнта ще протягом 30 хв, очікуючи адекватної відповіді.
Дози препарату можна поступово підвищувати з часовим інтервалом між наступними ін’єкціями щонайменше 40 хв до досягнення задовільної рухової відповіді.
Оптимізація схеми лікування. Після визначення відповідної дози виконується одна п/ш ін’єкція препарату в нижню частину поверхні живота або зовнішню поверхню стегна при перших симптомах епізоду «вимкнення». Не можна виключити того, що абсорбція апоморфіну в одного й того самого пацієнта може відрізнятися при введенні препарату в різні ділянки тіла. Тому пацієнт повинен перебувати під наглядом протягом 1 год після ін’єкції для оцінки задовільності відповіді на терапію. Враховуючи відповідь пацієнта, дозу препарату можна коригувати.
Оптимальна доза апоморфіну гідрохлориду гемігідрату може відрізнятися у різних пацієнтів, однак для окремого пацієнта вона залишається відносно постійною після того, як була визначена.
Запобіжні заходи при продовженні лікування. Добова доза препарату Дацептон варіює в широкому діапазоні у різних пацієнтів, зазвичай у діапазоні 3–30 мг при кількості ін’єкцій 1–10, а інколи і до 12 р/добу.
Рекомендується, щоб загальна добова доза апоморфіну гідрохлориду гемігідрату не перевищувала 100 мг, а індивідуальна болюсна доза була не вище 10 мг.
Пристрій Ді-майн Пен, необхідний для введення препарату Дацептон, р-н для ін’єкцій у картриджах, не підходить для пацієнтів, які потребують введення доз вище 6 мг болюсно.
Таким пацієнтам необхідно застосовувати інші препарати.
Під час клінічних досліджень зазвичай вдавалося знижувати дози леводопи деякою мірою, однак цей ефект суттєво варіює між різними пацієнтами і тому потребує ретельного контролю досвідченого лікаря.
Після оптимізації схеми лікування деяким пацієнтам можна поступово знижувати дозу домперидону, однак його повна відміна без симптомів блювання або артеріальної гіпотензії можлива лише у невеликої кількості пацієнтів.
Пацієнти літнього віку. Серед пацієнтів із хворобою Паркінсона багато осіб літнього віку. Вони становлять значну частку серед тих, хто був включений у клінічні дослідження апоморфіну. Схеми лікування апоморфіном пацієнтів літнього віку не відрізняються від схем для молодших пацієнтів. Однак на початку лікування пацієнтів літнього віку необхідна особлива обережність, враховуючи ризик розвитку ортостатичної гіпотензії.
Пацієнти з порушенням функції нирок. У пацієнтів з порушенням функції нирок можна дотримуватися схеми дозування, що є подібною до рекомендованої для дорослих пацієнтів і пацієнтів літнього віку (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
Опис шприца-ручки.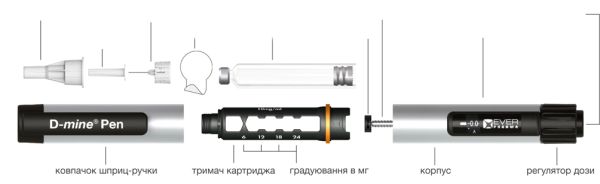
• Для запобігання контамінації необхідно використовувати нову голку для кожної ін’єкції.
• Голки та шприц-ручку не можна надавати для застосування іншим особам.
• Перед застосуванням препарату Дацептон необхідно вивчити посібник з використання та зрозуміти принципи роботи шприца-ручки, щоб ознайомитися з вимогами до відповідного поводження з пристроєм.
• Якщо шприц-ручка пошкоджена або не працює належним чином (через механічні дефекти), звернутися до інструкції для застосування шприца-ручки.
Де і як проводити ін’єкцію препарату Дацептон?
• Спочатку потрібно помити руки.
• Перед використанням шприца-ручки необхідно підготувати хірургічні серветки та одну голку в захисному футлярі конічної форми.
• Необхідно дотримуватися інструкцій, наведених у посібнику з використання шприца-ручки.
Підготовка шприца-ручки/заміна картриджа.
Вийняти шприц-ручку з футляра і зняти ковпачок шприца-ручки.
Зняти муфту картриджа, повернувши її за годинниковою стрілкою.
Вставити новий картридж у муфту картриджа.
Повністю заштовхнути назад нарізний стрижень. Це найзручніше виконувати за допомогою кінчика пальця.
Заштовхнути муфту картриджа в корпус і повернути проти годинникової стрілки до фіксації.
Під’єднання голки до шприца-ручки.
Дотримуватися інструкції для застосування голок, призначених для даного шприца-ручки.
Потягнути та зняти відривну фольгу.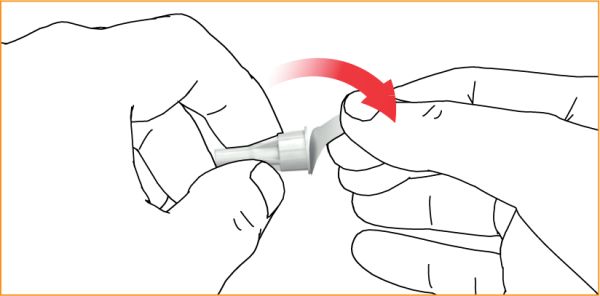
Під’єднати голку, призначену для шприца-ручки, до муфти картриджа шляхом натискання до клацання/накручування.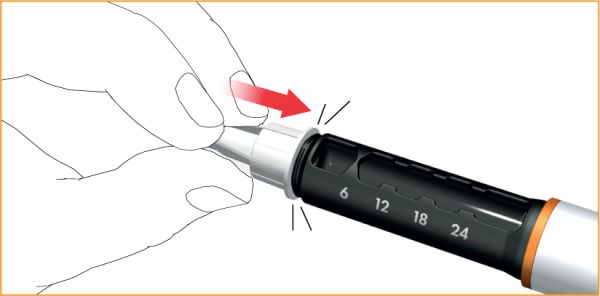
Зняти зовнішній захисний ковпачок голки. Зберігати зовнішній захисний ковпачок голки для безпечного зняття та утилізації голки, призначеної для шприца-ручки, після використання.
Зняти й утилізувати внутрішній захисний ковпачок голки.
Первинне заповнення/перевірка функції. Перед використанням слід видалити будь-який залишок повітря в картриджі. Установити пробну дозу шляхом повороту дозувального барабана. Перевірити встановлену дозу, поглянувши на дисплей вертикально згори, але не під кутом, щоб на дисплеї був чітко відображений символ «». Це називається «первинним заповненням» і є важливим моментом, тому що це гарантує отримання повної дози при використанні шприца-ручки.
Для перевірки функції тримати шприц-ручку спрямованим догори та обережно постукати муфту картриджа, щоб бульбашки повітря могли піднятися догори.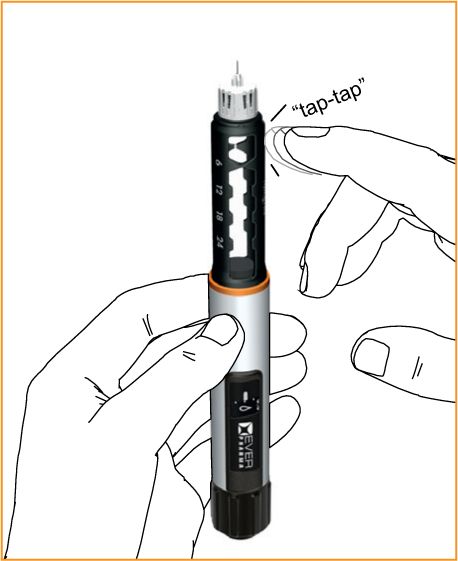
Натиснути кнопку.
З кінчика голки, призначеної для шприца-картриджа, вийде кілька крапель лікарського засобу. Якщо краплі не з’являться, повторити крок.
Встановлення дози. Встановити потрібну дозу шляхом повороту дозувального барабана за годинниковою стрілкою. Коригувати дозу шляхом повороту проти годинникової стрілки.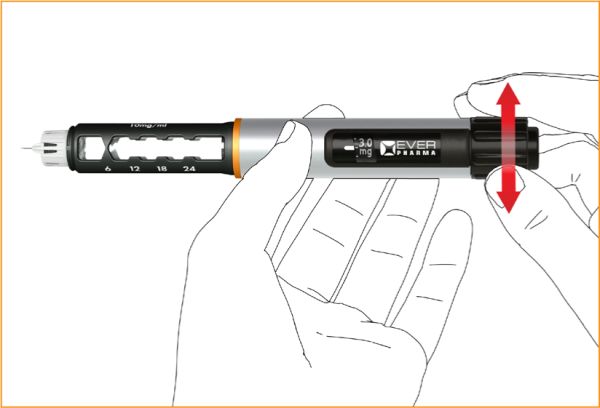
Ін’єкція
• Використовуючи хірургічну серветку, очистити ділянку шкіри, де планується ін’єкція лікарського засобу, а також навколо цієї ділянки.
• Препарат Дацептон необхідно вводити п/ш в ділянку передньої поверхні талії (живота) або зовнішньої поверхні стегон.
• Використовувати техніку ін’єкції, рекомендовану лікарем та/або медичним працівником.
Повністю натиснути кнопку для виконання ін’єкції. Під час введення лікарського засобу тримати кнопку повністю натиснутою. Після повного введення лікарського засобу зачекати 6 с, а потім повільно витягнути голку. Можна або утримувати кнопку натиснутою, або відпустити її впродовж цих 6 сек. Переконатися, що дисплей знаходиться в положенні «0,0», що підтверджує введення повної дози.
• Місце ін’єкції необхідно змінювати кожного разу, коли застосовується препарат Дацептон. Це знизить ризик виникнення шкірної реакції у місці ін’єкції препарату Дацептон. Препарат Дацептон не можна вводити у ділянку шкіри, яка є болісною, червоною, інфікованою або пошкодженою.
• Ніколи не можна робити ін’єкцію цим шприцом-ручкою безпосередньо у вену (в/в) або у м’яз (в/м).
Видалення голки після кожної ін’єкції. Після кожної ін’єкції голку необхідно видалити та утилізувати.
Обережно під’єднати зовнішній захисний ковпачок голки до самої голки.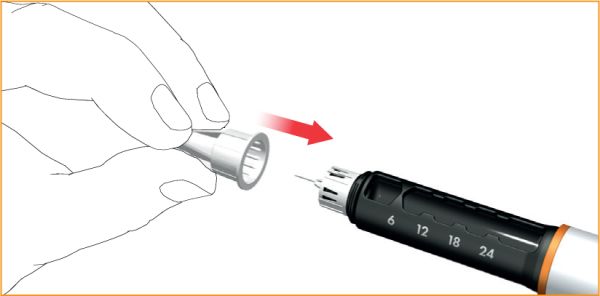
Відкрутити голку від шприца-ручки, повертаючи зовнішній ковпачок за годинниковою стрілкою, й утилізувати належним чином.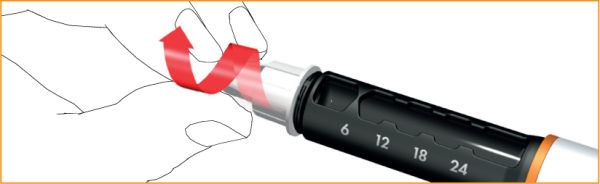
Додатковий варіант. Розмістити зовнішній ковпачок голки у відповідне ліве заглиблення футляра для зберігання. Отвір ковпачка голки має бути спрямований догори. Обережно вставити голку (під’єднану до шприца-ручки) в отвір ковпачка. Не тримаючись за ковпачок, щільно натиснути донизу і повернути проти годинникової стрілки, щоб відкрутити голку.
Після кожного використання щільно закрити шприц-ручку його ковпачком.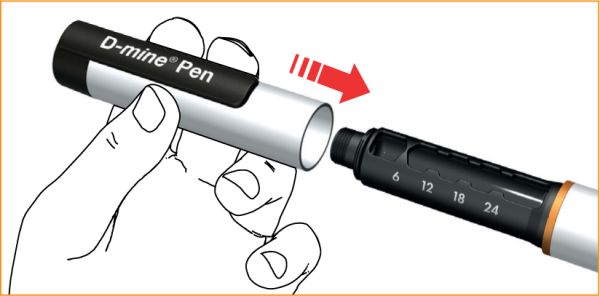
• Картридж залишається у шприці-ручці.
• Новий картридж можна використовувати до 15 днів (докладну інформацію див. УМОВИ ЗБЕРІГАННЯ).
• Якщо не залишилося достатньої кількості р-ну для наступної дози, картридж необхідно видалити та утилізувати.
• Необхідно утилізувати голку безпечним чином, як описано в інструкції для застосування шприца-ручки.
З мікробіологічної точки зору, за винятком випадків, коли спосіб відкриття та подальшого поводження виключає ризик мікробного забруднення, препарат слід використовувати негайно. Якщо він не використовується негайно, за час та умови зберігання після відкриття відповідає користувач.
Особливі заходи безпеки. Не можна використовувати р-н, якщо він набув зеленого кольору.
Перед введенням слід перевірити р-н візуально. Слід використовувати винятково прозорий, безбарвний або жовтуватого кольору р-н без механічних включень, що міститься у непошкоджених контейнерах.
Будь-який невикористаний лікарський засіб або відходи повинні бути утилізовані відповідно до місцевих вимог.
Слід утилізувати всі картриджі, що містять невикористаний лікарський засіб, не пізніше ніж через 15 днів після першого відкриття.
Пацієнту слід надати інструкції з безпечної утилізації голки після кожної ін’єкції.
Упаковка не містить ні шприца-ручки, ні голок для шприца-ручки.
Картриджі препарату Дацептон призначені для використання лише зі спеціально призначеним пристроєм Ді-майн Пен і одноразовими голками для шприца-ручки, як зазначено в інструкції для застосування шприца-ручки.
Придбати шприц-ручку Ді-майн Пен і одноразові голки для шприца-ручки можна в аптеці.
Протипоказання
• підвищена чутливість до діючої речовини або будь-якої з допоміжних речовин.
• Пригнічення функції дихання, деменція, психотичні захворювання або печінкова недостатність.
• Апоморфіну гідрохлорид гемігідрат не можна застосовувати у пацієнтів, які мають відповідь «включення» на леводопу з тяжкою дискінезією або дистонією.
• Одночасне застосування з ондансетроном (див. ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
• Препарат Дацептон, р-н для ін’єкцій 10 мг/мл, протипоказаний дітям та підліткам віком до 18 років.
Побічна дія
залежно від частоти побічні реакції розподілені на такі категорії: дуже часто (>1/10), часто (>1/100, <1/10), нечасто (>1/1000, <1/100), рідко (>1/10 000, <1/1000), дуже рідко (<1/10 000), частота невідома (не може бути оцінена за наявними даними).
З боку крові та лімфатичної системи: нечасто — повідомляли про розвиток гемолітичної анемії і тромбоцитопенії у пацієнтів, які отримували апоморфін; рідко — еозинофілія рідко відмічалася під час лікування апоморфіну гідрохлоридом гемігідратом.
З боку імунної системи: рідко — оскільки препарат містить натрію метабісульфіт, можливі алергічні реакції (зокрема анафілаксія і бронхоспазм).
Психічні розлади: дуже часто — галюцинації; часто — нейропсихічні розлади (зокрема легка транзиторна сплутаність свідомості та зорові галюцинації) відмічали під час лікування апоморфіну гідрохлоридом гемігідратом; частота невідома — розлади контролю імпульсивної поведінки (патологічна пристрасть до азартних ігор, підвищене лібідо, гіперсексуальність, непереборний потяг до покупок або витрачання грошей, булімія та компульсивне переїдання) можуть спостерігатися у пацієнтів під час лікування агоністами дофаміну, включаючи апоморфін; агресія, тривожне збудження.
З боку нервової системи: часто — транзиторний седативний ефект при введенні кожної дози апоморфіну гідрохлориду гемігідрату може спостерігатися на початку лікування; зазвичай цей ефект минає через кілька тижнів після початку лікування; застосування апоморфіну супроводжується сонливістю; також повідомляли про випадки запаморочення; нечасто — апоморфін може індукувати дискінезії під час періоду «включення», які в деяких випадках можуть бути тяжкими і призвести до відміни терапії у певної кількості пацієнтів; застосування апоморфіну супроводжувалося епізодами раптового засинання; частота невідома — непритомність, головний біль.
З боку судин: нечасто — ортостатична гіпотензія, яка зазвичай є транзиторною.
Респіраторні, торакальні та медіастинальні розлади: часто — позіхання під час лікування апоморфіном, нечасто — утруднене дихання.
З боку ШКТ: часто — нудота і блювання, особливо у початковий період лікування апоморфіном, зазвичай за відсутності застосування домперидону.
З боку шкіри та підшкірної клітковини: нечасто — повідомлялося про локальний та генералізований висип.
Системні розлади та ускладнення у місці введення: дуже часто — у більшості пацієнтів відмічають реакції у місці ін’єкції, особливо при безперервному застосуванні, зокрема підшкірні вузлики, ущільнення, еритема, болючість і панікуліт; можливі інші місцеві реакції (зокрема подразнення, свербіж, синці та біль); нечасто — некроз і виразки у місці ін’єкції; частота невідома — периферичний набряк.
Результати лабораторних досліджень: нечасто — позитивні проби Кумбса при лікуванні пацієнтів апоморфіном.
Особливості застосування
апоморфіну гідрохлорид гемігідрат слід з обережністю застосовувати у пацієнтів з нирковими, легеневими або серцево-судинними захворюваннями, а також пацієнтів, схильним до нудоти і блювання.
Особлива обережність необхідна у початковий період лікування пацієнтів літнього віку та/або ослаблених хворих.
Оскільки апоморфін може спричинити артеріальну гіпотензію навіть у разі премедикації домперидоном, особливу увагу слід приділяти пацієнтам із серцевими захворюваннями, хворим, які приймають вазоактивні лікарські засоби, зокрема гіпотензивні препарати, особливо пацієнтам з ортостатичною гіпотензією в анамнезі.
Оскільки апоморфін, особливо у високих дозах, може спричиняти подовження інтервалу Q–T, необхідна обережність при лікуванні пацієнтів з ризиком порушень серцевого ритму типу пірует (torsades de pointes).
При застосуванні в комбінації з домперидоном слід ретельно оцінити фактори ризику в окремого пацієнта. Це необхідно робити до початку і під час лікування. Важливі фактори ризику включають серйозні фонові серцеві захворювання, такі як застійна серцева недостатність, тяжке порушення функції печінки або значний електролітний дисбаланс. Також необхідно оцінити лікарські засоби, які можуть впливати на електролітний баланс, метаболізм CYP 3A4 або інтервал Q–T. Рекомендується проводити моніторинг впливу на інтервал Q–Tc. Необхідно зробити ЕКГ:
— до лікування домперидоном;
— під час фази початку лікування;
— надалі за клінічними показаннями.
Пацієнту слід вказати на необхідність повідомляти про можливі серцеві симптоми, включаючи серцебиття, непритомність або стани, що наближаються до непритомності. Пацієнти також повинні повідомляти про клінічні зміни, які можуть призвести до гіпокаліємії, такі як гастроентерит або початок лікування сечогінними препаратами.
Під час кожного медичного візиту слід переглядати фактори ризику.
Лікування апоморфіном може спричиняти місцеві підшкірні ефекти. Інколи їх вдається зменшити шляхом чергування місць ін’єкцій. У разі наявності можна використовувати ультразвукове дослідження для уникнення ін’єкцій у ділянки з вузликами та ущільненнями.
Повідомляли про розвиток гемолітичної анемії і тромбоцитопенії у пацієнтів, які отримували апоморфін. Гематологічні показники слід контролювати через певні проміжки часу, як і для леводопи, при одночасному застосуванні з апоморфіном.
Необхідна обережність при застосуванні апоморфіну у комбінації з іншими лікарськими засобами, особливо з вузьким терапевтичним діапазоном (див. ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
У багатьох пацієнтів з прогресуючою хворобою Паркінсона відзначаються нейропсихічні порушення. Є свідчення того, що апоморфін може посилювати нейропсихічні порушення у деяких пацієнтів. У випадках застосування апоморфіну таким пацієнтам необхідна особлива обережність.
Апоморфін може спричиняти сонливість та епізоди раптового засинання, зокрема у пацієнтів з хворобою Паркінсона. Про це слід попередити пацієнтів і порадити їм дотримуватися обережності при керуванні транспортними засобами або роботі з іншими механізмами під час лікування апоморфіном. Пацієнти, у яких спостерігаються сонливість та/або епізоди раптового засинання, повинні утримуватися від керування транспортними засобами або роботи з іншими механізмами. Крім того, в таких випадках можна розглянути доцільність зниження дози або припинення терапії.
Пацієнти потребують систематичного моніторингу щодо розвитку розладів контролю імпульсивної поведінки. Пацієнти та їх опікуни повинні знати, що при лікуванні агоністами дофаміну, зокрема апоморфіном, можуть відзначатися такі симптоми розладів контролю імпульсивної поведінки, як патологічна пристрасть до азартних ігор, підвищене лібідо, гіперсексуальність, непереборний потяг до покупок або витрачання грошей, булімія та компульсивне переїдання. У разі появи таких симптомів слід розглянути доцільність зниження дози або поступової відміни препарату.
Синдром дофамінової дисрегуляції є адиктивним розладом, що призводить до надмірного застосування препарату, це відмічається у деяких пацієнтів, які отримували апоморфін. Перед початком лікування пацієнтів та опікунів слід попередити про потенційний ризик розвитку синдрому дофамінової дисрегуляції.
Допоміжні речовини з відомою дією. Препарат Дацептон, р-н для ін’єкцій 10 мг/мл у картриджах, містить 1 мг натрію метабісульфіту (Е223) на 1 мл, що може рідко спричиняти тяжкі реакції гіперчутливості та бронхоспазм.
Препарат містить менше 1 ммоль (23 мг) натрію у 10 мл, тобто практично не містить натрію.
Застосування у період вагітності або годування грудьми. Досвід застосування апоморфіну у вагітних відсутній.
У дослідженнях репродуктивної функції у тварин жодні тератогенні ефекти не виявлені, але введення токсичних доз вагітним самицям щурів може спричиняти дихальну недостатність у потомства. Потенційний ризик для людини невідомий.
Препарат Дацептон не слід застосовувати у період вагітності, за винятком випадків очевидної необхідності такого застосування.
Інформація про екскрецію апоморфіну у грудне молоко людини відсутня. Рішення щодо припинення/продовження годування грудьми або припинення/продовження лікування препаратом Дацептон слід приймати з урахуванням потреби у грудному вигодовуванні дитини та очікуваної користі від лікування препаратом Дацептон для жінки.
Здатність впливати на швидкість реакції при керуванні транспортними засобами або іншими механізмами. Апоморфіну гідрохлорид гемігідрат чинить незначний або помірний вплив на здатність керувати транспортними засобами або іншими механізмами.
Пацієнти, які лікуються апоморфіном та у яких відмічають сонливість та/або епізоди раптового засинання, повинні утримуватися від керування транспортними засобами або інших видів діяльності (наприклад роботи з механізмами), при яких порушення пильності може наражати їх самих або оточуючих на небезпеку серйозного травмування або летального наслідку, поки рецидиви таких епізодів і сонливість не минуть (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
Взаємодія з іншими лікарськими засобами
пацієнти, відібрані для лікування апоморфіну гідрохлоридом гемігідратом, майже напевно приймають одночасно інші лікарські засоби для лікування хвороби Паркінсона. Тому на початковій стадії лікування апоморфіну гідрохлоридом гемігідратом необхідно пильно стежити за можливими незвичними побічними реакціями або ознаками потенціювання дії лікарських препаратів.
При одночасному застосуванні з нейролептиками може виникати антагоністична взаємодія. Існує можливість взаємодії між клозапіном та апоморфіном, однак клозапін також можна застосовувати з метою зменшення вираженості симптомів нейропсихічних ускладнень. Можливий вплив апоморфіну на концентрацію у плазмі крові інших лікарських засобів не вивчали. Тому необхідна обережність при застосуванні апоморфіну у комбінації з іншими лікарськими засобами, особливо з вузьким терапевтичним діапазоном.
Антигіпертензивні та кардіоактивні препарати. Навіть у разі одночасного застосування з домперидоном апоморфін може потенціювати антигіпертензивний ефект таких препаратів (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ). Рекомендується уникати одночасного застосування апоморфіну та інших препаратів, які подовжують інтервал Q–T.
Враховуючи повідомлення про випадки глибокої гіпотензії та втрати свідомості при застосуванні апоморфіну разом з ондансетроном, одночасне застосування апоморфіну та ондансетрону протипоказане.
Несумісність. Через відсутність досліджень сумісності цей препарат не слід змішувати з іншими лікарськими засобами.
Передозування
існує невелика кількість клінічних відомостей щодо передозування апоморфіну при п/ш введенні. Лікування симптомів передозування може проводитися емпірично, як запропоновано нижче:
при надмірному блюванні можна застосовувати домперидон;
при пригніченні функції дихання можна застосовувати налоксон;
при артеріальній гіпотензії — відповідні заходи (наприклад підвищення частини ліжка, де розташовані ноги);
при брадикардії можна застосовувати атропін.
Умови зберігання
в оригінальній упаковці у недоступному для дітей місці при температурі не вище 25 °С. Не охолоджувати і не заморожувати.
