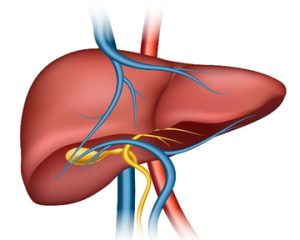
 Гемангіоми — доброякісні судинні пухлини, які можуть уражувати шкіру або внутрішні органи, у тому числі печінку. Пацієнти з гемангіомами печінки (ГП) можуть бути клінічно безсимптомними, і лише при ультразвуковому дослідженні лікар може діагностувати ГП.
Гемангіоми — доброякісні судинні пухлини, які можуть уражувати шкіру або внутрішні органи, у тому числі печінку. Пацієнти з гемангіомами печінки (ГП) можуть бути клінічно безсимптомними, і лише при ультразвуковому дослідженні лікар може діагностувати ГП.
Класифікація
У дорослих ГП класифікуються на:
- кавернозну;
- капілярну;
- склерозуючу (характеризується дегенерацією та фіброзним заміщенням і може бути неправильно діагностована як злоякісна пухлина) (Leon M. et al., 2020).
ГП можуть бути обмежені однією часткою (більше у правій частці печінки) або поширюватися на всю печінку. Залежно від розміру ГП може бути маленькою або гігантською (>5 см) і може варіювати в межах 1–50 см.
У дітей розрізняють:
- інфантильну ГП (ІГП) — може бути осередковою, багатоосередковою (мультифокальною) або дифузною;
- вроджену ГП (ВГП).
ВГП за характером інволюції класифікується на:
- ГП зі швидкою, частковою інволюцією;
- без інволюції.
ІГП та ВГП відрізняються за різним клінічним перебігом. ІГП швидко росте у дитини після народження, потім повільно інволютує; тоді як ВГ повністю формується при народженні дитини, а потім у ранньому дитинстві інволюціонує.
Причини
Згідно з однією гіпотезою, ГП виникає в результаті аномального ангіогенезу та збільшення проангіогенних факторів — фактор росту ендотелію судин (VEGF) є важливим проангіогенним фактором для ендотеліальних клітин.
Крім того, в рості ГП відіграють важливу роль естрогени, оскільки вони частіше діагностуються у жінок та їх розмір збільшується після замісної гормональної терапії, прийому оральних контрацептивів та вагітності. Прямі механізми дії гормонів невідомі, оскільки ГП не взаємодіє з рецепторами естрогену та прогестерону (Leon M. et al., 2020).
ІГП та ВГП є судинними пухлинами дитячого віку, але відрізняються за своєю основною причиною та клінічним перебігом. Основний патогенез у обох випадках вивчений лише частково. У разі ІГП передбачається, що ураження формуються як продукт порушення регуляції васкулогенезу та ангіогенезу. Пусковим сигналом є гіпоксичний стрес, який спричиняє гіперекспресію VEG-F та інших ангіогенних факторів, що призводить до аномальної проліферації ендотеліальних клітин плода.
У разі ВГП до їх патогенезу залучені соматичні активуючі мутації. Нещодавні дослідження продемонстрували мутації в алелях GNAQ та GNA11 при ВГП. Згідно з дослідженнями, ВГП з частковою інволюцією та ВГП без інволюції мають подібні мутації в результаті постнатальних факторів або епігенетики (Lewis D. et al., 2022).
Патофізіологія
ГП є пухлиною мезодермального походження, що складається із заповненого кров’ю простору. Це найбільш поширена доброякісна пухлина печінки, що є чітко окресленим гіперваскулярним ураженням, яке частіше діагностується у жінок (Leon M. et al., 2020).
Три різних типи ураження ІГП:
- вогнищева ІГП являє собою одиночне ураження печінки, яке зазвичай має безсимптомний перебіг і рідко пов’язане зі шкірною інфантильною гемангіомою (ІГ);
- багатоосередкова (мультифокальна) ІГП складається з декількох окремих уражень печінки, які в літературі по-різному визначаються як мінімум 5 уражень або до 10 уражень. Ураження часто мають безсимптомний перебіг, хоча частіше призводять до розвитку серцевої недостатності з високим викидом через артеріовенозне або портовенозне шунтування;
- дифузна ІГП (дифузний неонатальний гемангіоматоз) — характеризується значним ураженням печінки. Масивна гепатомегалія може призвести до стискування прилеглих локальних структур (грудної порожнини, нижньої порожнини та черевної порожнини). Це може призвести до абдомінального компартмент-синдрому, дихальної недостатності та полісистемної недостатності органів. Дифузний ІГП може також надмірно продукувати йодтиронін-дейодиназу III типу, яка деактивує тироксин, що призводить до гіпотиреозу. Це може зумовити значну затримку розвитку та серцеву недостатність через погану скоротливість.
ВГП може мати безсимптомний перебіг або бути виявленим при рутинному скринінгу. За наявності симптомів ВГП може викликати транзиторну тромбоцитопенію та коагулопатію, яка відрізняється від феномену Казабаха — Мерріта, небезпечного для життя процесу, пов’язаного виключно з капозіформною гемангіоендотеліомою та пучковою ангіомою. Інші рідкісні ускладнення включають дисеміноване внутрішньосудинне згортання, печінкову недостатність через зміщення паренхіми печінки та серцеву недостатність з високим викидом через артеріовенозне та портовенозне шунтування (Lewis D. et al., 2022).
Симптоми
 Як ІГП, так і ВГП можуть бути клінічно безсимптомними і виявлені тільки при ультразвуковому дослідженні, при звичайному пренатальному ультразвуковому дослідженні. Якщо ГП збільшується у розмірі, то при фізичному огляді можна виявити гепатомегалію (Lewis D. et al., 2022).
Як ІГП, так і ВГП можуть бути клінічно безсимптомними і виявлені тільки при ультразвуковому дослідженні, при звичайному пренатальному ультразвуковому дослідженні. Якщо ГП збільшується у розмірі, то при фізичному огляді можна виявити гепатомегалію (Lewis D. et al., 2022).
Найпоширеніші симптоми при гемангіомі печінки:
- біль у правому верхньому квадранті живота;
- здуття живота;
- відсутність апетиту;
- нудота.
Клінічні прояви можливі при серцевій недостатності з високим викидом, гіпотиреозі або компресії нижньої порожнистої вени, прилеглих органів у грудній, а також черевній порожнині. У разі ВГП легка транзиторна коагулопатія може спричинити петехіальний висип.
При виявленні 5 та більше шкірних ІГП рекомендується проведення ультразвукового дослідження (УЗД) печінки.
ГП зазвичай має безсимптомний перебіг, проте симптоми можуть виявлятися, коли ГП більше 5 см. Симптоми неспецифічні, пацієнти зазвичай скаржаться на біль у животі, дискомфорт та відчуття переповнення у правому підребер’ї.
Пухлини >10 см супроводжуються здуттям живота, нудотою, раннім насиченням та постпрандіальним здуттям живота. Іноді у пацієнта можливі супутні симптоми — лихоманка, жовтяниця, задишка, серцева недостатність із високим викидом та гемомобілія.
Гігантська ГП може викликати небезпечне для життя порушення згортання крові, відоме як синдром Казабаха — Мерріта (тромбоцитопенія, дисеміноване внутрішньосудинне згортання крові та системна кровотеча), що виявляється коагулопатією, вторинною по відношенню до тромбоцитопенії, анемією, гіпофібриногенімією, зменшенням протромбінового часу та підвищенням D-димера. Цей синдром відзначають із частотою від 0,3% усіх випадків ГП до 26% при ГП >15 см (Leon M. et al., 2020).
Діагностика
УЗД, комп’ютерна томографія (КТ) та магнітно-резонансна томографія (МРТ) є найбільш поширеними візуалізуючими тестами. Атипові ураження можуть потребувати більше однієї візуалізації. Унікальними особливостями ГП при візуалізації є наявність периферичного вузлового посилення та прогресуючого доцентрового заповнення.
УЗД дорослих
На УЗД ГП виглядає як чітко окреслена однорідна гіперехогенна маса із заднім акустичним посиленням. Кольорове допплерівське УЗД не підвищує точності діагностики, оскільки показує кровообіг тільки при ГП із внутрішньоартеріопортальним шунтом.
Деякі злоякісні ураження печінки (гепатоцелюлярна карцинома та метастази в печінку) можуть давати подібні акустичні патерни, і для підтвердження діагнозу необхідно використовувати інші методи візуалізації.
Для діагностики ГП також ефективно УЗД з контрастним посиленням (CEUS). Контраст з мікропухирцями допомагає медичному персоналу бачити потік крові через органи та кровоносні судини. Мікропухирці у контрасті існують лише короткий час. Коли бульбашки лопаються, нешкідливий газ розчиняється у крові пацієнта та виходить із диханням. При CEUS, ГП можна діагностувати за посиленням контрасту периферичних вузлів у ранній фазі (артеріальній) з доцентровим наповненням у пізніших фазах.
КТ та МРТ
На КТ ГП описуються як чітко окреслені гіподенсивні маси. При введенні внутрішньовенно контрасту — периферичне вузлове посилення з доцентровим однорідним наповненням, проте ГП з кістозними ділянками, фіброзом або тромбозом характеризується атиповою картиною.
На МРТ лікар може діагностувати чітко окреслене, гладке, гомогенне ураження на зображеннях (гіпоінтенсивне або гіперінтенсивне). Введення контрастної речовини (гадолінія) показує периферичне посилення в артеріальну фазу та затримку контрасту у відстрочену фазу, що дозволяє диференціювати гіперваскулярні пухлини печінки, для яких зазвичай характерне вимивання контрасту у відстрочену фазу.
Ангіографія
Для атипових ГП, які важко діагностувати за допомогою інших методів візуалізації, рекомендована ангіографія. ГП виглядає як «снігове дерево» або «вата» з великою судиною живлення і дифузним скупченням контрасту, яке триває під час відстроченої фази.
Інші методи візуалізації
Інші методи візуалізації, доступні для діагностики ГП у пацієнтів з атиповими пухлинами, хронічними захворюваннями печінки або злоякісними новоутвореннями:
- сцинтиграфія пулу еритроцитів, мічених технецієм-99m пертехнетатом;
- однофотонна емісійна КТ;
- позитронно-емісійна томографія/КТ (Leon M. et al., 2020).
Пункційна аспіраційна біопсія
 Пункційна аспіраційна біопсія не рекомендується через високий ризик кровотечі та низьку діагностичну цінність.
Пункційна аспіраційна біопсія не рекомендується через високий ризик кровотечі та низьку діагностичну цінність.
Діти
Остаточний діагноз ІГП та ВГП може бути встановлений за допомогою біопсії та подальшого гістопатологічного дослідження печінки. Однак це може призвести до ризику кровотечі, оскільки ураження сильно васкуляризовані.
Тому для встановлення діагнозу лікар може спостерігати за клінічним перебігом, рентгенологічними даними пацієнта та виключати злоякісні процеси при лабораторних дослідженнях.
ІГП та ВГП слід контролювати за допомогою декількох УЗД. Ураження, яке швидко збільшується від народження приблизно до 8-місячного віку, а потім починає регресувати, відповідає ІГП, тоді як ураження, яке повністю сформувалося при народженні та повільно регресує, відповідає ВГП.
Відмінні характеристики ІГП та ВГП при візуалізації
У разі ВГП ураження печінки може виглядати неоднорідним на УЗД, КТ або МРТ з периферичним обідком контрастного посилення та мінімальним центральним посиленням. ІГП може мати схожі риси. Можливою відмінністю між ними можуть бути кальцифікації, які часто лікар діагностує при ВГП, але відсутні при ІГП.
При зниженні рівня ангіотензинперетворювального ферменту (АПФ) у плазмі крові та негативних показниках катехоламінів у сечі — можливе виключення діагнозу гепатобластоми або нейробластоми (Lewis D. et al., 2022).
Лікування
Дорослі
При невеликих безсимптомних ГП лікар не призначає лікування. Рекомендовано наступне спостереження при ГП >5 см через 6–12 міс для оцінки швидкого росту за допомогою того ж візуалізаційного тесту, який використовувався при встановленні діагнозу.
Лікування проводиться пацієнтам із симптомами, з безперервним масовим ростом, компресією сусідніх органів (непрохідність вихідного отвору шлунка, синдром Бадда — Кіарі) або такими ускладненнями, як розрив ГП із внутрішньочеревною кровотечею або синдромом Казабаха — Мерріта.
Хірургічне лікування
Хірургічне втручання включає резекцію печінки, енуклеацію, перев’язку печінкової артерії та трансплантацію печінки. У всьому світі найбільш поширеними процедурами є резекція печінки та енуклеація (за допомогою відкритої хірургії, лапароскопії або роботизованої хірургії).
Вибір хірургічної техніки залежить від розміру, кількості уражень, локалізації, досвіду хірурга та ресурсів установи. Обидва методи зумовлюють мінімальну післяопераційну захворюваність.
Енуклеація пов’язана з нижчою захворюваністю, коротшим часом операції, меншою крововтратою і меншою кількістю ускладнень. Однак коли ГП більше 10 см, немає значної різниці між енуклеацією та резекцією печінки.
Енуклеація технічно простіша при периферичній ГП, при центральній ГП процедура викликає більш тривалий час оклюзії судинного припливу, триваліший час операції та велику крововтрату. Центрально розташовані ГП (сегменти I, IV, V та VIII) лікують розширеною правобічною та лівобічною гепатектомією. За допомогою цього втручання можна видалити 60–80% паренхіми печінки, що підвищує ризик післяопераційної печінкової недостатності. Деякі ураження підходять для клиноподібної резекції.
Лапароскопічна хірургія печінки краща при невеликих лівобічних ураженнях з невеликими резекціями.
Трансплантація печінки при доброякісних солідних пухлинах не вважається терапією першої лінії через захворюваність та нестачу органів. Трансплантація печінки рекомендована для нерезектабельних гігантських ГП, що спричиняють тяжкі симптоми (респіраторний дистрес, біль у животі), неефективність попередніх втручань або небезпечні для життя ускладнення, такі як синдром Казабаха — Мерріта.
Нехірургічне лікування
Транскатетерна артеріальна емболізація (ТАЕ) використовується для зупинки гострої кровотечі або зменшення ГП перед операцією за допомогою металевих спіралей, частинок гелеподібної форми, полівінілового спирту та рідких агентів.
Згідно з результатами дослідження, у 73,9% пацієнтів, яким проводили ТАЕ з блеоміцином, відзначено >50% регресію ГП за об’ємом. Введення блеоміцину призводить до утворення мікротромбів, що зумовлює атрофію та фіброз пухлини, але зафіксовані такі ускладнення: гостра печінкова недостатність, інфаркт печінки, абсцес, внутрішньопечінкова білома, холецистит, інфаркт селезінки, перфорація печінкової артерії і склерозуючий холангіт.
Радіочастотна абляція (РЧА) може застосовуватися черезшкірно, лапароскопічно або шляхом відкритої операції:
- РЧА зумовлює термічне пошкодження ендотеліальних судинних структур та викликає тромбоз;
- РЧА зазвичай виконується під КТ-контролем;
- черезшкірну РЧА використовують для ГП, розташованих глибоко в паренхімі печінки;
- лапароскопічна РЧА під контролем УЗД переважно при субкапсулярній ГП; показання до РЧА — максимальний діаметр ГП >5 см, ріст пухлини >1 см протягом 2 років, персистуючий біль у животі, пов’язаний з ГП, за винятком інших захворювань ШКТ;
- протипоказання — тенденція до кровотечі, пацієнти зі злоякісними пухлинами, синдромом Казабаха — Мерріта, інфекцією (запалення жовчовивідних шляхів), тяжкою органною недостатністю.
При тривалій РЧА можливі гемоліз, гемоглобінурія та гостра ниркова недостатність, тому не підходить для великих ГП. Інші ускладнення РЧА: кровотеча у місці введення електрода, розрив ГП та пошкодження сусідніх органів внаслідок проколу або термічної травми (Leon M. et al., 2020).
Діти
Лікування ІГП та ВГП є підтримувальним і спрямоване на усунення потенційних ускладнень, оскільки обидва ураження зазвичай минають без втручання. Лікування показане під час ускладнень.
Для лікування ІГП ефективний пропранолол. Точний механізм не з’ясований, але передбачається, що він регулює шлях VEGF, який бере участь в розвитку ураження.
Хірургічна резекція та емболізація ІГП показані при ускладненнях, включаючи серцеву недостатність з високим викидом, абдомінальний компартмент-синдром і дихальну недостатність. Важливо враховувати ускладнення хірургічної резекції — кровотечу, а емболізації ІГП — некроз печінки, цироз та сепсис. Немовлятам із дифузною формою ІГП із гіпотиреозом буде потрібна замісна терапія гормонами щитовидної залози.
Хірургічна резекція або емболізація рідко можуть бути показані в умовах активної кровотечі або тяжкої серцевої недостатності.
ІГП швидко росте в ранньому дитинстві, зазвичай досягає пікового розміру до 9-місячного віку і, як очікується, регресує на 80% до 4 років, тоді як ВГП із швидкою інволюцією повністю регресує до 12–14 міс. Мінімальна або часткова регресія можуть відзначатися при ВГП з частковою інволюцією або без інволюції (Lewis D. et al., 2022).
Дієта при гемангіомі печінки
Рекомендовано відмовитися від вживання алкоголю та газованих напоїв. Не рекомендовано вживати жирну, смажену, копчену їжу та консервовані продукти. Важливо включити до раціону харчування печінку, нежирну рибу, овочі, солодкі фрукти та молочні продукти.
Профілактика
Оскільки причини появи ГП не повністю вивчені, немає методів її профілактики. Проте, враховуючи, що високий рівень естрогену може бути предиктором росту ГП, жінкам можна уповільнити або запобігти росту ГП шляхом припинення прийому або уникнення замісної гормональної терапії.