Джокер (Joker)

Силденафіл - 25 мг/мл
фармакодинаміка
Механізм дії. Силденафіл — препарат для перорального застосування, призначений для лікування еректильної дисфункції. У нормальних умовах, тобто при сексуальному збудженні, препарат відновлює порушену еректильну функцію шляхом посилення припливу крові до статевого члена.
Фізіологічний механізм, що зумовлює ерекцію, включає вивільнення оксиду азоту (NO) у кавернозних тілах під час сексуального збудження. Потім вивільнений NO активує фермент гуанілатциклазу, що стимулює підвищення рівня циклічного гуанозинмонофосфату (цГМФ), що, у свою чергу, викликає розслаблення гладких м’язів кавернозних тіл, сприяючи припливу крові.
Силденафіл є потужним та селективним інгібітором цГМФ-специфічної фосфодіестерази-5 (ФДЕ-5) у кавернозних тілах, де ФДЕ-5 відповідає за розпад цГМФ. Ефекти силденафілу на ерекцію мають периферичний характер. Силденафіл не чинить безпосередньої розслаблювальної дії на окремі кавернозні тіла людини, але потужно посилює розслаблювальну дію NO на дану тканину.
При активації метаболічного шляху NO/цГМФ, що відбувається при сексуальній стимуляції, інгібування силденафілом ФДЕ-5 призводить до підвищення рівня цГМФ у кавернозних тілах. Таким чином, для того щоб силденафіл викликав потрібний фармакологічний ефект, необхідне сексуальне збудження.
Фармакодинамічна дія. Дослідження in vitro продемонстрували, що силденафіл є селективним до ФДЕ-5, що бере активну участь у процесі ерекції. Ефект силденафілу на ФДЕ-5 потужніший, ніж на інші відомі ФДЕ. Цей ефект у 10 разів потужніший, ніж ефект на ФДЕ-6, що бере участь у процесах фотоперетворення в сітківці. При застосуванні максимальних рекомендованих доз відмічається селективність у 80 разів порівняно з ФДЕ-1 і більше ніж у 700 разів порівняно з ФДЕ-2, ФДЕ-3, ФДЕ-4, ФДЕ-7, ФДЕ-8, ФДЕ-9, ФДЕ-10 та ФДЕ-11. Зокрема, селективність силденафілу до ФДЕ-5 у 4000 разів перевищує його селективність до ФДЕ-3 — цАМФ-специфічної ізоформи ФДЕ, що бере участь у регуляції серцевої скоротливості.
Фармакокінетика
Абсорбція. Силденафіл швидко абсорбується. Cmax досягалася протягом 30–120 хв (у середньому 60 хв) після перорального застосування натще. Середня абсолютна пероральна біодоступність становить 41% (діапазон — 25–63%). Після перорального прийому силденафілу AUC та Cmax збільшуються пропорційно підвищенню дози в рамках рекомендованого діапазону доз (25–100 мг).
При прийомі силденафілу разом з їжею швидкість абсорбції знижується із середньою затримкою Tmax 60 хв та із середнім зниженням Cmax на 29%.
Розподіл. Середній об’єм розподілу в стабільному стані (Vd) для силденафілу становить 105 л, що свідчить про розподіл у тканинах організму. Після перорального застосування одноразової дози 100 мг середня максимальна загальна концентрація силденафілу в плазмі крові становить близько 440 нг/мл (CV 40%). Оскільки силденафіл (та його основний метаболіт N-дезметил у загальному кровообігу) на 96% зв’язується з білками плазми крові, це призводить до середньої Cmax вільного силденафілу в плазмі крові — 18 нг/мл (38 нМ). Зв’язування з білками не залежить від загальної концентрації препарату.
У здорових добровольців, які приймали силденафіл (100 мг — одноразова доза), менше ніж 0,0002% (в середньому 188 нг) введеної дози виявлено в еякуляті через 90 хв після дозування.
Метаболізм. Силденафіл головним чином перетворюється за допомогою мікросомальних ізоферментів печінки CYP 3A4 (основний шлях) та CYP 2C9 (другорядний шлях). Основний метаболіт у загальному кровообігу утворюється шляхом N-деметилювання силденафілу. Цей метаболіт має профіль селективності ФДЕ, подібний до силденафілу, та потужність in vitro для ФДЕ-5 близько 50% тієї, що має первинний препарат. Концентрація цього метаболіту в плазмі крові становить близько 40% тих концентрацій, що відмічені для силденафілу. Метаболіт N-дезметил далі метаболізується з кінцевим Т½ близько 4 год.
Виведення. Загальний кліренс силденафілу становить 41 л/год, зумовлюючи Т½ тривалістю 3–5 год. Як після перорального, так і після в/в застосування екскреція силденафілу у вигляді метаболітів здійснюється головним чином із калом (близько 80% введеної пероральної дози) та меншою мірою із сечею (близько 13% введеної пероральної дози).
Фармакокінетика у особливих груп пацієнтів
Пацієнти літнього віку. У здорових добровольців літнього віку (віком від 65 років) відзначалося зниження кліренсу силденафілу, що зумовлювало підвищення плазмових концентрацій силденафілу та його активного N-деметильованого метаболіту приблизно на 90% порівняно з відповідними концентраціями у здорових добровольців молодшого віку (18–45 років). У зв’язку з віковими відмінностями у зв’язуванні з білками плазми крові відповідне підвищення плазмової концентрації вільного силденафілу становило близько 40%.
Ниркова недостатність. У добровольців із порушеннями функції нирок легкого та помірного ступеня (кліренс креатиніну 30–80 мл/хв) фармакокінетика силденафілу залишалася незміненою після його одноразового перорального застосування в дозі 50 мг. Середні AUC та Cmax N-деметильованого метаболіту підвищувалися максимум на 126 та 73% відповідно порівняно з такими показниками у добровольців такого ж віку без порушень функції нирок. Однак через високу індивідуальну варіабельність ці відмінності не були статистично значущими. У добровольців із тяжкими порушеннями функції нирок (кліренс креатиніну <30 мл/хв) кліренс силденафілу знижувався, що призводило до середнього підвищення AUC та Cmax на 100 та 88% відповідно порівняно із добровольцями такого ж віку без порушень функції нирок. Крім того, значення AUC та Cmax N-деметильованого метаболіту значуще підвищувалися — на 200 та 79% відповідно.
Печінкова недостатність. У добровольців із цирозом печінки легкого та помірного ступеня (класи А та В за класифікацією Чайлда — П’ю) кліренс силденафілу знижувався, що призводило до підвищення AUC (84%) та Cmax (47%) порівняно із добровольцями такого ж віку без порушень функції печінки. Фармакокінетика силденафілу у пацієнтів із порушеннями функції печінки тяжкого ступеня не вивчалася.
рекомендується застосовувати у дорослих чоловіків із еректильною дисфункцією, яка визначається як нездатність досягти або підтримати ерекцію статевого члена, необхідну для успішного статевого акту.
Для ефективної дії препарату необхідне сексуальне збудження.
дорослі. Рекомендована доза становить 2 мл (4 активації дозатора), що еквівалентно 50 мг силденафілу, прийнятого за потреби, приблизно за годину до статевої активності. Враховуючи ефективність та переносимість, дозу можна знизити до 1 мл (2 активації дозатора), що еквівалентно 25 мг силденафілу. Крім того, лікар рекомендуватиме дозу, яка відповідно підходить для кожного пацієнта.
Максимальна рекомендована доза становить 2 мл (4 активації дозатора), що еквівалентно 50 мг силденафілу. Максимальна рекомендована частота прийому — 1 раз на добу. Ефективність лікарського засобу під час прийому їжі може виявлятися пізніше, порівняно з прийомом натще (див. Фармакокінетика).
| Кількість активацій дозатора | Кількість вивільненої суспензії, мл | Кількість силденафілу, мг |
| 2 | 1 | 25 |
| 4 | 2 | 50 |
Кожна активація дозатора вивільнює 0,5 мл суспензії, яка містить 12,5 мг силденафілу.
Особливі групи пацієнтів
Пацієнти літнього віку. Для пацієнтів літнього віку (віком від 65 років) зміна дози не потрібна.
Пацієнти з нирковою недостатністю. Для пацієнтів із нирковою недостатністю легкого та помірного ступеня тяжкості (кліренс креатиніну 30–80 мл/хв) рекомендована доза препарату є такою ж, як наведено вище у Дорослі.
Оскільки у пацієнтів із нирковою недостатністю тяжкого ступеня (кліренс креатиніну <30 мл/хв) кліренс силденафілу знижений, слід розглянути можливість застосування дози 25 мг (2 активації дозатора). Залежно від ефективності та переносимості препарату при необхідності дозу можна підвищити поступово до 50 та 100 мг.
Пацієнти із печінковою недостатністю. Оскільки у пацієнтів із печінковою недостатністю (наприклад із цирозом) кліренс силденафілу знижений, слід розглянути можливість застосування дози 25 мг (2 активації дозатора). Залежно від ефективності та переносимості препарату при необхідності дозу можна підвищити поступово до 50 та 100 мг.
Пацієнти, які застосовують інші лікарські засоби. Якщо пацієнти одночасно застосовують інгібітори СYP 3A4 (див. ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ), слід розглянути можливість застосування початкової дози в 1 мл (2 активації дозатора), що еквівалентно 25 мг силденафілу (за винятком ритонавіру, застосування якого одночасно із силденафілом не рекомендується, див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
З метою мінімізації можливого розвитку постуральної гіпотензії у пацієнтів, які застосовують блокатори α-адренорецепторів, їх стан потрібно стабілізувати за допомогою блокаторів α-адренорецепторів до початку застосування силденафілу. Також слід розглянути можливість застосування початкової дози в 1 мл (2 активації дозатора), що еквівалентна 25 мг силденафілу (див. ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ та ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
Спосіб застосування. Приймати перорально. За жодних обставин р-н не вводити будь-яким іншим способом.
Рекомендовано приймати натще, оскільки абсорбція може затримуватися при прийомі з їжею.
Перед першим застосуванням необхідно тричі натиснути на активатор дозатора, щоб відкинути вміст для заповнення дозатора. Неможливість заповнити дозатор може призвести до введення нижчої дози при першому застосуванні.
За жодних обставин не вводити лікарський засіб назально або підшкірно.
1. Перед кожним застосуванням енергійно струсити флакон для розчинення осаду лікарського засобу (див. рис. 1).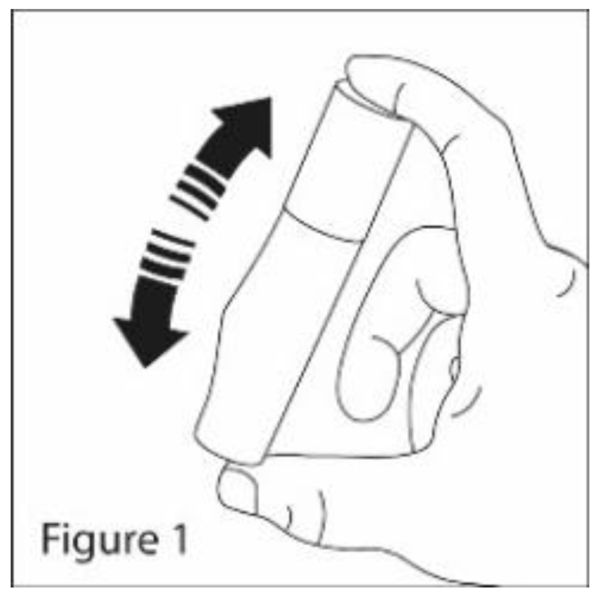
2. Повернути дозатор у відкрите положення (див. рис. 2).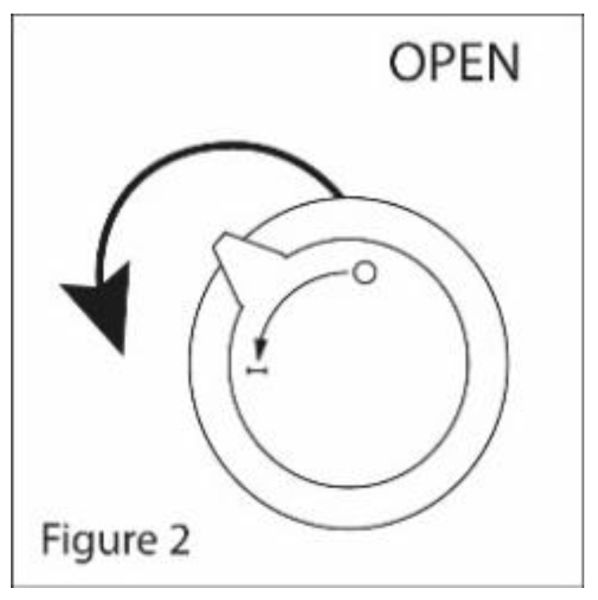
3. Тільки для першого використання: тричі натиснути на активатор дозатора для його заповнення та не використовувати першу дозу препарату, яка виприскується з дозатора після третього натиснення (через конструкцію дозатора при перших двох активаціях дозатора продукт відсутній).
4. Трошки нахилити голову назад. Помістити дозатор у рот. Натискати на дозатор стільки разів, скільки необхідно, відповідно до дози, яка призначена лікарем, і нанести суспензію на язик та негайно проковтнути її зі слиною. Уникати прямого контакту між кінцем дозатора та внутрішньою частиною рота та язика (див. рис. 3).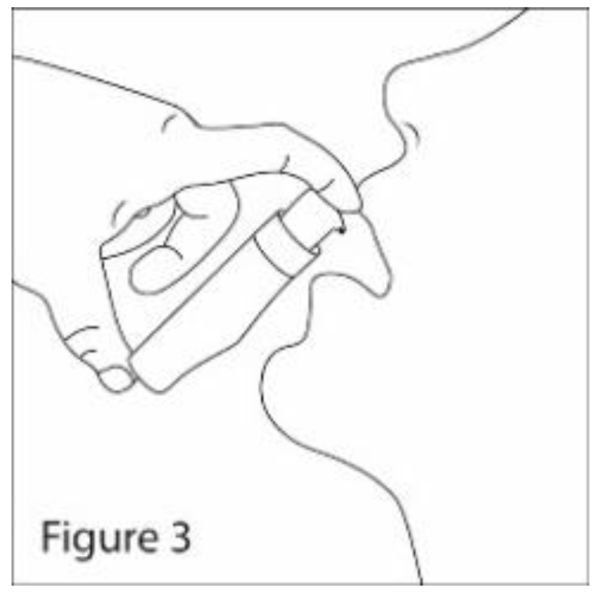
5. Повернути дозатор у закрите положення (див. рис. 4).
Діти. Лікарський засіб не показаний до застосування у дітей віком до 18 років.
— підвищена чутливість до активної речовини або будь-якої з допоміжних речовин препарату.
— Одночасне застосування із донорами NO (такими як амілнітрит) або нітратами в будь-якій формі протипоказане, оскільки відомо, що силденафіл впливає на шляхи метаболізму NO/цГМФ (див. Фармакодинаміка) та потенціює гіпотензивний ефект нітратів.
— Одночасне застосування інгібіторів ФДЕ-5 (у тому числі силденафілу) зі стимуляторами гуанілатциклази, такими як ріоцигуат, протипоказане, оскільки може призвести до симптоматичної гіпотензії (див. ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
— Стани, при яких не рекомендована сексуальна активність (наприклад пацієнтам із тяжкими серцево-судинними розладами, такими як нестабільна стенокардія або серцева недостатність тяжкого ступеня).
— Втрата зору на одне око внаслідок неартеріальної передньої ішемічної нейропатії зорового нерва (NAION), незалежно від того, пов’язана ця патологія із попереднім застосуванням інгібіторів ФДЕ-5 чи ні (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
— Наявність таких захворювань, як порушення функції роботи печінки тяжкого ступеня, артеріальна гіпотензія (артеріальний тиск <90/50 мм рт. ст.), нещодавно перенесений інсульт або інфаркт міокарда та відомі спадкові дегенеративні захворювання сітківки, такі як пігментний ретиніт (невелика кількість таких пацієнтів має генетичні розлади ФДЕ сітківки), оскільки безпека застосування силденафілу не досліджувалася у таких підгрупах пацієнтів.
короткий зміст профілю безпеки. Профіль безпеки силденафілу базується на даних 9570 пацієнтів у процесі 74 подвійних сліпих плацебо-контрольованих клінічних досліджень. Найчастішими побічними реакціями під час клінічних досліджень у пацієнтів, які приймали силденафіл, були головний біль, почервоніння обличчя, диспепсія, закладеність носа, біль у спині, запаморочення, нудота, припливи жару, порушення зору, ціанопсія та затьмарення зору.
Інформація щодо побічних реакцій у рамках постмаркетингового спостереження застосування силденафілу зібрана протягом більше ніж 10 років. Оскільки не про всі побічні реакції повідомлялося власнику реєстраційного посвідчення та включалися до бази даних з безпеки, частоту цих реакцій неможливо точно визначити.
Табличний перелік побічних реакцій. Нижче вказані всі клінічні важливі побічні реакції, які мали місце в клінічних дослідженнях при частоті появи більше, ніж при прийомі плацебо, за системами організму та частотою:
— дуже часто (≥1/10);
— часто (≥1/100, <1/10);
— нечасто (≥1/1000, <1/100);
— рідко (≥1/10 000, <1/1000);
— дуже рідко (<1/10 000);
— частота невідома (не може бути визначена на основі наявних даних), яка повідомлялася з постмаркетингового досвіду.
У кожній групі за частотою побічні ефекти представлені в порядку зниження серйозності.
Клінічно значимі побічні реакції, які відмічені в контрольованих клінічних дослідженнях при частоті, вищій, ніж плацебо, та клінічно значимі побічні реакції, відмічені протягом постмаркетингового періоду.
Інфекційні та інвазивні захворювання: нечасто — риніт.
З боку імунної системи: нечасто — гіперчутливість.
З боку нервової системи: дуже часто — головний біль; часто — запаморочення; нечасто — сонливість, гіпестезія; рідко — інсульт, транзиторна ішемічна атака, судоми*, рецидиви судом*, синкопе.
З боку органа зору: часто — порушення сприйняття кольору**, розлади зору, затьмарення зору; нечасто — розлади сльозовиділення***, біль в очах, фотофобія, фотопсія, гіперемія очей, яскравість зору, кон’юнктивіт; рідко — неартеріальна передня ішемічна нейропатія зорового нерва*, оклюзія судин сітківки*, ретинальний крововилив, артеріосклеротична ретинопатія, порушення з боку сітківки, глаукома, дефекти поля зору, диплопія, зниження гостроти зору, міопія, астенопія, плаваючі помутніння скловидного тіла, порушення з боку райдужної оболонки, мідріаз, поява сяючих кругів навколо джерела світла (гало) у полі зору, набряк очей, припухлість очей, порушення з боку очей, гіперемія кон’юнктиви, подразнення очей, аномальні відчуття в очах, набряк повік, знебарвлення склери.
З боку органа слуху та вестибулярного апарату: нечасто — запаморочення, дзвін у вухах; рідко — глухота.
З боку серця: нечасто — тахікардія, посилене серцебиття; рідко — раптова серцева смерть*, інфаркт міокарда, шлуночкова аритмія*, фібриляція передсердь, нестабільна стенокардія.
З боку судин: часто — почервоніння обличчя, припливи жару; нечасто — гіпертензія, гіпотензія.
З боку респіраторної системи, органів грудної клітки та середостіння: часто — закладеність носа; нечасто — носова кровотеча, закладеність придаткових пазух носа; рідко — відчуття стиснення в горлі, набряк слизової оболонки носа, сухість у носі.
З боку ШКТ: часто — нудота, диспепсія; нечасто — гастроезофагеальна рефлюксна хвороба, блювання, біль у верхній частині живота, сухість у роті; рідко — гіпестезія ротової порожнини.
З боку шкіри та підшкірної тканини: нечасто — висип; рідко — синдром Стівенса — Джонсона*, токсичний епідермальний некроліз*.
З боку опорно-рухового апарату та сполучної тканини: нечасто — міалгія, біль у кінцівках.
З боку сечовидільної системи: нечасто — гематурія.
З боку репродуктивної системи та молочних залоз: рідко — кровотеча зі статевого члена, пріапізм*, гематоспермія, подовжена ерекція.
Загальні розлади та реакції у місці введення: нечасто — біль у грудях, підвищена стомлюваність, відчуття жару; рідко — подразнення.
Обстеження: нечасто — підвищена ЧСС.
*Повідомлялося лише під час дослідження після виходу препарату на ринок.
**Порушення сприйняття кольору: хлоропсія, хроматопсія, ціанопсія, еритропсія, ксантопсія.
***Порушення сльозовиділення: сухість в очах, порушення сльозовиділення та підвищення сльозовиділення.
Зазначені нижче побічні реакції відмічали у <2% пацієнтів у процесі контрольованих клінічних досліджень; їх причинний взаємозв’язок із застосуванням силденафілу є невизначеним. Зазначені побічні реакції, що мали вірогідний зв’язок із застосуванням лікарського засобу. При цьому не включали побічні реакції легкого ступеня та ті, повідомлення про які були дуже неточними, щоб мати значення.
Загальні: набряк обличчя, реакції фоточутливості, шок, астенія, біль, раптове падіння, біль у животі, раптове пошкодження.
З боку серцево-судинної системи: стенокардія, АV-блокада, мігрень, постуральна гіпотензія, ішемія міокарда, тромбоз судин головного мозку, раптова зупинка серця, порушення результатів на ЕКГ, кардіоміопатія.
З боку ШКТ: глосит, коліт, дисфагія, гастрит, гастроентерит, езофагіт, стоматит, порушення результатів печінкових проб, ректальна кровотеча, гінгівіт.
З боку системи крові та лімфатичної системи: анемія, лейкопенія.
Розлади метаболізму та харчування: спрага, набряк, подагра, нестабільний діабет, гіперглікемія, периферичні набряки, гіперурикемія, гіпоглікемія, гіпернатріємія.
З боку скелетно-м’язової системи: артрит, артроз, розрив сухожилля, теносиновіт, біль у кістках, міастенія, синовіт.
З боку нервової системи: атаксія, невралгія, нейропатія, парестезія, тремор, вертиго, депресія, безсоння, аномальні сновидіння, зниження рефлексів.
З боку дихальної системи: БА, диспное, ларингіт, фарингіт, синусит, бронхіт, посилене слиновиділення, посилення кашлю.
З боку шкіри: кропив’янка, герпес, свербіж, підвищена пітливість, виразки шкіри, контактний дерматит, ексфоліативний дерматит.
Специфічні відчуття: раптове зниження чи втрата слуху, біль у вухах, крововилив в око, катаракта, сухість в очах.
З боку урогенітальної системи: цистит, ніктурія, підвищена частота сечовипускань, збільшення молочних залоз, нетримання сечі, порушення еякуляції, набряк статевих органів, аноргазмія.
Досвід застосування після виходу на ринок. Зазначені нижче побічні реакції були виявлені після реєстрації даного лікарського засобу. Оскільки про такі реакції повідомляють добровільно та повідомлення надходять від популяції невідомої чисельності, не завжди можна достовірно оцінити їх частоту та встановити причинний зв’язок із експозицією лікарського засобу. Ці побічні реакції було взято до уваги у зв’язку з наявністю таких факторів: серйозність, частота повідомлення, відсутність чіткого альтернативного зв’язку та комбінація всіх цих факторів.
Серцево-судинні та цереброваскулярні явища. Повідомлялося про серйозні серцево-судинні, цереброваскулярні та судинні явища, включаючи цереброваскулярну кровотечу, субарахноїдальну і внутрішньоцеребральну кровотечу та легеневу кровотечу, що були пов’язані в часі із застосуванням силденафілу. У більшості пацієнтів, але не у всіх, наявні фактори серцево-судинного ризику. Багато з цих явищ виникли під час або відразу після сексуальної активності та декілька явищ виникли відразу після застосування силденафілу без сексуальної активності. Інші явища розвинулися протягом наступних годин чи днів після застосування силденафілу та сексуальної активності. Неможливо встановити, чи пов’язані ці явища із застосуванням лікарського засобу, із сексуальною активністю, із наявними факторами ризику чи з комбінацією цих факторів, чи з іншими факторами.
З боку кровоносної та лімфатичної системи: вазооклюзивний криз. У невеликому, завчасно припиненому дослідженні застосування препарату Ревацио (силденафіл) пацієнтам із легеневою артеріальною гіпертензією, вторинною щодо серпоподібно-клітинної анемії, при застосуванні силденафілу про розвиток вазооклюзивних кризів, що потребували госпіталізації, повідомлялося частіше, ніж при застосуванні плацебо. Клінічне значення цієї інформації для пацієнтів, які застосовують препарат Джокер з метою лікування еректильної дисфункції, невідоме.
З боку нервової системи: тривога, транзиторна глобальна амнезія.
Специфічні відчуття
Слух. Після реєстрації силденафілу зафіксовано випадки раптового зниження чи втрати слуху, пов’язані в часі із застосуванням лікарського засобу. У деяких випадках повідомлялося про наявність медичних станів та інших факторів, що могли відіграти роль у розвитку побічних реакцій з боку слуху. У багатьох випадках інформація щодо подальшого медичного спостереження відсутня. Визначити, чи ці явища прямо пов’язані із застосуванням лікарського засобу, чи з наявними факторами ризику втрати слуху, чи з комбінацією цих факторів або з іншими факторами, неможливо.
Зір. Тимчасова втрата зору, почервоніння очей, печіння в очах, підвищення внутрішньоочного тиску, набряк сітківки, судинні захворювання сітківки чи кровотеча, відшарування скловидного тіла. Після реєстрації силденафілу рідко повідомлялося про випадки неартеріальної передньої ішемічної нейропатії зорового нерва, що є причиною зниження зору, включаючи постійну втрату зору, які були пов’язані в часі із застосуванням інгібіторів ФДЕ-5, включаючи силденафіл. У багатьох пацієнтів були наявні анатомічні або судинні фактори ризику розвитку неартеріальної передньої ішемічної нейропатії зорового нерва, включаючи такі фактори: низьке співвідношення діаметра екскавації та диска зорового нерва (застійний диск зорового нерва), вік старше 50 років, гіпертензія, захворювання коронарних артерій, гіперліпідемія та паління. Неможливо визначити, чи ці явища прямо пов’язані із застосуванням інгібіторів ФДЕ-5, з наявними анатомічними або судинними факторами ризику, з комбінацією цих всіх факторів чи з іншими факторами.
для діагностики порушень ерекції, визначення можливих причин захворювання та призначення адекватного лікування необхідно ретельно вивчити історію хвороби пацієнта та провести ретельне медичне обстеження.
Тільки для перорального застосування. Не вводити будь-якими іншими способами.
Фактори ризику серцево-судинних захворювань. Оскільки сексуальна активність супроводжується певним ризиком з боку серця, до початку будь-якого лікування еректильної дисфункції лікар має оцінити стан серцево-судинної системи пацієнта.
Силденафіл чинить судинорозширювальну дію, що виявляється легким та короткочасним зниженням АТ (див. Фармакодинаміка). До призначення силденафілу лікар має ретельно зважити, чи може такий ефект несприятливо впливати на пацієнтів із певними основними захворюваннями, особливо в комбінації із сексуальною активністю. До пацієнтів із підвищеною чутливістю до вазодилататорів належать хворі з обструкцією вивідного тракту лівого шлуночка (наприклад стеноз аорти, гіпертрофічна обструктивна кардіоміопатія) або пацієнти із рідкісним синдромом мультисистемної атрофії, одним із проявів якої є тяжке порушення регуляції АТ з боку вегетативної нервової системи.
Лікарський засіб посилює гіпотензивну дію нітратів (див. ПРОТИПОКАЗАННЯ).
У період після впровадження силденафілу в широку медичну практику повідомлялося про серйозні серцево-судинні ускладнення, включаючи інфаркт міокарда, нестабільну стенокардію, раптову серцеву смерть, вентрикулярну аритмію, цереброваскулярну геморагію, транзиторну ішемічну атаку, артеріальну гіпертензію та артеріальну гіпотензію, які за часом збігалися із застосуванням силденафілу. Більшість, але не всі, з цих пацієнтів мали попередні серцево-судинні фактори ризику. Переважна кількість таких випадків відмічена протягом або відразу після статевого акту і лише кілька — невдовзі після застосування силденафілу без сексуальної активності. Тому неможливо визначити, чи пов’язаний розвиток таких побічних реакцій безпосередньо із факторами ризику, чи їх розвиток зумовлений іншими чинниками.
Пріапізм. Засоби для лікування еректильної дисфункції, у тому числі й силденафіл, слід призначати з обережністю пацієнтам з анатомічною деформацією статевого члена (такою як ангуляція, кавернозний фіброз або хвороба Пейроні) або пацієнтам зі станами, що спричиняють розвиток пріапізму (такими як серпоподібно-клітинна анемія, множинна мієлома або лейкемія). Після виходу силденафілу на ринок повідомлялося про випадки подовженої ерекції та пріапізму. Якщо ерекція триває більше ніж 4 год, пацієнтам слід негайно звернутися за медичною допомогою. За відсутності негайного лікування пріапізм може призвести до пошкодження тканин статевого члена та стійкої втрати потенції.
Одночасне застосування з іншими інгібіторами ФДЕ-5 або іншими препаратами для лікування еректильної дисфункції. Безпека та ефективність одночасного застосування силденафілу з іншими інгібіторами ФДЕ-5, препаратами для лікування гіпертензії легеневої артерії, які містять силденафіл (наприклад препарат Ревацио), або іншими препаратами для лікування еректильної дисфункції не вивчалися, тому застосовувати такі комбінації не рекомендується.
Вплив на зір. Дефекти зору та випадки неартеріальної передньої ішемічної нейропатії здорового нерва відмічали у зв’язку з прийомом силденафілу та інших інгібіторів ФДЕ-5 (див. ПОБІЧНА ДІЯ). Про випадки неартеріальної передньої ішемічної нейропатії зорового нерва, що є рідкісним станом, надходили спонтанні повідомлення та повідомлялося в наглядовому дослідженні асоційовано із застосуванням силденафілу та інших інгібіторів ФДЕ-5 (див. ПОБІЧНА ДІЯ). Пацієнтів слід попередити, що у разі раптового порушення зору застосування лікарського засобу слід припинити та негайно звернутися до лікаря (див. ПРОТИПОКАЗАННЯ).
Одночасне застосування з ритонавіром. Одночасне застосування силденафілу та ритонавіру не рекомендується (див. ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
Одночасне застосування з блокаторами α-адренорецепторів. Силденафіл рекомендується з обережністю застосовувати у пацієнтів, які одночасно застосовують блокатори α-адренорецепторів, оскільки в деяких випадках це може призвести до симптоматичної гіпотензії у деяких схильних до цього пацієнтів (див. ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ). Симптоматична гіпотензія зазвичай виникає протягом 4 год після застосування силденафілу. З метою мінімізації можливого розвитку постуральної гіпотензії у пацієнтів, які застосовують блокатори α-адренорецепторів, їх стан необхідно стабілізувати за допомогою блокаторів α-адренорецепторів до початку застосування силденафілу. Також слід розглянути можливість застосування початкової дози 25 мг (2 активації дозатора) (див. ЗАСТОСУВАННЯ). Крім того, слід поінформувати пацієнтів, як діяти у разі появи симптомів ортостатичної гіпотензії.
Вплив на кровотечі. Дослідження тромбоцитів людини in vitro свідчать, що силденафіл посилює антиагрегаційний ефект натрію нітропрусиду. Немає жодної інформації з безпеки щодо призначення силденафілу пацієнтам зі схильністю до кровотечі або з гострою виразкою шлунка, тому цій групі пацієнтів силденафіл слід призначати тільки після ретельної оцінки користі та ризику.
Втрата слуху. Лікарям слід порадити пацієнтам припинити застосування інгібіторів ФДЕ-5, включаючи силденафіл, та негайно звернутися за медичного допомогою у разі раптового зниження чи втрати слуху. Про ці явища, які також можуть супроводжуватися дзвоном у вухах та запамороченням, повідомлялося з асоціацією в часі із застосуванням інгібіторів ФДЕ-5, включаючи силденафіл. Визначити, чи ці явища прямо пов’язані із застосуванням інгібіторів ФДЕ-5, чи з іншими факторами, неможливо.
Одночасне застосування із гіпотензивними препаратами. Силденафіл чинить системну судинорозширювальну дію та може в подальшому знижувати АТ у пацієнтів, які застосовують гіпотензивні лікарські засоби. У окремому дослідженні лікарської взаємодії при одночасному застосуванні амлодипіну (5 або 10 мг) та силденафілу перорально виявлено середнє додаткове зниження систолічного тиску на 8 мм рт. ст. та діастолічного — на 7 мм рт. ст.
Захворювання, що передаються статевим шляхом. Застосування силденафілу не захищає від захворювань, що передаються статевим шляхом. Слід розглянути можливість інформування пацієнтів щодо необхідних запобіжних заходів для захисту від захворювань, що передаються статевим шляхом, включаючи ВІЛ.
Фертильність. Після застосування дози 100 мг у здорових добровольців не відмічено впливу на морфологію чи рухомість сперматозоїдів (див. Фармакодинаміка).
Застосування у період вагітності або годування грудьми. Лікарський засіб не призначений для застосування у жінок.
Здатність впливати на швидкість реакції при керуванні транспортними засобами або іншими механізмами. Препарат може чинити незначний вплив на керування транспортними засобами або іншими механізмами. У процесі клінічних досліджень застосування силденафілу повідомлялося про випадки запаморочення та порушення з боку органа зору, тому перед керуванням транспортними засобами або іншими механізмами пацієнтам необхідно з’ясувати, якою є їх індивідуальна реакція на застосування лікарського засобу.
вплив інших лікарських засобів на силденафіл
Дослідження in vitro. Метаболізм силденафілу відбувається переважно за участю ізоформи 3A4 (головний шлях) та ізоформи 2C9 (другорядний шлях) цитохрому P450 (CYP). Тому інгібітори цих ізоферментів можуть знижувати кліренс силденафілу, а індуктори цих ізоферментів — підвищувати кліренс силденафілу.
Дослідження in vivo. Популяційний фармакокінетичний аналіз даних клінічних досліджень продемонстрував зниження кліренсу силденафілу при його одночасному застосуванні з інгібіторами CYP 3A4 (такими як кетоконазол, еритроміцин, циметидин). Хоча у цих пацієнтів при одночасному застосуванні силденафілу та інгібіторів CYP 3A4 зростання частоти побічних явищ не виявлено, слід розглянути можливість застосування початкової дози силденафілу 25 мг (2 активації дозатора).
Одночасне застосування інгібітора ВІЛ-протеази — ритонавіру, дуже потужного інгібітора CYP, у стані рівноважної концентрації (500 мг 2 рази на добу) та силденафілу (одноразова доза 100 мг) призводило до підвищення Cmax силденафілу на 300% (у 4 рази) та підвищення плазмової AUC силденафілу на 1000% (у 11 разів). Через 24 год плазмові рівні силденафілу все ще становили близько 200 нг/мл порівняно з рівнем близько 5 нг/мл, характерним для застосування силденафілу окремо, що відповідає значному впливу ритонавіру на широкий спектр субстратів CYP. Силденафіл не впливає на фармакокінетику ритонавіру. Враховуючи ці фармакокінетичні дані, одночасне застосування силденафілу та ритонавіру не рекомендується (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ); у будь-якому випадку максимальна доза силденафілу за жодних обставин не повинна перевищувати 25 мг (2 активації дозатора) протягом 48 год.
Одночасне застосування інгібітора ВІЛ-протеази — саквінавіру, інгібітора СYP 3A4, у дозі, що забезпечує рівноважну концентрацію (1200 мг 3 рази на добу), та силденафілу (100 мг одноразово) призводило до підвищення Cmax силденафілу на 140% та збільшення AUC силденафілу на 210%. Не виявлено впливу силденафілу на фармакокінетику саквінавіру (див. ЗАСТОСУВАННЯ). Передбачається, що більш потужні інгібітори CYP 3A4, такі як кетоконазол та ітраконазол, будуть чинити більш виражений вплив.
При застосуванні силденафілу (100 мг одноразово) та еритроміцину, помірного інгібітора CYP 3A4, у рівноважному стані (500 мг 2 рази на добу протягом 5 днів) відмічено підвищення AUC силденафілу на 182%. У здорових добровольців чоловічої статі не виявлено впливу азитроміцину (500 мг/добу протягом 3 діб) на AUC, Cmax та Тmax, константу швидкості елімінації та подальший Т½ силденафілу та його головного циркулюючого метаболіту. Циметидин (інгібітор CYP та неспецифічний інгібітор CYP 3A4) у дозі 800 мг при одночасному застосуванні із силденафілом у дозі 50 мг у здорових добровольців призводив до підвищення плазмових концентрацій силденафілу на 56%.
Грейпфрутовий сік є слабким інгібітором CYP 3A4 у стінці кишечнику і може викликати помірне підвищення рівня силденафілу у плазмі крові.
Одноразове застосування антацидів (магнію гідроксиду/алюмінію гідроксиду) не впливало на біодоступність силденафілу.
Хоча досліджень специфічної взаємодії з усіма лікарськими засобами не проводилося, за даними популяційного фармакокінетичного аналізу, фармакокінетика силденафілу не змінювалася при його одночасному застосуванні з лікарськими засобами, що належать до групи інгібіторів CYP 2C9 (толбутамід, варфарин, фенітоїн), групи інгібіторів CYP 2D6 (таких як селективні інгібітори зворотного захоплення серотоніну, трициклічні антидепресанти), групи тіазидних та тіазидоподібних діуретиків, петльових та калійзберігаючих діуретиків, інгібіторів АПФ, антагоністів кальцію, антагоністів β-адренорецепторів або індукторів метаболізму CYP (таких як рифампіцин, барбітурати).
У процесі дослідження за участю здорових добровольців-чоловіків одночасне застосування антагоніста ендотеліну босентану (помірний індуктор CYP 3A4, CYP 2C9 та, можливо, CYP 2C19) у рівноважному стані (125 мг 2 рази на добу) та силденафілу в рівноважному стані (80 мг 3 рази на добу) призводило до зниження AUC та Cmax силденафілу на 62,6 та 55,4% відповідно. Тому одночасне застосування таких потужних індукторів CYP 3A4, як рифампін, може призводити до більш вираженого зниження концентрації силденафілу в плазмі крові.
Нікорандил являє собою гібрид активатора кальцієвих каналів та нітрату. Нітратний компонент зумовлює можливість його серйозної взаємодії із силденафілом.
Вплив силденафілу на інші лікарські засоби
Дослідження in vitro. Силденафіл — це слабкий інгібітор ізоформ CYP 1A2, 2C9, 2C19, 2D6, 2E1 та 3A4 (IC50>150 мкМ). Оскільки Cmax силденафілу дорівнює близько 1 мкмоль, вплив лікарського засобу на кліренс субстратів цих ізоферментів малоймовірний. Відсутні дані щодо взаємодії силденафілу та таких неспецифічних інгібіторів ФДЕ, як теофілін та дипіридамол.
Дослідження in vivo. Оскільки відомо, що силденафіл чинить вплив на метаболізм NO/цГМФ (див. Фармакодинаміка), встановлено, що силденафіл потенціює гіпотензивну дію нітратів, тому його одночасне застосування з донорами NO або з нітратами в будь-якій формі протипоказане (див. ПРОТИПОКАЗАННЯ).
Ріоцигуат. Доклінічні дослідження продемонстрували адитивний системний ефект зниження АТ при одночасному застосуванні інгібіторів ФДЕ-5 з ріоцигуатом. Клінічні дослідження показали, що ріоцигуат посилює гіпотензивну дію інгібіторів ФДЕ-5. У пацієнтів, які брали участь у дослідженні, не виявлено позитивного клінічного ефекту при одночасному застосуванні інгібіторів ФДЕ-5 із ріоцигуатом. Протипоказане одночасне застосування ріоцигуату з інгібіторами ФДЕ-5, у тому числі із силденафілом (див. ПРОТИПОКАЗАННЯ).
Одночасне застосування силденафілу та блокаторів α-адренорецепторів може призвести до розвитку симптоматичної гіпотензії у деяких схильних до цього пацієнтів. Така реакція найчастіше виникала протягом 4 год після застосування силденафілу (див. ЗАСТОСУВАННЯ та ОСОБЛИВОСТІ ЗАСТОСУВАННЯ). У процесі 3 досліджень специфічної взаємодії лікарських засобів блокатор α-адренорецепторів доксазозин (4 мг та 8 мг) та силденафіл (25 мг, 50 мг та 100 мг) застосовувалися одночасно у пацієнтів із доброякісною гіперплазією передміхурової залози, стабілізація стану яких була досягнута при застосуванні доксазозину.
У цих популяціях виявлено середнє додаткове зниження АТ у положенні лежачи на 7/7 мм рт. ст., 9/5 мм рт. ст. та 8/4 мм рт. ст. та середнє зниження АТ у положенні стоячи на 6/6 мм рт. ст., 11/4 мм рт. ст., 4/5 мм рт. ст. відповідно. При одночасному застосуванні силденафілу та доксазозину у пацієнтів, стабілізація стану яких досягнута при застосуванні доксазозину, іноді повідомлялося про розвиток симптоматичної гіпотензії. У цих повідомленнях йшлося про випадки запаморочення та стан перед непритомністю, але без синкопе.
Не відмічено жодних значущих взаємодій при одночасному застосуванні силденафілу (50 мг) і толбутаміду (250 мг) або варфарину (40 мг), що метаболізуються CYP 2C9.
Силденафіл (50 мг) не призводить до збільшення тривалості кровотечі, спричиненої ацетилсаліциловою кислотою (150 мг).
Силденафіл (50 мг) не потенціював гіпотензивну дію алкоголю у здорових добровольців при середніх максимальних рівнях етанолу у крові 80 мг/дл.
У пацієнтів, які застосовували силденафіл, не виявлено жодних відмінностей у профілі побічних ефектів порівняно з плацебо при одночасному застосуванні таких класів гіпотензивних лікарських засобів, як діуретики, блокатори β-адренорецепторів, інгібітори АПФ, антагоністи ангіотензину II, антигіпертензивні лікарські засоби (судинорозширювальні та центральної дії), блокатори адренергічних нейронів, блокатори кальцієвих каналів та блокатори α-адренорецепторів. У специфічному дослідженні взаємодії при одночасному застосуванні силденафілу (100 мг) та амлодипіну у пацієнтів із артеріальною гіпертензією відмічено додаткове зниження систолічного АТ в положенні лежачи на 8 мм рт. ст. Відповідне зниження діастолічного АТ становило 7 мм рт. ст.
За величиною ці додаткові зниження АТ були порівнянними з тими, що виявлені при застосуванні лише силденафілу у здорових добровольців (див. ФАРМАКОЛОГІЧНІ ВЛАСТИВОСТІ).
Силденафіл у дозі 100 мг не впливав на фармакокінетичні показники інгібіторів ВІЛ-протеази, саквінавіру та ритонавіру, які є субстратами СYP 3A4.
У здорових добровольців чоловічої статі застосування силденафілу в рівноважному стані (80 мг 3 рази на добу) призводило до підвищення AUC та Cmax босентану (125 мг 2 рази на добу) на 49,8 та 42% відповідно.
у процесі клінічних досліджень за участю добровольців під час застосування одноразової дози силденафілу до 800 мг побічні реакції були подібними до тих, що відмічені при застосуванні силденафілу в нижчих дозах, але виникали частіше та були більш тяжкими. Застосування силденафілу в дозі 200 мг не призводило до підвищення ефективності, але спричинило зростання кількості випадків розвитку побічних реакцій (головного болю, почервоніння обличчя, запаморочення, диспепсії, закладеності носа, порушень з боку органа зору).
У разі передозування при необхідності вживають звичайних підтримувальних заходів. Прискорення кліренсу силденафілу при гемодіалізі малоймовірне внаслідок високого ступеня зв’язування препарату з білками плазми крові та відсутності елімінації силденафілу із сечею.
в оригінальній упаковці при температурі не вище 30 °С у недоступному для дітей місці.
Термін придатності після першого відкриття флакона — 12 міс.

