У більшості випадків хворий не може точно вказати час і причину появи симптомів остеоартрозу. Досить тривалий час захворювання навіть при наявності патогістологічних змін і рентгенографічних ознак має безсимптомний перебіг (Cobb S. et al., 1957; Bagge E. et al., 1991).
Фактори ризику виникнення або прогресування ОА колінних і кульшових суглобів та суглобів кистей наведені в табл. 6.1.
Таблиця 6.1
Фактори ризику виникнення або прогресування ОА колінних і кульшових суглобів та суглобів кистей
| Процес | Локалізація | ||
| Колінні суглоби | Кульшові суглоби | Суглоби кистей | |
| Виникнення ОА |
Вік
Жіноча стать Фізична активність ІМТ Попередні ураження ЗГТ Вітамін D Тютюнопаління (захисний вплив) Інтенсивні заняття спортом Сила чотириголового м’яза стегна (m. quadriceps) |
Вік
Фізична активність ІМТ Попередні ушкодження Інтенсивні заняття спортом |
Вік
Сила стискання ІМТ Професія Інтенсивні заняття спортом |
| Прогресування ОА | Вік
Вітамін D ЗГТ Синовіт Інтенсивні заняття спортом Набряк субхондральної кістки на МРТ |
Вік
Симптоматична активність Стать Інтенсивні заняття спортом |
Невідомі |
Найбільш частою ранньою ознакою хвороби є дифузний, непостійний біль у суглобі, що зазвичай виникає під час або відразу після навантаження на суглоб. Для остеоартрозу також характерна ранкова скутість тривалістю не більш 30 хв. Іноді визначається незначна болючість навколосуглобових тканин (головним чином м’язів). Поступово і, як правило, непомітно зменшується обсяг рухів у суглобі. Наприклад, пацієнт може поскаржитися на те, що останнім часом (рік/кілька років) йому усе складніше нахилятися, щоб надягти панчохи, через відчуття скутості в кульшовому суглобі.
Рідко перші симптоми ОА розвиваються швидко (протягом декількох днів або тижнів) після травми. Імовірно, травма в цьому випадку відіграє роль «тригера» для клінічної маніфестації змін у суглобі, що тривалий час мали безсимптомний перебіг.
Основні симптоми і ознаки ОА (за: Dieppe P.A., 1995, зі змінами)
| Симптоми |
|
| Ознаки |
|
Біль. Найважливішим симптомом ОА, безсумнівно, є біль. У порівняльних дослідженнях продемонстрована відмінність кількісних і якісних характеристик болю при ОА і РА (Bellamy N., Buchanan W.W., 1984; Charter R.A. et al., 1985). Для ОА характерний «механічний» біль, тобто такий, що виникає/посилюється під час навантаження на суглоб і згасає у стані спокою. Біль зазвичай виникає через деякий час (хвилини/години) після початку дії навантаження на суглоб (рідше — відразу після навантаження) і може тривати протягом декількох годин після його припинення. Характер больового синдрому є однією із головних диференційно-діагностичних ознак ОА: для запальних процесів у суглобах (артрит, у тому числі й РА), на відміну від дегенеративних, характерний запальний характер болю (виникає/наростає у стані спокою і вночі, зменшується при рухах у суглобі). Рідко хворі на ОА скаржаться на біль у спокої і вночі, проте одночасно їх, як правило, турбує і біль у суглобі при фізичному навантаженні, тобто «механічний біль».
Біль при маніфестному ОА не так виражений, як при артритах, більш локальний, хоча з прогресуванням хвороби набуває стійкого характеру. Певною мірою за характером болю, його стійкістю при ОА можна визначити ступінь тяжкості захворювання в цілому. Наприклад, спочатку біль у конкретному суглобі пов’язаний з рухом і при його припиненні зникає. Пізніше біль у суглобі (суглобах) турбує і у спокої, посилюючись при навантаженні. Зрештою, біль турбує хворого вже й вночі. І хоча клінічно біль у суглобі сприймається однозначно, але в дійсності механізми болю при ОА пов’язані не тільки із синовітом, як при артриті. При синовіті біль виникає при підйомі з ліжка з відчуттям скутості («гелю») в ураженому суглобі, згодом біль посилюється при навантаженні. Біль при певних рухах у суглобі може бути зумовлений залученням періартикулярних тканин, а біль, викликаний відшаруванням періосту у зв’язку з розвитком остеофітів, має локальний характер, посилюючись при пальпації суглоба. Крім того, при ОА біль може бути зумовлений м’язовою патологією, посилюється з наростанням тривоги і депресії, а також у зв’язку з порушенням рухової активності та ін. (Насонова В.А., 2001).
При епідеміологічних і клінічних дослідженнях виявили значні розбіжності інтенсивності болю у різних груп хворих на ОА. Так, за даними J.S. Lawrence та співавторів (1966), наведеними на рис. 6.1, рентгенологічно діагностований коксартроз практично завжди маніфестує клінічно, у той час як лише у невеликої частини хворих на ОА суглобів кистей є специфічні скарги. Тяжкість змін, що виявляються на рентгенограмах уражених суглобів, асоціюється з підвищенням імовірності клінічної маніфестації ОА (Hochberg M.C. et al., 1989). Водночас автори цього дослідження відзначають, що навіть значно виражені зміни на рентгенограмах можуть бути безсимптомними. J. Cashnaghan (1991) вказує на те, що у жінок, хворих на ОА, больовий синдром виражений більш інтенсивно, ніж у чоловіків. Результати дослідження M.N. Summers та співавторів (1988) свідчать про наявність прямого кореляційного зв’язку між болем і занепокоєнням/депресією у пацієнтів з ОА.
Вивчення особливостей болю у пацієнтів з ОА було предметом кількох досліджень. F.A. Hart (1974) описав шість типів больових відчуттів при ОА. Результати детального дослідження болю у 500 пацієнтів з ОА периферичних суглобів (Cashnaghan J., 1991) підтвердили ці дані. Так, найбільш частим варіантом був біль при рухах у суглобі або опорі на кінцівку (use-related pain). Такий біль, за даними авторів, зазвичай виникав протягом декількох секунд/хвилин від початку статичного або динамічного навантаження і міг зберігатися протягом кількох годин після його припинення. Деякі пацієнти скаржилися на непостійний гострий біль, що точно збігається з певними рухами в суглобах або перенесенням важких речей; інші — на постійний характер болю, при цьому вони не могли точно вказати на його локалізацію. У той час як майже всі хворі з маніфестним ОА скаржилися на біль, пов’язаний з рухами в суглобі або опорою на кінцівку, тільки половина з них вказувала на наявність болю у спокої і близько 30% — на біль, що виникає вночі (Cashnaghan J., 1991). Лише у невеликої кількості обстежених інтенсивність болю в уражених суглобах викликала труднощі у повсякденній активності або викликала безсоння. Як правило, у цих випадках на рентгенограмах суглобів виявляли значні й швидкопрогресуючі зміни, часто із залученням субхондральної кістки.
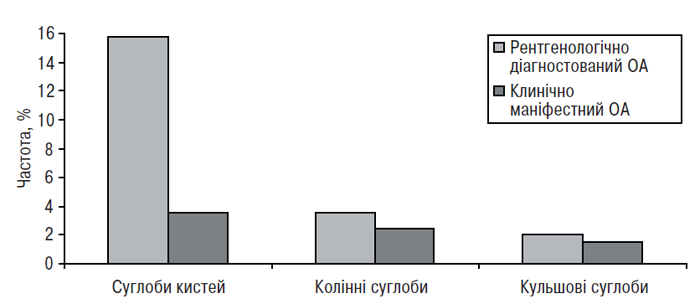
Рис. 6.1. Гістограма, що ілюструє приблизну оцінку частоти тяжкого діагностованого рентгенологічно ОА (II–IV стадії за класифікацією Келлгрена — Лоуренса) і клінічно маніфестного ОА трьох суглобових груп, які найчастіше уражуються при первинному ОА
Біль у суглобі при ОА нерідко супроводжується відчуттям болючості при пальпації області суглоба. Пацієнт може вказати на наявність декількох болючих точок, розміщених по ходу суглобової щілини і в ділянці прилеглих скелетних м’язів.
Механізм, що лежить в основі больового синдрому при ОА, дотепер залишається предметом дискусій (табл. 6.2). Оскільки суглобовий хрящ не має нервових закінчень та є нечутливим до больових стимулів, біль при ОА виникає в результаті ураження позахрящових структур, таких як періост, внутрішньосуглобові зв’язки, внаслідок тиску на субхондральну кістку, венозного стазу, набряку кісткового мозку, розтягнення суглобової капсули, органічних змін у синовіальній оболонці, сухожилках та фасції, а також за наявності бурситу. До цього часу дискутабельним залишається питання щодо посилення больового синдрому у хворих на ОА при зниженні атмосферного тиску та змінах погодних умов (Wilder F.V. et al., 2003; Verges J. et al., 2004). У цілому фактори, що впливають на виникнення болю при ОА, можна розподілити на локальні, системні і фактори з боку ЦНС.
Таблиця 6.2
Фактори, що впливають на вираженість болю при ОА, і можливі причини його виникнення (за: Dieppe P.A., 1995)
| Фактори, що впливають на вираженість болю при ОА | Можливі причини виникнення болю при ОА |
|
|
Зміна контурів суглобових поверхонь, остеофітоз та інші локальні механічні фактори можуть бути причиною виникнення аномального навантаження на зв’язки, суглобову капсулу та інші структури суглоба. Подібний механізм, вірогідно, відіграє важливу роль у появі болючості періартикулярних структур і гострого болю, що виникає в суглобі під час руху.
Відомо, що при ОА підвищується внутрішньокістковий тиск у субхондральній кістці внаслідок утруднення венозного відтоку (Arnoldi C.C. et al., 1971; 1980). Зниження внутрішньокісткового тиску зменшує біль при ОА (Revell P.A. et al., 1988). Припускають, що цей механізм відповідальний за виражений больовий синдром — тривалий, що виникає вночі у стані спокою. Можливо, одним із джерел болю при ОА є періост, який потовщується в результаті появи остеофітів і хондрофітів (Kellgren J.H., 1983). Водночас доведено, що кореляційний зв’язок між інтенсивністю больового синдрому та ступенем рентгенологічних змін в результаті ОА є доволі слабким (Hannan M.T. et al., 2000). Хоча в той же час набряк кісткового мозку, що виявляється на МРТ, за даними D.T. Felson та співавторів (2001) добре корелює з інтенсивністю болю при ОА колінного суглоба, причому цей зв’язок є більш вираженим у випадку виявлення значного ступеню набряку кісткового мозку, що поєднується з дефектами суглобового хряща, які поширюються до ділянки субхондральної кістки (Sowers M.F. et al., 2003).
Помірний синовіт часто супроводжує ОА, особливо на пізніх стадіях (Dieppe P.A., 1978; Revell P.A. et al., 1988), і може сприяти посиленню болю. На користь цього механізму свідчить зменшення болю при ОА у відповідь на лікування НПЗП (Dieppe P.A. et al., 1993).
Біль, зумовлений запаленням, давно є предметом серйозної уваги, на сьогодні механізми болю, асоційованого із запаленням, активно вивчаються. Показано, що будь-який периферичний біль пов’язаний з підвищенням чутливості спеціалізованих нейронів — ноціцепторів, що створюють сигнал, який розпізнається як біль. Підвищення чутливості первинного ноціцептора в ураженій периферичній тканині призводить до підвищення активності нейронів, що посилають сигнал у спинний мозок і ЦНС, однак необхідно підкреслити, що у вогнищі запалення може генеруватися спонтанна електрична активність, що зумовлює стійкий больовий синдром. Таким потужним індуктором больової чутливості є прозапальні компоненти: брадикініни, гістамін, нейрокініни, комплемент, оксид азоту, які зазвичай виявляють у вогнищі запалення. В останні роки все більше уваги приділяють простагландинам, накопичення яких корелює з інтенсивністю запалення і гіпералгезією. Проте власне простагландини не є медіаторами болю, вони лише підвищують чутливість ноціцепторів до різних стимулів. Вони ніби включають нормальні (мовчазні) ноціцептори, призводячи до такого стану, коли вони легко збуджуються при різному впливі.
Порушення біомеханіки в ураженому суглобі сприяє розвитку вторинних періартикулярних синдромів — бурситів, теносиновітів та ін. Під час збирання анамнезу та огляді хворого на ОА необхідно визначити, чим зумовлений біль — безпосередньо ураженням суглоба або запаленням, що локалізується в суглобових сумках і синовіальних піхвах.
Хворі на ОА нерідко скаржаться на біль в навколосуглобових м’язах при пальпації. Припускають, що слабкість м’язів, що здійснюють рух у суглобі, може бути однією із причин болю. На користь цього свідчить зменшення болю у пацієнтів з гонартрозом, що виконують вправи на зміцнення чотириголового м’яза стегна (Chamberiain M.A. et al., 1982).
J.H. Kellgren (1939) вказував на спрямованість болю і болючості при пальпації від уражених суглобів до м’язів, що здійснюють рух у суглобах. Це явище може пояснити часте виникнення болю у м’язах поруч з ураженим суглобом.
Хворі на ОА можуть мати ознаки фіброміалгії (Mologofsky H., 1989). Крім того, M.N. Summers та співавтори (1988) вказують на важливість центральних нейрогенних механізмів у генезі болю при ОА.
Скутість. Відчуття скутості в суглобах — часта скарга хворих. Скутість зазвичай характеризується утрудненням перших рухів, феноменом «замороженого» суглоба після періоду спокою, обмеженням обсягу рухів в ураженому суглобі. Скутість при ОА, як правило, триває кілька хвилин (рідко до 30 хв) і виникає тільки в ураженому суглобі.
Причина виникнення скутості при ОА залишається невідомою. Скарги на «замороженість» суглоба після періоду спокою можна пояснити простими механічними причинами (потовщення суглобової капсули та ін.). Тривала (до 30 хв) ранкова скутість, що спостерігається у деяких хворих на ОА, можливо, виникає внаслідок розвитку синовіту (за аналогією з ранковою скутістю при РА).
Обмеження обсягу рухів — часта скарга хворих на ОА. Воно зазвичай супроводжується скаргами на біль при рухах у суглобі, причому максимум болю відзначається на висоті обмеженого руху. Хондрофітоз і остеофітоз, ремоделювання суглоба, потовщення суглобової капсули сприяють обмеженню обсягу рухів у суглобі, ураженому ОА. Останнє може також пояснити утруднення виконання доступного обсягу руху в ураженому суглобі.
Щільні потовщення суглобових країв часто добре пальпуються і можуть бути болючими. Поряд із грубими крепітаціями, які відчуваються при рухах в уражених суглобах, щільні потовщення суглобових країв є важливою диференційно-діагностичною ознакою ОА (Altman R.D. et al., 1986). Крепітації виявляють при пальпаторному дослідженні ураженого суглоба, на пізніх стадіях ОА їх можна почути на відстані. Доведено, що виявлення крепітації у пателофеморальному, великогомілковому та стегнових виростках навколо колінного суглоба корелює зі ступенем дегенеративних змін, що виявляються при артроскопії (Ike R.W. et al., 1995). Імовірною причиною виникнення крепітації при ОА поряд з утворенням газових пухирців у синовіальній рідині, які лопаються при рухах у суглобі, є шорсткість суглобових поверхонь ураженого суглоба (Watson P. et al., 1989). Необхідно диференціювати крепітації і відчуття грубого хрускоту при рухах у нормальних суглобах. Останній, як правило, завжди чути на відстані, він являє собою один або кілька непостійних окремих звукових феноменів під час руху в суглобі. Крепітації відчуваються (іноді їх можна почути) в суглобах постійно під час руху в суглобі.
Утворення щільних (кісткових) потовщень по краю суглобової щілини найбільш характерне для ОА кистей: вузлуватість проксимальних міжфалангових суглобів називається вузлами Бушара, а дистальних міжфалангових суглобів — вузли Гебердена. Рідше щільні потовщення виявляють по краю суглобових щілин інших суглобів, зокрема колінних.
Крепітації є одією із основних диференційно-діагностичних ознак ОА. Крепітації при ОА необхідно диференціювати із хрускотом у суглобі здорової людини, причиною якого можуть бути газові пухирці в синовіальній рідині, які лопаються при рухах.
Синовіт. Найчастіше синовіт при ОА виникає в колінних суглобах. У пацієнтів із синовітом змінюється характер болю: він виникає в ряді випадків відразу ж після опори на ногу і при звичайній (не тривалій) ході. Такий «стартовий» біль не зникає повністю у стані спокою, а у частини хворих набуває невизначеного ритму (хворий не може чітко визначити час його найвищої інтенсивності). Синовіт при гонартрозі може бути субклінічним, слабким, помірним, значним (табл. 6.3); за поширеністю — обмеженим і дифузним; залежно від перебігу — первинним, рецидивуючим і часто рецидивующим.
Таблиця 6.3
Клінічні прояви синовіту (за: Астапенко М.Г. и соавт., 1984)
| Симптоми синовіту | Синовіт | |||
| Субклінічний | Слабкий | Помірний | Значний | |
| Біль | ||||
| інтенсивність | Дуже слабка | Невелика | Помірна | Сильна |
| час виникнення | Тільки при спуску сходами | Тільки при тривалій ході, у спокої зникає | При ході, у спокої не зникає відразу | При опорі на ногу |
| Підвищення температури шкіри над суглобом | ||||
| інтенсивність | Дуже слабка | Слабка | Помітна | Помірна |
| локалізація | На обмеженій ділянці внутрішньої поверхні | По всій внутрішній поверхні | На внутрішній і зовнішній поверхні | Над усім суглобом |
| Болючість | ||||
| інтенсивність | — | Слабка | Помітна | Помірна |
| локалізація | — | По внутрішній поверхні | По всій суглобовій щілині | Уся поверхня суглоба |
| Припухлість | ||||
| інтенсивність | — | Слабка | Помітна | Помірна |
| локалізація | — | У ділянці внутрішньої поверхні суглоба | На внутрішній поверхні і у препателярній ділянці | Увесь суглоб |
| Випіт | — | — | Підозра на випіт | Невеликий випіт |
Cиновіт при ОА має не тільки діагностичне, але й патогенетичне значення. Виявлення прозапальних медіаторів у синовіальній рідині хворих на ОА, у тому числі й на ранній стадії, призвело до перегляду існуючої раніше концепції патогенезу захворювання як «неминучого результату процесу старіння суглобів». У середині 90-х років ХХ ст. формула патогенезу ОА «дегенерація — первинна, запалення — вторинне» змінилася з точністю до навпаки. На сьогодні, незважаючи на активні пошуки в цьому напрямку, довести первинність запалення так і не вдалося, тому ідеї «первинності» запалення в патогенезі ОА висловлюються все менш активно. З іншого боку, майже всі без винятку дослідники однозначно схиляються до однієї думки: запалення відіграє важливу роль у прогресуванні захворювання. Так, ще в 1984 р. М. Г. Астапенко та співавтори продемонстрували виражений кореляційний зв’язок синовіту (що оцінювався клінічно за власним методом авторів і сцинтиграфічно з 99m Tc). M. Takahashi та співавтори (2004) виявили статистично значимий негативний кореляційний зв’язок між висотою рентгенологічної суглобової щілини і маркером запалення піридиноліном у сечі хворих на ОА (р = 0,034), а також між ступенем рентгенологічних змін за класифікацією Келлгрена — Лоуренса і піридиноліном у сечі (р = 0,039) і ТІМП-1 (р = 0,017) у крові хворих на ОА. Крім того, автори виявили, що у пацієнток з генералізованою формою ОА С-реактивний білок (СРБ) (кількісно), піридинолін, глікопротеїн хряща-39 (YKL-40) і ТІМП-1 були значно вищими, ніж у хворих з негенералізованим ОА.
Остаточно нез’ясованим залишається питання про існування системного запалення при ОА. Результати численних досліджень свідчать про наявність маркерів системного запалення у хворих на ОА. Прихильники концепції пояснюють цей феномен системною стимуляцією прозапальних цитокінів, що продукуються локально, в тому числі індукування ними синтезу реактантів гострої фази в печінці.
Так, F. Wolfe (1997) виявив у 572 пацієнтів з гонартрозом і коксартрозом підвищення рівня СРБ у сироватці крові (5,9 мкг/мл при нормі менше 0,8 мкг/мл). Також автор відзначив незначний, але значимий зв’язок між рівнем СРБ у хворих на ОА і функціональною неспроможністю, болючістю суглобів, болем, слабкістю, тяжкістю загального стану і депресією, а також з ІМТ і жіночою статтю. Найбільш виражений зв’язок був з рівнем СРБ за даними HAQ (опитувальник стану здоров’я (Health Assessment Qustionary)). Водночас автор дослідження повідомив про відсутність будь-якого зв’язку між ШОЕ і клінічними симптомами ОА, за винятком слабкої кореляції з даними HAQ.
За даними L.D. Loose та співавторів (1993) рівень СРБ у 365 хворих на ОА становив 5 мкг/мл, у той час як у контрольній групі здорових осіб — 1,9 мкг/мл). У цьому дослідженні лікування хворих НПЗП призвело до значного зниження СРБ у сироватці крові, що супроводжувалося клінічним покращанням.
T.D. Spector та співавтори (1997) визначали рівень СРБ у сироватці крові 105 жінок з ОА (≥ІІ стадії за класифікацією Келлгрена — Лоуренса) і 740 здорових осіб, що брали участь у популяційному дослідженні. Виявилося, що у жінок з ОА рівень СРБ був значно вищим (2,4 мкг/мл), ніж у контрольній групі (0,7 мкг/мл). Повторна рентгенографія колінних суглобів виконана 70 жінкам з ОА із 105 через 4 роки після вихідного обстеження. Виявлено, що у 32 жінок з ознаками прогресування хвороби за 4 роки вихідний рівень СРБ був значно вищим, ніж у таких без ознак прогресування на рентгенограмах (2,6 vs 1,3 мкг/мл відповідно). Водночас біль у колінному суглобі не впливав на рівень СРБ у сироватці крові. Автори дослідження припустили, що рівень СРБ у сироватці крові можна вважати прогностичним фактором прогресування хвороби. Аналогічні результати одержали T. Сonrozier та співавтори (1998), що виявили значно вищий рівень СРБ у хворих зі швидко прогресуючим ОА (5,61 vs 1,94 мкг/мл).
Контраргументи супротивників концепції системного запалення при ОА ґрунтуються на неспецифічності використовуваних маркерів системного запалення і неадекватному трактуванню результатів досліджень (більш докладно див. главу 9).
Останнім часом у літературі з’явилися повідомлення про виявлення ділянок панусоподібної фіброзної тканини на поверхні уражених суглобів (Shibakawa A., et al., 2003; Yuan G.-H., et al., 2004). Про схожі знахідки повідомляли і більше 30 років тому, однак ці зміни трактували як феномен ремоделювання (Meaсhim G., et al., 1970; Meaсhim g., 1972; Nakata K., et al., 1982). На сьогодні відомо, що панус ― інвазивна грануляційна тканина, що покриває суглобові поверхні суглобів, уражених РА, і викликає їх деструкцію (Bresnihan B., 1999). Нещодавно A. Shibakawa та співавтори (2003) повідомили, що 80% зразків суглобових тканин, одержаних у хворих на ОА, містили панусоподібну тканину з катаболічними властивостями.
За даними G.-H. Yuan і співавторів (2004) у 15 суглобах з 21 (71,4%), ураженого ОА, була макроскопічно виявлена панусоподібна тканина. Але лише в 5 з них тканини було досить для того, щоб виділити її для гістологічного дослідження. На відміну від пануса при РА, що дифузно покриває всю суглобову поверхню з ділянками локальних крововиливів та інвазії в прилеглі тверді тканини, панусоподібна тканина розміщується лише маленькими ділянками на периферії або в центрі суглобової поверхні. Крім того, на відміну від пануса при РА, що характеризується гіперваскуляризацією та інфільтрацією запальними клітинами, а також містить лімфатичні фолікули, панусоподібна тканина при ОА васкуляризирована у значно меншому ступені.
A. Shibakawa та співавтори (2003) виділили два типи панусоподібної тканини: фіброзний і судинний. Крім того, панусоподібна тканина не містить CD68-лімфоцитів, якими інфільтрований панус у пацієнтів з РА, а її товщина може досягати 5 мм (Yuan G.-H. et al., 2004).
У результаті гістохімічного дослідження панусоподібної тканини було виявлено експресію генів маркера фібробластів колагену I типу, а також агрекану і колагену II типу, що свідчить про загальні властивості панусоподібної тканини з хондроцитами. На підставі даних гістохімічних досліджень G.-H. Yuan та співавтори (2004) припустили, що можливими попередниками панусоподібної тканини можуть бути: синовіальна тканина, хрящова тканина (змінена в результаті фіброзної метаплазії), субартикулярні мезенхімальні клітини (тільки клітини панусоподібної тканини при ОА експресують віментин — маркер мезенхіальних клітин). У хворих з ОА клітини панусоподібної тканини продукують ММП-1; -3 і -13 у значно більшій кількості, ніж хондроцити. З дією цих ферментів пов’язують інвазивні властивості панусоподібної тканини і деградацію тканин суглобів.
На думку G.-H. Yuan та співавторів (2004) дефекти суглобового хряща можуть заміщатися фіброзною тканиною з метою подальшої репарації, але несприятливі умови (наприклад неадекватне тривале навантаження на суглоб, мікротравми, дія цитокінів тощо) можуть затримати процес репарації і перемкнути на катаболічні процеси. Експресія протеогліканів і колагену ІІ типу клітинами панусоподібної тканини свідчить про можливу її репаративну дію у певних умовах.
Рідко синовіт виникає в проксимальних і дистальних міжфалангових суглобах кистей за наявністю вузлів Гебердена та/або Бушара (проявляється болючістю, припухлістю, гіперемією суглобів), що вимагає диференціальної діагностики з РА (Huskisson E.C. et al., 1979).
Ознаки деструкції суглобів. На пізніх стадіях ОА виявляють ознаки деструкції хряща, кістки і навколишніх м’яких тканин: варусна деформація колінних суглобів (у зв’язку з ураженням медіальної тибіофеморальної частини суглоба), слабкість зв’язкового апарату, нестабільність суглобів (часто розвивається в дистальних міжфалангових суглобах). Деструкція кісткової тканини при ОА кульшового суглоба може призвести до вкорочення кінцівки.
Перебіг ОА різних локалізацій відрізняється один від одного. Загалом захворювання прогресує повільно. Перебіг ОА у більшості пацієнтів відбувається у вигляді періодів загострення (можуть тривати дні/місяці), коли біль особливо інтенсивний, значно порушена функція уражених суглобів і може з’являтися суглобовий випіт, і періодів відносної ремісії, коли біль відсутній або слабко виражений, уражені суглоби функціонують у повному обсязі або їх функція незначно знижена і відсутній випіт (Dieppe P.A., 1995). У деяких хворих з діагностованим ОА протягом місяців і навіть років можуть не бути ніяких скарг (Massardo L. et al., 1989).
Найбільш швидке прогресування ОА спостерігається в суглобах кистей, найбільш повільне — у колінних суглобах, ураження тазостегнових суглобів займає проміжне положення. Швидке прогресування, що означає зміну клінічних симптомів і рентгенологічних ознак протягом короткого часу, що вимірюється місяцями, виявляють лише у невеликої кількості пацієнтів (Siefert M.H. et al., 1969). Деструкція кісткової тканини характерна для жінок похилого віку (Dieppe P.A. et al., 1984). Для ОА суглобів кистей і кульшових суглобів описане явище зворотного розвитку не тільки клінічних симптомів, але й рентгенологічних ознак (Perry G.H. et al., 1979; Bland J.H., Cooper S.M., 1984). Рентгенологічні ознаки змін анатомії суглобів не завжди корелюють зі змінами клінічних симптомів ОА і непрацездатністю хворих (Danielsson L.G., 1964; Dieppe P.A., Cushnaghan J., 1991).
Фактори, які можуть впливати на результат ОА (за: Felson D.T., 1988):
- вік на початку захворювання, раса і стать;
- ожиріння та інші фактори, з якими пов’язаний ОА;
- надмірне використання відповідних суглобів;
- ступінь розвиненості навколосуглобових м’язів та іннервація;
- стабільність суглоба;
- реакція кісткової та синовіальної тканини;
- відкладання кристалів;
- психологічні та соціальні фактори;
- медикаментозна та інша терапія.
ОА — захворювання, що не має системних проявів, тому ускладнення завжди пов’язані з ураженим суглобом/суглобами. Локальні ускладнення включають розвиток вторинних періартикулярних синдромів (бурсит, тендовагініт та ін.), тунельних синдромів, зумовлених утворенням значних остеофітів або деформацією суглобів. Тяжкі деформації уражених суглобів можуть бути причиною вторинних переломів та асептичного некрозу кісток (Bauer G.C.H., 1978).
ОСОБЛИВОСТІ ОСТЕОАРТРОЗУ РІЗНИХ ЛОКАЛІЗАЦІЙ
Найбільш часто первинним ОА уражуються суглобові групи, які несуть найбільшу статичну (колінні, кульшові, апофізарні суглоби хребта) і динамічну (проксимальні й дистальні міжфалангові суглоби кистей) навантаження. Клінічні прояви ОА значно відрізняються залежно від локалізації ураження (табл. 6.4).
Таблиця 6.4
Клінічні ознаки та симптоми, характерні для суглобів, що найчастіше уражаються ОА (Moskowitz R.W. et al., 2007)
| Локалізація | Симптоми |
| Для всіх | Біль, скутість (відчуття «гелю»), крепітація, збільшення кістки, обмеження обсягу рухів, деформація суглоба |
| Суглоби кистей | Дистальні міжфалангові (вузлики Гебердена), проксимальні міжфалангові (вузлики Бушара), медіальна або латеральна девіація дистальних та проксимальних міжфалангових суглобів; квадратизація основи кисті |
| Колінні суглоби | Симптоми з боку пателофеморального суглоба погіршуються при спуску по сходах порівняно з рівною поверхнею; у випадку ураження медіального відділу суглоба характерна варусна деформація; при ураженні латерального відділу суглоба — вальгусна деформація; характерними є утворення підколінних кист (кист Бейкера) та болючість сумки «гусячої лапки» |
| Кульшовий суглоб | Типовим є біль у паху, але також може бути присутній біль у сідничній ділянці; менш характерною локалізацією є біль у колінному суглобі та нижче нього; можуть бути присутні згинальні контрактури та симптом Тренделенбурга |
| Шийний відділ хребта | Локальний біль у хребті; спазм м’язів; обмеження обсягу рухів (латерального згинання та розгинання); характерним є радикулярний біль; втрата чутливості та м’язова слабкість/атрофія у ділянці іннервації корінця; шийна мієлопатія, що характеризується слабкістю у нижніх кінцівках, порушення функції сечового міхура, гіперактивністю рефлексів на нижніх кінцівках |
| Поперековий відділ хребта | Локальний біль та спазм м’язів; обмеження розгинання; біль у сідничній ділянці; погіршення стану у другій половині дня, але не вночі; ураження певної корінцевої ділянки з болем, чутливими та руховими змінами у зоні іннервації; у випадку стенозу поперекового відділу спинного мозку; типовим є виникнення болю у спині/нижніх кінцівках при стоянні, ходьбі та полегшення стану при сидінні |
ОА колінного суглоба (гонартроз). Колінний суглоб складається із трьох анатомічних частин (компартментів): великогомілково-стегнового (тибіофеморального (ТФВ)) відділу, що має медіальну та латеральну ділянки, і надколінниково-стегнового (пателофеморального (ПФВ)) відділу. Кожна із цих ділянок може бути окремо уражена ОА або можлива будь-яка комбінація уражень (Ahlback S., 1969). Найбільш часто відзначають ізольований ОА в медіальному ТФВ та комбіноване ураження медіального ТФВ і ПФВ.
У середньому медіальний ТФВ уражується в 75%, латеральний ТФВ — в 26%, а ПФВ — в 48% випадків (Mcalindon T.E. et al., 1993).
Втрата суглобового хряща зазвичай найбільш виражена в латеральному ПФВ і на суглобовій поверхні великогомілкової кістки в ТФВ, на ділянці, найменш покритій менісками. За даними артроскопії і МРТ поряд з ураженням суглобового хряща при гонартрозі уражуються меніски (Mcalindon T.E. et al., 1991). Остеофітоз найбільш виражений у латеральному тибіофеморальному компартменті, в той час як максимальну деструкцію хряща зазвичай виявляють у медіальному.
Біомеханіка колінного суглоба добре вивчена (Maquet P.G.J., 1976). У нормальному суглобі вісь навантаження проходить через центр ТФВ. Однак при рухах, коли навантаження на ТФВ в 2–3 рази перевищує масу тіла, максимум навантаження припадає на медіальну частину зчленування; при згинанні колінного суглоба навантаження на пателофеморальну його частину в 7–8 раз перевищує масу тіла. Можливо, цим пояснюється висока частота ураження саме медіального ТФВ і ПФВ колінного суглоба (Cooke T.D.V., 1985). Розвитку гонартрозу сприяють деякі фізіологічні аномалії колінного суглоба — фізіологічний genu varum, гіпермобільність суглоба та ін. Меніскектомія і ушкодження зв’язкового апарату порушують нормальний розподіл навантаження на колінний суглоб, що є фактором, який підвищує схильність до розвитку вторинного гонартрозу.
Хворих на ОА колінного суглоба можна розподілити на дві групи (Cobb S. et al., 1957). До першої групи належать пацієнти молодого віку, частіше чоловіки, з ізольованим ураженням одного, рідше обох колінних суглобів, що мають в анамнезі дані про травму або операцію (наприклад меніскектомію) на колінному суглобі (Bagge E. et al., 1991). До другої групи належать особи середнього і похилого віку, переважно жінки, у яких відзначають ОА одночасно інших локалізацій, включаючи кисті рук (Cushnaghan J., Dieppe P.A., 1991); багато пацієнтів цієї групи мають ожиріння (Felson D.T., 1988).
Найбільш важливими симптомами гонартрозу є біль у суглобі при ходьбі, тривалому перебуванні у стоячому положенні і спуску по сходах; хрускіт у суглобах при рухах; локальна болючість при пальпації, в основному у медіальній частині суглоба за ходом суглобової щілини; обмеження згинання внаслідок болючості, а пізніше й розгинання суглоба, крайові кісткові розростання, атрофія чотириголового м’яза стегна. Ураження медіального відділу колінного суглоба призводить до розвитку варусної деформації. Ураження латеральної частини тибіофеморального суглоба, що рідко відзначають, може викликати формування вальгусної деформації. При будь-якому типі ураження ОА колінного суглоба часто виявляють ознаки запалення. При цьому змінюється характер болю: біль посилюється, з’являються «стартовий» біль, біль у спокої, ранкова скутість у суглобі тривалістю до 30 хв. У ділянці суглоба з’являються невелика припухлість, місцеве підвищення температури шкіри. Внаслідок наявності в порожнині суглоба кісткового або хрящового відломка («суглобової миші») у хворого з гонартрозом можуть виникати симптоми блокади суглоба (гострий біль у суглобі, що позбавляє хворого можливості зробити будь-який рух). Частою ознакою ОА колінного суглоба є виникнення підколінних кіст (кіст Бейкера) — сумки, що з’єднана з порожниною суглоба. При накопиченні синовіальної рідини зазначені кісти можуть досягати великих розмірів та ставати причиною відчуття болю по задній поверхні колінного суглоба. Порушення їх цілісності, прорив у ділянку литкового м’язу може викликати судинну компресію та імітувати симптоми тромбозу глибоких вен, включаючи типовий набряк та симптом Гоманса (болючість литкових м’язів при пальпації та максимальному тильному згинанні стоп) (Curl W.W., 1996).
Важливим при наявності скарг на біль у колінному суглобі є огляд суміжного кульшового суглоба, оскільки біль може носити іррадіюючий характер за умови органічних змін у іншій ділянці.
Фактори, асоційовані з прогресуванням гонартрозу (за: Dieppe P.A., 1995):
- похилий вік;
- жіноча стать;
- надмірна маса тіла;
- генералізований ОА (вузли Гебердена);
- дієта з недостатньою кількістю антиоксидантів;
- дієта з недостатнім вмістом вітаміну D/низький рівень вітаміну D у плазмі крові.
Перебіг ОА колінного суглоба тривалий, хронічний, прогресуючий, з повільним наростанням симптомів, частіше без різко виражених загострень. У частини хворих гонартроз може мати стабільний перебіг як клінічно, так і рентгенологічно протягом багатьох років (Miller R. et al., 1973; Massardo L. et al., 1989). Періодично може виникати спонтанне зменшення вираженості симптомів. На відміну від коксартрозу і ОА суглобів кистей спонтанне покращання (зворотний розвиток) рентгенологічних ознак ОА виникає вкрай рідко (Dieppe P.A., 1995). ОА найчастіше має перебіг з періодами загострення, які зазвичай супроводжуються появою випоту в порожнину суглоба і тривають дні/місяці, і покращання або ремісії. У деяких випадках погіршення перебігу захворювання відбувається протягом декількох тижнів або місяців. Це може бути пов’язане з розвитком нестабільності суглоба або деструкцією субхондральної кістки. Раптовий, майже миттєвий біль у колінному суглобі може означати розвиток асептичного некрозу медіального епіфіза стегнової кістки — рідкісного, але тяжкого ускладнення ОА.
Остеоартроз кульшового суглоба (коксартроз). Найчастіше ОА уражує верхній полюс кульшового суглоба з верхньолатеральним зміщенням голівки стегнової кістки (близько 60% пацієнтів з коксартрозом, чоловіки хворіють частіше, ніж жінки). Рідше відзначають ураження медіального полюса суглоба з медіальним зміщенням голівки стегнової кістки і протрузією вертлужної западини (близько 25% пацієнтів з коксартрозом, жінки хворіють частіше, ніж чоловіки) (Solomon L., 1976). Концентричне ураження, при якому уражується весь суглоб, — варіант коксартрозу, що відзначають найрідше (близько 15% пацієнтів з коксартрозом, жінки хворіють частіше, ніж чоловіки) (Marks J.S. et al., 1979). Дуже рідко виявляють ураження задньонижньої частини суглоба, яке можна виявити тільки на рентгенівському знімку в бічній проекції.
Рентгенологічно можна виділити два типи остеоартрозу кульшового суглоба: гіпертрофічний, при якому переважають ознаки підвищеної репаративної відповіді (остеофіти, субхондральний склероз), і атрофічний, при якому ознаки підвищеної репаративної відповіді не виражені (Solomon L. et al., 1982). Деякі автори описують особливу форму швидко прогресуючого ОА, при якому звуження суглобової щілини відбувається протягом декількох місяців (Edelman J., Owth E.J., 1981).
Дослідження біомеханіки суглоба продемонструвало, що навантаження, яке припадає на кульшовий суглоб, складається з навантаження маси тіла і сил, що приводять стегно (Radin E.L., 1980). Верхній полюс суглоба — зона, через яку проходить вісь навантаження маси тіла, тому верхній полюс — найбільш вразлива ділянка.
За нашим даними (обстежено 54 пацієнта з коксартрозом і 40 осіб без патології з боку опорно-рухового апарату, групи були порівняні за віком і статтю), зменшення обсягу рухів у кульшовому суглобі асоціювалося з тяжкістю клініко-рентгенологічної стадії захворювання (табл. 6.5). Проте не всі види рухів були пов’язані з прогресуванням коксартрозу: так, найбільша кореляція була відзначена для згинання (r=–0,84), відведення і внутрішньої ротації стегна (r=–0,69 і r=–0,67 відповідно), більш слабка кореляція — для зовнішньої ротації (r=–0,40); не виявлено корелятивного зв’язку для приведення.
Таблиця 6.5
Розподіл хворих на коксартроз і осіб контрольної групи за клінічними ознаками залежно від рентгенологічної стадії
| Показник | Хворі на коксартроз (n=54) | Контрольна група (n=40) | ||||
| Рентгенологічна стадія | ||||||
| 0 | I | II | III | IV | 0 | |
| Кількість обстежених | 12 | 13 | 15 | 10 | 4 | 40 |
| Клінічна симптоматика є/відсутня | 6/6 | 11/2 | 15/0 | 10/0 | 4/0 | 0/40 |
| Біль (за візуальною аналоговою шкалою (ВАШ)), см | 1,3±2,4 | 2,84±3,10 | 3,6±2,5 | 5,7±2,9 | 6,2±4,7 | 0 |
| Індекс Lequesne, бали | 3,6±2,8 | 6,4±4,2 | 7,1±3,8 | 14,0±5,5 | 16,3±6,9 | 0 |
| Обсяг рухів у суглобі (°): | ||||||
| — згинання | 125,4±3,6 | 123,7±2,9 | 122,5±4,1 | 117,6±6,9* | 111,2±8,8* | 126,2±4,7 |
| — відведення | 47,8±9,2 | 45,0±6,9 | 41,5±8,2* | 38,1±11,1* | 35,4±4,8* | 46,7±5,8 |
| — внутрішня ротація | 44,6±4,4 | 41,7±5,2 | 39,2±6,5* | 33,3±7,1* | 30,9±6,2* | 45,1±3,6 |
| — зовнішня ротація | 48,8±3,8 | 45,6±6,9 | 44,1±4,8 | 42,3±5,5* | 37,4±4,2* | 47,6±4,2 |
*Відмінність показників статистично вірогідна порівняно з контрольною групою.
Отже, зменшення обсягу рухів у кульшовому суглобі (згинання, відведення і внутрішня ротація стегна) значно корелює з тяжкістю рентгенологічної стадії коксартрозу.
На пізніх стадіях коксартрозу виявляють значні зміни синовіальної оболонки і потовщення суглобової капсули (Byers P.D. et al., 1970). Дослідження матеріалу, одержаного під час артропластики кульшового суглоба, свідчить про те, що при коксартрозі часто є невеликі зони асептичного некрозу голівки стегнової кістки (Dieppe P.A., 1995).
Коксартроз зазвичай уражує осіб віком 40–60 років. Основними факторами, що підвищують схильність до розвитку ОА кульшового суглоба є його вроджена дисплазія, хвороба Пертеса, аномалії довжини нижньої кінцівки, дисплазія вертлужної западини (Harris W., 1986). Однобічне ураження суглоба відзначають набагато частіше, ніж двобічне.
Основний симптом остеоартрозу кульшового суглоба — біль при ході та опорі на ногу в стегні, сідниці, паху, іноді тільки в колінному суглобі значно утруднює діагностику і зумовлений іррадіцією болю вздовж замикального нерва суглоба, ураженого ОА (Khan A.M. et al., 2004). Хворих турбують скутість в ураженому суглобі після періоду спокою; болюче зменшення обсягу рухів, причому першим зменшується обсяг внутрішньої, а потім зовнішньої ротації і кут відведення ноги. Зменшується функціональна здатність хворого: важко, нагнувшись, надягти панчохи, взуття, підняти що-небудь із підлоги. У найбільш важких випадках можна почути (але не пропальпувати) крепітації при рухах у суглобі. Болючість над латеральною поверхнею суглоба може бути зумовлена вторинним вертельним бурситом. На пізніх стадіях коксартрозу з’являється кульгавість у зв’язку з вкороченням ноги внаслідок міграції голівки стегнової кістки, а при двобічному ураженні — «качина хода». Розвивається атрофія м’язів стегна й сідниці, з’являються характерні анталгічна (коксалгічна) хода і так звана ознака Тренделенбурга: при спробі хворого спертися на уражену кінцівку опускається таз (Brown M.D. et al., 2007).
Коксартроз — найбільш тяжка форма остеоартрозу. Перебіг коксартрозу — хронічний, прогресуючий. Швидкість прогресування захворювання варіює. У більшості випадків пацієнти, які потребують хірургічного лікування, мають відносно короткий анамнез — від 3 до 36 міс (Dieppe P.A., 1995). При швидко прогресуючому перебігу коксартрозу протягом декількох років наступає повна інвалідізація хворого, особливо при двобічному ураженні. За даними L.G. Danielsson (1964) у частини обстежених хворих стан залишався стабільним протягом 10 років і більше. Для концентричного ураження кульшового суглоба і гіпертрофічного варіанта коксартрозу характерний більш сприятливий прогноз (Rueble M., Dubois J.L., 1981). Для коксартрозу описані випадки спонтанного зворотного розвитку хвороби у випадку, якщо хірургічне лікування було відкладене (Dieppe P.A., 1995).
Найбільш часте ускладнення коксартрозу — деструкція кісткової тканини. До інших ускладнень остеоартрозу кульшового суглоба належать асептичний некроз голівки стегнової кістки, протрузія вертлужної западини, руйнування кист ділянки вертлужної западини. У деяких випадках швидко прогресуючий коксартроз може призвести до незвичайної картини — виражена деструкція кісткової тканини і широка суглобова щілина. Такий варіант коксартрозу називають «анальгетичним кульшовим суглобом», оскільки пов’язують з прийомом знеболювальних препаратів. Однак він може розвиватися і в пацієнтів, які не приймають взагалі або приймають досить мало анальгетиків і НПЗП (Rashad S. et al., 1989).
Коксартроз може виникати вторинно на фоні контралатерального або іпсілатерального гонартрозу (Dixon A.S.J., Campbell-Smith S., 1969). Серед ускладнень з боку періартикулярних структур найчастіше розвивається трохантеричний бурсит.
Остеоартроз суглобів кистей. На жаль, остеоартроз суглобів кистей не так детально вивчений, як гонартроз і коксартроз. Імовірно, це пов’язано з відносним доброякісним перебігом ОА цієї локалізації.
ОА переважно вражає дистальні (~70% хворих на ОА кистей), рідше — проксимальні (~35% хворих на ОА суглобів кистей) міжфалангові суглоби і зап’ястково-п’ястковий суглоб великого пальця (~60% жінок і ~40% чоловіків з ОА кистей). П’ястно-фалангові суглоби і променезап’ястковий суглоб уражуються рідко (у жінок ~10 і 5%, у чоловіків ~20 і 20% відповідно). ОА кистей уражає жінок в 4 рази (за іншим даними в 10 раз) частіше, ніж чоловіків (Swanson A.B., Swanson G.G., 1985). На думку E.L. Radin і співавторів (1971), вищеописаний розподіл частоти ураження суглобів кистей можна пояснити розподілом навантаження на них — максимальне навантаження припадає на дистальні міжфалангові суглоби. Частота ураження суглобів кистей у хворих на ОА є дзеркальним відбиттям такої при ревматоїдному артриті (Swanson A.B., Swanson G.G., 1985). Так, збільшення кісток у ділянці дистальних та проксимальних міжфалангових суглобів (вузлики Бушара та Гебердена) прийнято розгдядати як симптоми вузликового ОА. Доведеною є спадкова схильність до вузликового ОА кистей. Так, у сестер жінок, що страждають на вузликовий ОА, ймовірність виникнення аналогічного стану є втричі вищою (Spector T.D. et al., 1996).
ОА кистей зазвичай починається в середньому віці, частіше у жінок у клімактеричний період (Acheson R.M. et al., 1970; Spector T.D., Campion G.D., 1989), при цьому типовим є підгострий перебіг патологічного процесу протягом декількох років (Moskowitz R.W. et al., 2007). Нерідко ОА кистей, асоційований з гонартрозом і ожирінням (особливо ізольований ОА зап’ястково-п’ясткового суглоба великого пальця і міжфалангових суглобів). Ізольовані артрози окремих дрібних суглобів кистей (за винятком зап’ястково-п’ясткового суглоба I пальця), а також ізольований артроз променезап’ясткового суглоба зазвичай вторинні (наприклад ОА променезап’ясткового суглоба після перенесеної хвороби Кінбека (асептичний некроз луноподібної кістки) або посттравматичний ОА).
Відмінною ознакою ОА міжфалангових суглобів кистей є вузлики Гебердена (дистальні міжфалангові суглоби) і Бушара (проксимальні міжфалангові суглоби). Вони являють собою щільні вузлуваті потовщення переважно на верхньолатеральній поверхні суглобів. Вузли болючі, часто ускладнюються вторинним синовітом, при якому можуть з’являтися невелика припухлість м’яких тканин, локальне підвищення температури шкіри, іноді гіперемія шкіри над суглобом, що супроводжується посиленням інтенсивності больового синдрому. Хворі на ОА міжфалангових суглобів частіше, ніж хворі з іншою локалізацією, скаржаться на скутість тривалістю до 30 хв в уражених суглобах вранці і після періоду спокою. На ранніх стадіях ОА міжфалангових суглобів кистей над суглобами можуть утворюватися кисти, які іноді спонтанно розкриваються з вивільненням в’язкого безбарвного желеподібного вмісту, багатого на гіалуронову кислоту. На пізніх стадіях ОА міжфалангових суглобів може виникнути їх нестабільність, зменшення обсягу згинання, а також зниження функціональної здатності суглобів, яка проявляється утрудненням при виконанні дрібної роботи, тонких рухів (Pattrick M. et al., 1989).
Пацієнтів з ізольованим ОА зап’ястково-п’ясткового суглоба І пальця турбує біль в області основи І п’ясткової кістки. Рідко хворий може скаржитися на невизначений біль «десь у променезап’ясковому суглобі». Гіпермобільність є фактором ризику розвитку ОА І зап’ястково-п’ясткового суглоба (Jonsson H. et al., 1996). Частою скаргою хворих при ОА зап’ястково-п’ясткового суглоба І пальца є утруднення при складанні пальців у щепіть. Пальпація суглоба болюча, іноді можна чути й пальпаторно відчувати крепітації при рухах у суглобі. У тяжких випадках дегенеративні зміни зап’ястково-п’ясткового суглоба І пальця супроводжуються приведенням п’ясткової кістки та атрофією прилеглих м’язів, що веде до формування «квадратної кисті». ОА зап’ястково-п’ясткового суглоба І пальця кисті також може ускладнюватися вторинним синовітом, що супроводжується посиленням болю, припухлістю м’яких тканин, гіперемією і підвищенням локальної температури шкіри над суглобом. Ураження ОА зап’ястково-п’ясткового суглоба І пальця у більшості випадків супроводжується інтенсивним больовим синдромом та значно більшою обмеженістю функції кисті порівняно з ураженням дистальних чи проксимальних міжфалангових суглобів кисті (Moskowitz R.W. et al., 2007).
У тяжких випадках ОА суглобів кистей рентгенологічно виявляють не тільки характерні для ОА ознаки (звуження суглобової щілини, склероз субхондральної кістки, остеофітоз, субхондральні кисти), але й переривчастий характер білої кортикальної лінії. Такий ОА називають ерозивним (Utsinger P.D. et al., 1978). Для ерозивної (безвузликової) форми ОА кистей характерно рецидивування синовітів. Особливістю клінічної картини ерозивного ОА суглобів кистей є ураження не тільки проксимальних і дистальних міжфалангових суглобів і зап’ястково-п’ясткового суглоба I пальця кисті, але й залучення першого (частіше), другого і третього (рідше) п’ястково-фалангових суглобів (Ehrlich G.E., 1972a). Ерозивні зміни дуже рідко виявляють при ОА колінних, кульшових суглобів і п’ястково-фалангових суглобів стоп і майже ніколи — при ОА плечових, ліктьових суглобів і суглобів хребта (Crain D.C., 1961; Ehrlich G.E., 2001). За даними G.E. Ehrlich (1972b) приблизно у 15% хворих з ерозивним ОА згодом розвивається РА, що проявляється стійким підвищенням ШОЕ і виявленням ревматоїдного фактора у крові.
Клінічно ерозивний ОА суглобів кистей визначають за ознаками локального запалення над ураженими суглобами (нерідко вже візуально зміненими у вигляді вузлів Гебердена і/або Бушара), їх латеральної нестабільності (результат ерозивних змін) і шишкоподібної деформації пальців (Balboza B. et al., 1968; Ehrlich G.E., 1972).
Гістологічно в синовіальній оболонці виявляють явища запалення без пануса, в аналізах крові — ознаки гострофазової відповіді (гіпергамаглобулінемія, підвищення ШОЕ і вмісту СРБ та ін.).
Природа ерозивного ОА не визначена. Його іноді трактують як перехресний стан між ОА і РА, хоча частіше — як тяжку форму ОА суглобів кистей (Dieppe P.A., 1995). В основі змін, що відзначають при ерозивному ОА, можливо, лежить явище неоангіогенезу (Ehrlich G.E., 1975; 2001; Walsh D.A., 2001). Результати більш раннього дослідження свідчили про підвищену неоваскуляризацію в ділянці вузликових деформацій пальців, останнє дослідження підтвердило це спостереження. Відомо, що неоваскуляризація — відповідь на ураження тканин запаленням. Крім того, цей процес може сприяти хронізації запалення при ряді хвороб, у тому числі й при ОА (Ehrlich G.E., 2001). Диференціювати ерозивний ОА потрібно з псоріатичним артритом, РА і рідше з мультицентричним ретикулогістіоцитозом.
Еволюція ОА суглобів кистей зазвичай завершується протягом декількох років (Kellgren J.H., Moore R., 1952; Ehrlich G.E., 1972; Hutton C.W. et al., 1986). Захворювання починається з відчуттів дискомфорту, болючості, іноді свербежу в ділянці міжфалангових суглобів і основи I п’ясткової кістки. Протягом кількох років (іноді місяців) симптоматика періодично загострюється і стихає, часто виникають ознаки локального запалення. Над суглобами можуть формуватися кісти. Через деякий час процес стабілізується, біль і запалення затихають, припухлість над суглобами стає твердою і фіксованою, набуває вузлуватого характеру; обсяг рухів у суглобах зменшується, іноді розвивається нестабільність суглобів.
Для ОА суглобів кистей характерно неодночасне ураження суглобів. Тому в кожний певний момент часу в одних суглобах зміни стабільні, в інших — є ознаки активного запалення й прогресування морфологічних змін. Ерозії, що з’являються, згодом піддаються зворотному розвитку, залишаючи типовий симптом «крила чайки». На думку P.A. Dieppe (1995), ОА суглобів кистей являє собою стадійний процес, у якому кожний суглоб проходить період активних змін, за яким йде стабілізація стану.
ОА суглобів кистей рідко супроводжується ускладненнями. Ураження променезап’ясткового суглоба може ускладнюватися тунельним синдромом. У кожному суглобі може розвиватися нестабільність. Наслідком ерозивної (безвузликової) форми ОА міжфалангових суглобів кистей може бути зрощення суглобових поверхонь (Crain D.C., 1961); цей процес прискорюється внутрішньосуглобовим введенням кортикостероїдних препаратів пролонгованої дії (Gray R.G. et al., 1981).
ОА хребта. ОА апофізарних суглобів хребта (спондилоартроз) і дегенерація міжхребетних дисків (остеохондроз) — різні захворювання (Dieppe P.A., 1995). Нагадаємо, що за визначенням ОА — захворювання синовіальних суглобів або диартрозів (див. Вступ), а остеохондроз — дегенеративне ураження хрящових суглобів або амфіартрозів. За класифікацією МКХ-10 остеохондроз і остеоартроз належать до різних класів хвороб — відповідно М42 і М47. Однак існує взаємозв’язок між остеоартрозом суглобів хребта та остеохондрозом: вони можуть сприяти виникненню один одного і зазвичай співіснують в одній і тій самій зоні хребта (Gotfried Y. et al., 1986).
Найчастіше ОА уражується шийний (особливо СV) і поперековий (особливо LIII–V) відділи хребта.
Морфологічні і рентгенологічні зміни в апофізарних суглобах хребта аналогічні таким при ОА інших локалізацій (Farfan H.S., 1973). Дегенерація міжхребетних дисків часто супроводжується крайовим остеофітозом. Імовірно, клінічний зв’язок між ОА апофізарних суглобів і дегенерацією міжхребетних дисків відображає їх біомеханічний взаємозв’язок: будь-які зміни в одному із цих зчленувань неминуче спричиняють аномальне навантаження на інший. Розміщення остеофітів на хребцях, можливо, демонструє прикладання максимального навантаження.
Рентгенологічні ознаки ОА хребта настільки часто виявляються у осіб віком близько 40 років, що дискутується питання: чи не є ОА хребта природнім процесом при старінні (Lawrense J.S. et al., 1966; Frymoyer J.W. et al., 1984)? На користь цієї гіпотези свідчить і те, що не виявлений зв’язок між ступенем рентгенологічних змін у суглобах хребта і вираженістю симптоматики — навіть значне прогресування морфологічних змін в апофізарних суглобах хребта з утворенням великих остеофітів нерідко клінічно не маніфестує (Dieppe P., 1995). Це також є відмінною рисою ОА хребта від остеохондрозу, для якого характерний чіткий взаємозв’язок між ступенем вираженості дегенеративних змін у дисках і клінічною маніфестацією. Найчастішою локалізацією ОА шийного відділу є ділянка від CV–CVII. Провокувати виникнення місцевого болю або навіть парестезії в зоні іннервації корінця можуть рухи у шийному відділі хребта, а саме розгинання та бокове згинання. При огляді характерними є болючість ураженого сегмента при пальпації і спазм паравертебральних та трапецієподібного м’язів. У більш тяжких випадках виникає порушення чутливості, слабкість та атрофія м’язів, а також порушення глибоких сухожилкових рефлексів у зоні іннервації ураженого корінця, а також розвиток симптоматики шийної мієлопатії, що характеризується виникненням відчуття слабкості у нижніх кінцівках, порушенням функції сечового міхура та гіперактивністю рефлексів нижніх кінцівок (Moskowitz R.W. et al., 2007).
Для ОА хребта характерний «механічний» характер болю в поперековому відділі: біль з’являється/посилюється при рухах, тривалому сидінні, стоянні. Вона може іррадіювати в ділянку сідниць і стегон. Посилення болю при розгинанні хребта більш характерне для ОА, посилення болю при згинанні хребта — для дегенерації міжхребетних дисків (Dieppe P., 1995). Серед інших типових ознак — зникнення поперекового лордозу, спазм паравертебральних м’язів. При виражених дегенеративно-дистрофічних змінах у міжхребцевих дисках або значних гіпертрофічних змінах тіл хребців виникає загроза стенозу поперекового відділу хребта з залученням у процес спинного мозку та спинномозкових корінців. У таких випадках типовим є виникнення болю у спині або сідницях, що посилюється при стоянні, менш виражений при ході та зниження його інтенсивності при сидінні (Katz J.N. et al., 1996).
Основним ускладненням ОА хребта є стискання нервових корінців остеофітами або при підвивиху апофізарних суглобів, що може супроводжуватися чутливими та руховими порушеннями. Подібні ускладнення можуть виникати при ураженні будь-якого відділу хребта; вони особливо виражені при ОА шийного відділу. Тяжкі неврологічні порушення спостерігаються при стисканні спинного мозку великими остеофітами. При стисканні хребетних артерій можливе порушення кровопостачання головного мозку у вертебробазилярному басейні. Великі передні остеофіти шийних хребців можуть стати причиною розвитку дисфагії. Проте слід зазначити, що такі ускладнення при ОА відзначають значно рідше, ніж при остеохондрозі хребта.
ОА інших локалізацій. ОА — одна із причин болю і дисфункції скронево-нижньощелепного суглоба (від 8 до 12% випадків) (Сrooks M.C. et al., 1991). Частота виникнення зростає з віком, наявністю патологічного прикусу, втратою зубів, бруксизмі та травмі зазначеного суглоба (Zarb G.A. et al., 1999). Найчастіше відзначають вторинний ОА цього суглоба на фоні запальних артропатій (Zart G.A., Carlsson g.E., 1979; Guralnick W., Keith D.A., 1991).). Клінічними проявами є обмеження рухів нижньої щелепи, включаючи зменшення відкриття рота, бокових рухів та висування нижньої щелепи вперед (Martinez-Bianco M. et al., 2004).
Як випадкову знахідку часто виявляють характерні для ОА зміни в груднино-ключичнім зчленуванні. Ці зміни вкрай рідко проявляються клінічно (Cierboom M.A.C., 1992). ОА — часта причина болю в акроміально-ключичному суглобі. Хворий, як правило, не може точно визначити джерело болю й характеризує її як біль у плечовому суглобі. При огляді ділянки суглоба виявляють болючість над його проекцією, іноді над верхнім полюсом можна пропальпувати остеофіт.
ОА плечового суглоба виявляють рідко й переважно у жінок похилого віку (Maquet P.G.J., 1976; Cushnaghan J., Dieppe P.A., 1991). Основні симптоми ОА плечового суглоба — болючість при рухах і пальпації, обмеження рухів у зв’язку з болем, особливо утруднені піднімання руки і зовнішня ротація. На рентгенограмах виявляють класичні рентгенологічні симптоми ОА, часто з великими остеофітами в ділянці нижнього полюса гленоїдальної ямки.
Ліктьовий суглоб рідко уражується ОА. Чоловіки хворіють частіше, ніж жінки, причому зазвичай у процес втягується плечоліктьовий відділ цього складного суглоба (Doherty M., Preston B., 1989). Больовий синдром при ОА ліктьового суглоба зазвичай не виражений (іноді відсутній), основними ознаками захворювання є фіксована флексія суглоба, крепітації та обмеження обсягу рухів.
Незважаючи на те що гомілковостопний суглоб часто травмується і несе більше навантаження, він рідко уражується ОА (Mann R.A., 1991).
У жінок будь-якого віку (особливо середнього і похилого) часто можна виявити вальгусну деформацію плюснофалангового суглоба I пальця стопи (hallux valgus) — результат носіння вузького взуття на високих підборах (Mann R.A. et al., 1979). Ця деформація, як правило, супроводжується ОА плюснофалангового суглоба I пальця стопи. Сам ОА цієї локалізації рідко проявляється клінічно, біль у ділянці суглоба зазвичай викликана вторинним запаленням суглобової сумки.
КЛІНІЧНІ ФОРМИ ТА ВАРІАНТИ ОСТЕОАРТРОЗУ
Аналіз результатів великих популяційних досліджень дозволив виділити чотири клінічні форми ОА, що найчастіше відзначають (Dieppe P.A., 1995) (рис. 6.2):
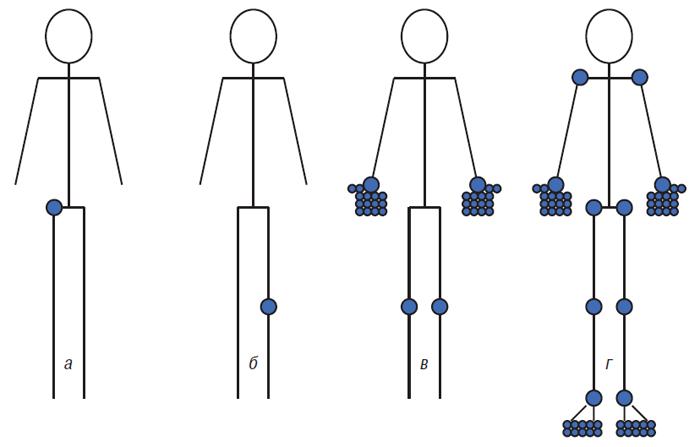
Рис. 6.2. Чотири найпоширеніші клінічні форми ОА (за Dieppe P.A., 1995). а — молодий чоловік з монококсартрозом, б — чоловік середнього віку з посттравматичним моноартрозом нижньої кінцівки, в — жінка середнього віку з ОА суглобів кистей і колінних суглобів, г — жінка похилого віку з розповсюдженим деструктивним ОА
1. Ранній моноартроз суглобів нижніх кінцівок. Очевидно, що моноартроз колінного, гомілковостопного або інших суглобів нижніх кінцівок в осіб молодого віку вторинний — після травми або операції (наприклад меніскектомії). Таку форму ОА відзначають рідко.
2. Ранній моноартроз тазостегнового суглоба також вторинний — посттравматичний (переважно у чоловіків молодого віку) або на фоні вроджених дисплазій (переважно у жінок молодого віку).
3. Комбінація ОА колінних суглобів та суглобів кистей. Цю форму часто відзначають у жінок середнього віку з ожирінням і гіпертонічною хворобою. Уражуються міжфалангові суглоби з утворенням вузликів і переважно медіальний тибіофеморальний і пателофеморальний компартменти колінного суглоба.
4. Комбінація гонартрозу, ОА кистей, хребта та ОА інших локалізацій прийнято називати генералізованим ОА. I.H. Kellgren і R. Moore (1952) рекомендували називати генералізований ОА «…наявність рентгенологічних ознак ОА в шести і більше групах суглобів, включаючи перші зап’ястково-п’ясткові суглоби кистей, проксимальні міжфалангові суглоби кистей, апофізарні суглоби хребта, колінні суглоби і перші плесневофалангові суглоби стоп». Згідно з класифікацією остеоартрозу ACR генералізованим називають ОА з ураженням трьох і більш суглобових груп з обов’язковим залученням наступних: колінні, тазостегнові суглоби, апофізеальні суглоби хребта і суглоби кистей і стоп.