ЩО З ЛОНЧАМИ?
Протягом останніх 10 років Центр з оцінки та досліджень лікарських засобів (Center for Drug Evaluation and Research — CDER) у складі Управління з контролю за харчовими продуктами та лікарськими засобами США (Food and Drug Administration — FDA) схвалює 38 нових препаратів на рік. Левова їх частка — для лікування орфанних захворювань.
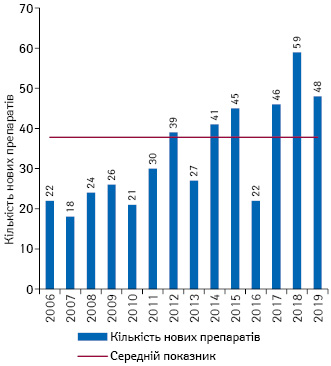
Слід зазначити, що у 2018 р. американським регулятором схвалено рекордні 59 нових молекулярних субстанцій (new molecular entities — NME). За підсумками 2019 р., допуск на ринок отримали трохи менше — 48 нових препаратів (рис. 1). Більш ніж половину з них розглянуто у пріоритетному порядку (Priority Review), що зумовлено прагненням регулятора якнайшвидше забезпечити доступ пацієнтів до інноваційних лікарських засобів, які покривають незадоволені медичні потреби. Проте слід зазначити, що така терміновість збалансована вимогою до фармвиробників щодо обов’язкового надання додаткових даних постмаркетингових досліджень. 41% NME, схвалених у 2019 р., визначені FDA як інноваційні препарати з принципово новим механізмом дії — перші у своєму класі (first-in-class).
ІНВЕСТИЦІЇ ТА ВИТРАТИ
Створення інноваційних препаратів — досить довготривалий та ризиковий процес, який потребує значних інвестицій.
Одним із найбільш ефективних механізмів забезпечення інноваційних процесів ресурсами для розвитку вважається венчурне фінансування. Це довготермінові високоризикові фінансові інвестиції в молоді інноваційні підприємства, діяльність яких спрямована на розробку та виробництво наукомістких високотехнологічних продуктів (з метою їх розвитку та отримання прибутку від приросту вартості вкладених грошових ресурсів).
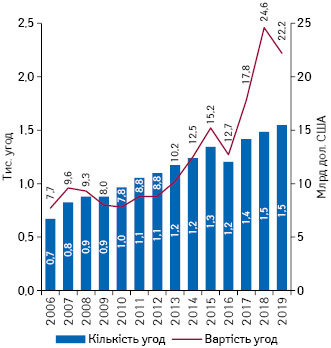
За даними IQVIA Institute for Human Data Science, протягом останніх 5 років обсяги венчурних інвестицій у галузі медико-біологічних наук збільшуються в середньому на 12% щороку. За підсумками 2019 р. закрито більш ніж 1,5 тис. угод загальною вартістю більше 22 млрд дол. США (рис. 2). Приблизно третина з них спрямована на надання фінансової підтримки компаніям на ранніх етапах розвитку, існування лише ідеї або бізнес-плану (angel & seed).
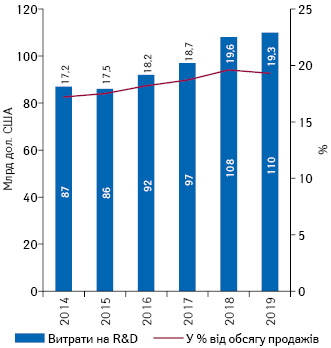
Також, за даними IQVIA Institute for Human Data Science, топ-15 найбільших фармкомпаній за підсумками 2019 р.** витрачають на R&D більш ніж 19% доходу від продажу (рис. 3). А в компаніях з меншим рівнем доходу цей показник може сягати 50%. Успіх більшості фармкомпаній майже цілком залежить від пошуку та розробки нових препаратів, тож не дивно, що R&D є такою вагомою статтею витрат. Дані порталу Statista за 2018 р. свідчать про те, що 21,7% загальносвітових витрат на R&D припадає саме на сферу охорони здоров’я, яку випереджає лише галузь обчислювальної техніки та електроніки (22,5%).
УСПІШНІСТЬ КЛІНІЧНИХ ДОСЛІДЖЕНЬ
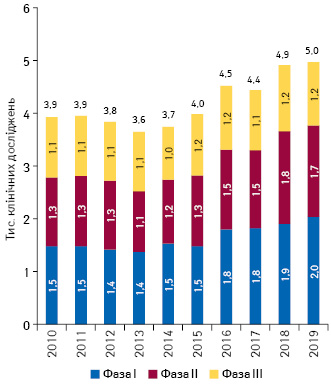
За даними IQVIA Institute for Human Data Science, загальна кількість клінічних досліджень фази I та II за останні 5 років збільшилася на 38% (рис. 4).
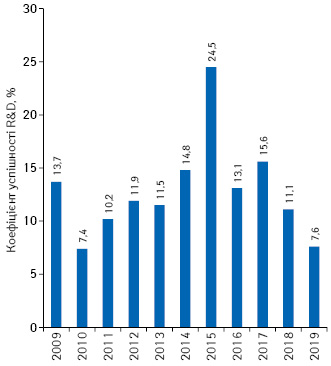
При цьому коефіцієнт успішності (проходження всіх етапів досліджень та схвалення регуляторним органом) протягом останніх 2 років значно знизився (рис. 5). На думку аналітиків IQVIA Institute for Human Data Science, це може бути пов’язано зі збільшенням числа проєктів у сфері онкології, біологічних препаратів, а також орфанних лікарських засобів.
ЯК ЗРОБИТИ ДОСЛІДЖЕННЯ БІЛЬШ ПРОГНОЗОВАНИМИ?
За даними компанії PricewaterhouseCoopers, для того щоб фармацевтична галузь стала більш інноваційною, а витрати на R&D скоротилися, життєво важливими є наступні 4 принципи:
- системне розуміння того, як працює людський організм на молекулярному рівні;
- краще розуміння патологічної фізіології, функціональних порушень в організмі, що виникають під час хвороби;
- більш широке використання новітніх технологій для «віртуалізації» та прискорення процесу клінічних досліджень;
- розширення співпраці між фармацевтичною індустрією, академічними колами, регуляторними органами, державою та постачальниками медичних послуг.
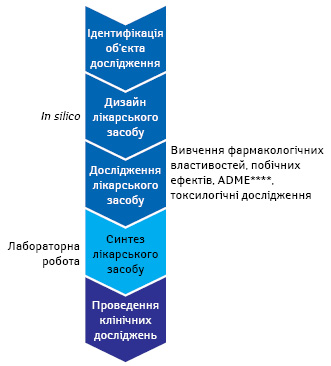
Що стосується «віртуалізації» та прискорення процесу клінічних досліджень, наразі доступні новітні технології, які допомагають досягати кращого розуміння природи того чи іншого захворювання, моделювати і прогнозувати дію кандидата в препарати до проведення клінічних досліджень. Перспективним напрямом є робота фахівців у сфері біоінформатики зі створення «віртуальної людини». Із впровадженням такої технології стане можливим застосування цифрового образу людського тіла з ознаками певного захворювання, а за допомогою прогнозного аналізу оцінити як молекула ймовірно абсорбуватиметься, розпадатиметься та виводитиметься з організму, які можливі довгострокові побічні реакції, в якій лікарській формі та дозуванні працюватиме найкраще тощо. Тобто значний обсяг роботи можна вирішити до початку клінічних досліджень. Схематичне зображення процесу розробки нового препарату із застосуванням «віртуальної людини» представлено на рис. 6.
МАЙБУТНЄ НЕ ЗА ГОРАМИ: ПЕРСПЕКТИВНІ НАПРЯМКИ R&D
Деякі з нових методів лікування не зовсім звичайні ліки, які можна випробувати звичайним способом.
КОЛИ ПРЕПАРАТ НЕ ПРЕПАРАТ
Наразі тривають десятки клінічних досліджень з оцінки ефективності лікування на основі генної терапії різних захворювань.
Ще один перспективний напрямок — клітинна терапія, або регенеративна медицина — відновлення ураженої хворобою або пошкодженої (травмованої) тканини за допомогою активації ендогенних стовбурових клітин або трансплантації клітин. Існує великий потенціал для застосування регенеративної медицини: лікування серцево-судинної системи, інсулінозалежного цукрового діабету, травм спинного мозку, хвороби Паркінсона.
Новітні досягнення науки допомагають фармкомпаніям створювати кращі способи доставки діючої речовини, що сприяють підвищенню прихильності пацієнтів до лікування (дотримання режиму терапії), а отже, і покращенню результатів терапії. Так, із досягненнями у сфері нанотехнологій можливо доставляти терапевтичний агент до певних клітин тіла людини, розробляти методи нанодіагностики та спостерігати за реакцією на препарат у пацієнтів.
Слід зазначити, що, за оцінками компанії GlobalData, на стадії клінічних досліджень знаходиться понад 230 нанофармацевтичних препаратів. З них 75% є розробками для боротьби з онкологічними захворюваннями.
SMALL MOLECULE
На «полі» низькомолекулярних препаратів також є величезний невикористаний потенціал та «гарячі» зони для залучення інвестицій.
Численні стартапи, а також деякі компанії Big Pharma спрямовують свої зусилля на розробку низькомолекулярних препаратів, які стимулюють деградацію білків.
Так, клінічні дослідження химерних молекул, що сприяють деградації білків (Proteolysis targeting chimeras — PROTAC), є новою надією на лікування онкологічних захворювань. PROTAC складаються з двох молекул, з’єднаних лінкером, причому одна молекула специфічно зв’язується з убіквітин-лігазою E3, а інша — з протеїном-мішенню. Це призводить до убіквітинування цільового протеїну та його деградації протеасомою. Таким чином, принцип дії таких препаратів принципово відрізняється від традиційних молекул-інгібіторів.
Мікробіом людини вважають одним із головних факторів впливу на імунну систему людини в цілому. Мікробіом означає сукупність генів усіх мікроорганізмів, що живуть в організмі людини. З ним пов’язують широкий спектр захворювань, серед яких запальні захворювання кишечнику, цукровий діабет, розсіяний склероз, аутизм, онкологічні захворювання, СНІД. Даний напрямок досліджень швидко розвивається та залучає великі інвестиції.
Протягом останніх десятиліть стара добра ідея оцінки біологічної активності великої кількості хімічних субстанцій зазнала серйозних перетворень. Центральною ідеєю став віртуальний скринінг, за допомогою якого можна проводити попередні дослідження in silico мільйонів нових молекул з метою виявлення сполук-«хітів» для подальшої розробки та проведення досліджень у лабораторіях.
З моменту відкриття технологій глибинного навчання (яке є частиною широкого сімейства методів машинного навчання) тема штучного інтелекту стала надзвичайно актуальною у багатьох аспектах досліджень фармкомпаній. Ця сфера є досить привабливою для венчурних інвестицій, проте варто враховувати, що тема штучного інтелекту схильна викликати навколо себе надмірний ажіотаж, тож може бути складно тверезо оцінити реальний потенціал проєкту.
За матеріалами fda.gov, iqvia.com, statista.com, pwc.com, globaldata.com, prnewswire.com