«Ситуація змінюється. Як тільки з’являється доступна вакцина, плацебо-контрольоване дослідження більш не є етичним або прийнятним», — говорить Скотт Гальперін (Scott Halperin), директор Канадського центру вакцинології при Університеті Далхаузі (Canadian Centre for Vaccinology at Dalhousie University), який очолює випробування 2 вакцин проти COVID-19 за участю людей.
Аналітики очікують, що вакцини першого покоління будуть широко доступні в найближчі 6–12 міс у більшості країн з високим рівнем доходів і в деяких країнах світу, що розвиваються. Тому виробники вакцин наступного покоління розглядають способи отримання доказів ефективності своїх продуктів без порівняння з плацебо.
«Вікно закривається», — зазначив імунолог Робін Шатток (Robin Shattock) з Імперського коледжу Лондона (Imperial College London), де також розробляється вакцина проти COVID-19, яка знаходиться на І етапі тестування за участю людей у 4 центрах на півдні Англії.
На сьогодні близько 60 вакцин-кандидатів проходять випробування на людях, а ще більше 170 знаходяться на різних стадіях доклінічної оцінки (рисунок). Деякі з них створені на основі генетичних технологій і при введенні допомагають виробляти в організмі білки коронавірусу, які запускають роботу імунітету. Також вакцини можуть включати білки коронавірусу, інактивовані форми вірусу або інші типи вірусів, модифіковані для передачі генетичних інструкцій зі створення білків коронавірусу.
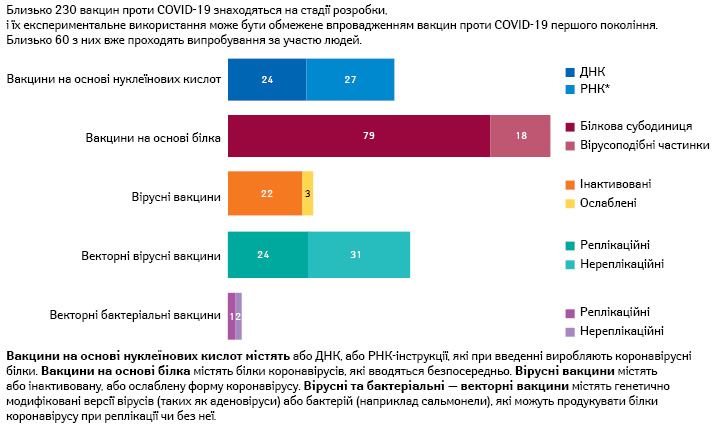
*РНК-вакцина від «Pfizer» та «BioNTech», вакцина першого покоління, включена до цього переліку, оскільки підприємство наразі здійснює набір для дослідження в Китаї.
Проблеми з набором учасників клінічних досліджень
Уже зараз масове впровадження вакцин проти COVID-19 серед певних груп населення починає впливати на набір учасників клінічних досліджень. Наприклад, «Novavax», компанія з виробництва вакцин в Гейтерсберзі, США, проводить дослідження вакцини проти COVID-19, в якій використовуються очищені вірусні білки, що є загальновизнаним підходом, який надає потенційні переваги з точки зору безпеки.
Такі вакцини також можна зберігати в холодильниках, що дозволяє розподіляти їх за допомогою стандартних каналів ланцюга постачання вакцин. Однак керівник відділу досліджень і розробок компанії «Novavax» Грегорі Гленн (Gregory Glenn) відзначає, що в дослідженні за участю 30 тис. осіб, розпочатого «Novavax» наприкінці минулого місяця, медичні працівники, які є однією з основних цілей попередніх досліджень ефективності вакцин проти COVID-19 (у зв’язку з наявністю у них підвищеного ризику інфікування), більше не є найпопулярнішими учасниками. Це пов’язано з тим, що медичні працівники входять до пріоритетної групи населення і вже зараз активно імунізуються вакцинами першого покоління.
Стати учасниками клінічних досліджень також буде важче людям літнього віку або особам із супутніми захворюваннями — 2 групам населення, які мають особливу потребу у вакцинах, враховуючи їх схильність до серйозних ускладнень COVID-19.
«Виведення цих груп з числа потенційних учасників випробування неминуче ускладнить набір», — підкресли К. Мері Хілі (C. Mary Healy), фахівець з інфекційних захворювань з Медичного коледжу Бейлора (Baylor College of Medicine), яка залучена до дослідження «Novavax».
Дизайнери досліджень розробили кілька обхідних шляхів, щоб стимулювати участь. Наприклад, у деяких плацебо-контрольованих дослідженнях на 1 людину, що отримує плацебо, припадає 2 людини, яким вводять активну вакцину-кандидат (замість звичайного рівного розподілу).
Такий підхід дозволяє компаніям збирати більше інформації про безпеку вакцин-кандидатів. Це пов’язано з тим, що більша кількість учасників отримують активну дозу і можуть відчувати побічні реакції. Як додатковий бонус, майбутні учасники дослідження охочіше ризикують, коли мають 2 з 3 шансів, що вони отримають активну вакцину-кандидат.
Інший обхідний шлях — це дослідження, в якому не використовують плацебо, а замість цього вакцину-кандидат порівнюють з уже затвердженою вакциною. Французький виробник вакцин «Sanofi Pasteur» і його британський партнер «GlaxoSmithKline» працюють над вакциною на основі білка, подібною до вакцини «Novavax», і наразі вони планують дослідження з таким дизайном.
Однак, згідно з неопублікованими підрахунками групи біостатистики програми уряду США із вакцинації «Operation Warp Speed», процес доведення того, що експериментальна вакцина істотно не поступається тій, яка є ефективною на 95%, як правило, вимагає більш тривалих та масштабних досліджень, ніж того вимагають плацебо-контрольовані випробування.
«Вони повинні бути настільки великими, що навряд чи будуть практичними», — наголосив Пітер Сміт (Peter Smith), епідеміолог Лондонської школи гігієни і тропічної медицини (London School of Hygiene and Tropical Medicine), Великобританія.
Непрямі показники захисту від COVID-19
Існує й інший варіант — виміряти ефективність вакцини за допомогою імунних маркерів, які виробляються в крові людини після щеплення. Наприклад, певний рівень антитіл може бути контрольним маркером (корелятом захисту) того, чи настроєна імунна система людини на знищення вхідних коронавірусів.
Нові вакцини проти грипу, сказу і багатьох інших інфекційних захворювань вже проходять оцінку з використанням цих корелятів захисту, і це усуває необхідність у використанні плацебо. Проблема розробників вакцини проти COVID-19 полягає в тому, що, на відміну від багатьох інших інфекційних захворювань, досі незрозуміло, який тип імунної відповіді є надійним показником індукованого вакциною захисту від нового коронавірусу.
«Випробування на сьогодні свідчать про те, що рівні антитіл, які називають імуноглобуліном G (IgG), можуть служити цим непрямим індикатором захисту, але докази є лише опосередкованими», — зазначив Ден Баруш (Dan Barouch), вірусолог з Медичного центру «Beth Israel Deaconess» в Бостоні, США.
Щоб підтвердити, що IgG є корелятом захисту, вченим необхідно вивчити показники людей, які отримали вакцину від COVID-19, але все одно захворіли — розвивається так звана проривна інфекція (breakthrough infections). Якщо рівень IgG в крові цих людей зменшиться нижче порогового значення, встановленого у людей, для яких вакцини працювали, це може допомогти вченим визначити кількість антитіл, яка необхідна для того, щоб будь-яка нова вакцина була визнана ефективною.
Спірне питання
Ще одним ускладненням є те, що більшість великих випробувань вакцин розроблено для того, щоб перевірити, чи не з’являються в учасників симптоми COVID-19, а не щоб з’ясувати, чи інфіковані вони новим коронавірусом. Але якщо вакцини мають зупинити поширення вірусу, розробникам потрібно мати імунний корелят, який вказує на те, що людина захищена від інфекції, а не тільки від її симптомів.
«Це те, що активно досліджується, але лише шляхом періодичних вимірювань, які можуть пропустити інфекції», — зауважив Холлі Джейнс (Holly Janes), біостатист з Онкологічного дослідницького центру Фреда Хатчінсона (Fred Hutchinson Cancer Research Center) в Сіетлі, США.
Деякі дослідники виступають за навмисне зараження вакцинованих людей новим коронавірусом у рамках випробування «human challenge» і подальше ретельне відстеження швидкості зараження і біомаркерів, що його супроводжують.
Цей підхід, як і раніше, зазвичай включає використання плацебо, але для нього потрібно набагато менше добровольців, ніж для випробувань в умовах практичної роботи (field trials), і він дає результати набагато швидше. Випробування «human challenge» залишаються спірними — навіть неетичними, як кажуть деякі експерти.
«Але чисто на науковому рівні всі згодні з тим, що такі випробування — кращий спосіб отримати точні імунні кореляти», — зазначив Нір Еял (Nir Eyal), фахівець з біоетики з Університету Рутгерса (Rutgers University), США.
Регуляторні органи наразі працюють із вченими та виробниками вакцин, щоб визначити найкращий шлях розробки вакцин наступного покоління.
«Зараз ми знаходимося в такій цікавій зоні, де немає чітких вказівок», — підкреслив Роб Коулман (Rob Coleman), співзасновник і виконавчий директор компанії «Codagenix», що незабаром розпочне тестування за участю людей вакцини-кандидата проти COVID-19, що містить ослаблену форму коронавірусу.
за матеріалами nature.com