Дарилия (Darylia)
Дарилия инструкция по применению
Состав
1 активная таблетка содержит 3 мг дроспиренона кристаллического 100% и 0,02 мг этинилэстрадиола микронизированного 100%;
другие составляющие: лактозы моногидрат, крахмал кукурузный, крахмал прежелатинизированный, макрогола и спирта поливиниловый сополимер, магния стеарат;
пленочная оболочка: спирт поливиниловый, титана диоксид (Е171), макрогол, тальк, лецитин (соевый);
1 таблетка плацебо содержит:
действующие вещества: отсутствуют;
другие составляющие: целлюлоза микрокристаллическая, лактоза безводная, крахмал прежелатинизированный, магния стеарат, кремния диоксид коллоидный безводный;
пленочная оболочка: спирт поливиниловый, титана диоксид (E171), полиэтиленгликоль (макрогол), тальк, индиготин (E132), хинолиновый желтый (E104), железа оксид черный (E172), желтый закат FCF (E110).
Дроспиренон - 3 мг
Этинилэстрадиол - 0,02 мг
Фармакологические свойства
фармакодинамика. Индекс Перля контрацептивных неудач: 0,41 (верхний двусторонний 95% доверительный интервал: 0,85).
Общий индекс Перля (контрацептивные неудачи + ошибки со стороны пациенток): 0,80 (верхний двусторонний 95% доверительный интервал: 1,30).
Контрацептивный эффект препарата Дарилия основывается на взаимодействии различных факторов, наиболее важными из которых являются торможение овуляции и изменение эндометрия.
Дарилия, таблетки, покрытые пленочной оболочкой — это комбинированный пероральный контрацептив (КПК), содержащий этинилэстрадиол и прогестоген дроспиренон. В терапевтической дозе дроспиренон обладает антиандрогенными и слабыми антиминералокортикоидными свойствами. Он лишен какой-либо эстрогенной, глюкокортикоидной и антиглюкокортикоидной активности. Это обеспечивает дроспиренону фармакологический профиль, крайне похожий на натуральный гормон прогестерон. Слабые антиминералокортикоидные свойства препарата вызывают слабый антиминералокортикоидный эффект.
Фармакокинетика
Дроспиренон (3 мг)
Всасывание. При пероральном применении дроспиренон быстро и почти полностью абсорбируется. Cmax активного вещества в плазме крови — 38 нг/мл — достигается через 1–2 ч после однократного приема. Биодоступность — 76–85%. Прием пищи не влияет на биодоступность дроспиренона.
Распределение. После перорального применения плазменные концентрации дроспиренона снижались с конечным T½ 31 ч. Дроспиренон связывается с сывороточным альбумином и не связывается с глобулином, связывающим половые гормоны (ГСПГ), или кортикостероидсвязывающим глобулином. Только 3–5% общей плазменной концентрации активного вещества представляет собой свободный гормон. Индуцированное этинилэстрадиолом повышение ГСПГ не влияет на связывание дроспиренона с белками плазмы крови. Средний предполагаемый объем распределения составляет 3,7±1,2 л/кг.
Метаболизм. После перорального приема дроспиренон экстенсивно метаболизируется. Большая часть метаболитов в плазме крови представлены кислотными формами дроспиренона, образовавшимися при раскрытии лактонового кольца, и 4,5-дигидро-дроспиренон-3-сульфатом, который образуется путем восстановления и дальнейшего сульфатирования. Дроспиренон также подвергается окислительному метаболизму, который катализируется CYP 3A4. In vitro дроспиренон может слабо или умеренно подавлять ферменты цитохрома P450: CYP 1A1, CYP 2C9, CYP 2C19 и CYP 3A4.
Выведение. Скорость метаболического клиренса дроспиренона в плазме крови составляет 1,5±0,2 мл/мин/кг. Дроспиренон выделяется только в следовых количествах в неизмененном виде. Метаболиты дроспиренона экскретируются с калом и мочой в соотношении примерно 1,2:1,4; T½ метаболитов составляет около 40 ч.
Равновесная концентрация. Во время одного цикла приема равновесная Cmax дроспиренона в плазме крови (около 70 нг/мл) достигается через 8 дней. Плазменные концентрации дроспиренона повышались приблизительно в 3 раза как следствие отношения (или пропорции) конечного T½ и интервала дозирования.
Отдельные категории пациенток
Недостаточность функции почек. Равновесный уровень дроспиренона в плазме крови женщин со слабой почечной недостаточностью (клиренс креатинина 50–80 мл/мин) был сравним с таковым у женщин с нормальной функцией почек (>80 мл/мин). Уровень дроспиренона в плазме крови в среднем был на 37% выше у женщин со средней степенью почечной недостаточности (клиренс креатинина 30–50 мл/мин) по сравнению с таковым у женщин с нормальной функцией почек. Терапия дроспиреноном хорошо переносилась пациентками с почечной недостаточностью легкой и средней степени и не оказывала клинически значимого влияния на концентрацию калия в плазме крови.
Недостаточность функции печени. Известно, что у добровольцев с умеренными нарушениями функции печени клиренс одной дозы после перорального применения был снижен примерно на 50% по сравнению с таким показателем у добровольцев. Выявленное уменьшение клиренса дроспиренона у добровольцев с умеренной почечной недостаточностью не приводит к каким-либо значимым расхождениям концентрации калия в плазме крови. Даже при сахарном диабете и одновременном лечении спиронолактоном (два фактора, которые могут провоцировать предрасположенность к развитию гипергликемии) не отмечено повышения концентрации калия в плазме крови выше верхнего предела нормы. Можно сделать вывод, что дроспиренон хорошо переносится пациентами с легкой и умеренной печеночной недостаточностью (класс В по Чайлда — Пью).
Этинилэстрадиол (0,02 мг)
Всасывание. Этинилэстрадиол после перорального применения быстро и полностью абсорбируется. Cmax в плазме крови после однократного приема одной дозы достигается через 1–2 ч и составляет около 33 пкг/мл. Aбсолютная биодоступность варьирует и составляет около 60%.
Одновременный прием пищи снижал биодоступность этинилэстрадиола примерно у 25% обследованных пациенток, а у остальных изменений не отмечено.
Распределение. Концентрация этинилэстрадиола в плазме крови снижалась двухфазно, в фазе конечного распределения T½ составляет около 24 ч. Этинилэстрадиол хорошо, но неспецифически связывается с сывороточным альбумином (около 98,5%) и индуцирует повышение концентрации в плазме крови ГСПГ и кортикостероидсвязывающего глобулина. Предполагаемый объем распределения — около 5 л/кг.
Метаболизм. Этинилэстрадиол подвергается значительному пресистемному метаболизму в тонкой кишке и печени. Первоначально этинилэстрадиол метаболизируется путем ароматического гидроксилирования, при этом образуется широкий спектр гидроксилированных и метилированных метаболитов, выявляемых в виде свободных метаболитов и конъюгатов с глюкуронидами и сульфатами. Скорость клиренса метаболитов этинилэстрадиола составляет около 5 мл/мин/кг.
Исследования in vitro показали, что этинилэстрадиол является обратным ингибитором CYP 2C19, CYP 1A1 и CYP 1A2, а также на основе механизма действия — ингибитором CYP 3A4/5, CYP 2C8 и CYP 2J2.
Выведение. Этинилэстрадиол практически не выводится в неизмененном виде. Метаболиты этинилэстрадиола выводятся с мочой и желчью в соотношении 4:6. T½ для метаболитов составляет около 1 сут.
Равновесная концентрация. Состояние равновесной концентрации достигается в течение второй половины цикла, причем сывороточный уровень этинилэстрадиола аккумулируется с кратностью около 2–2,3.
Этнические группы. Известно, что клинически значимых отличий в фармакокинетике дроспиренона и этинилэстрадиола у женщин европеоидной и монголоидной рас не отмечено.
Доклинические данные по безопасности. У лабораторных животных эффекты дроспиренона и этинилэстрадиола были ограничены теми, которые ассоциировались с известным фармакологическим действием. В частности, исследования по выявлению репродуктивной токсичности у животных показали наличие видоспецифического эмбриотоксического и фетотоксического воздействия. При экспозиции дроспиренона и этинилэстрадиола, превышающей терапевтическую, отмечено влияние на половую дифференциацию у эмбрионов крыс, но не у обезьян.
Показания Дарилия
пероральная контрацепция.
Применение Дарилия
в одной блистерной упаковке содержится 28 таблеток (24+4): 24 таблетки белого или почти белого цвета (активные таблетки) и 4 таблетки зеленого цвета (таблетки плацебо — неактивны).
Как принимать препарат Дарилия (24+4). Таблетки необходимо принимать ежедневно примерно в одно и то же время, в случае необходимости запивая небольшим количеством жидкости, в последовательности, указанной на блистерной упаковке. Перерывов между приемом таблеток быть не должно. Необходимо принимать по 1 таблетке в сутки в течение 28 дней. Прием таблеток из каждой последующей упаковки следует начинать после приема последней таблетки из предварительной упаковки. Менструальноподобное кровотечение обычно наступает на 2–3-й день после начала приема таблеток плацебо (таблетки зеленого цвета в последнем ряду) и не обязательно заканчивается до начала приема таблеток из новой упаковки.
Как начать прием препарата Дарилия (24+4)
Если гормональные контрацептивы в предыдущий период (прошлый месяц) не применяли. Прием таблеток следует начинать в первый день менструального цикла (т.е. в первый день менструального кровотечения).
Переход с другого комбинированного гормонального контрацептива (КГК) (таблетки, вагинальное кольцо или трансдермальный пластырь). Женщина должна начать прием препарата Дарилия на следующий день после обычного перерыва или после приема последней неактивной таблетки предыдущего КГК. При переходе с вагинального кольца или трансдермального пластыря прием таблеток Дарилия желательно начинать в день удаления предыдущего средства, но не позднее дня запланированного применения вагинального кольца или трансдермального пластыря.
Переход с метода, основанного на применении только прогестагена (мини-пили, инъекции, имплантаты) или внутриматочной системы с прогестагеном. Женщина может начать прием препарата Дарилия в любой день после прекращения приема «мини-пили» (в случае имплантата или внутриматочной системы — в день их удаления, в случае инъекции — вместо следующей инъекции). Однако во всех случаях рекомендуется использовать барьерный метод контрацепции в течение первых 7 дней приема препарата.
После аборта в I триместр беременности. Применение препарата следует начать немедленно в тот же день после операции. В таком случае нет необходимости применять дополнительные средства контрацепции.
После родов или аборта во ІІ триместр беременности. Если женщина кормит грудью, см. Применение в период беременности или кормления грудью.
Женщинам необходимо рекомендовать начинать прием препарата Дарилия с 21–28-го дня после родов или аборта во II триместр беременности. Если женщина позже начинает прием таблеток, следует рекомендовать дополнительно использовать барьерный метод контрацепции в течение первых 7 дней приема таблеток. Однако если половой акт уже произошел, то перед началом применения КГК необходимо исключить беременность или женщине следует дождаться первой менструации.
Пропуск приема таблетки. Пропуск приема зеленой таблетки плацебо из 4-го ряда можно не учитывать. Однако ее нужно выбросить во избежание случайного удлинения фазы плацебо. Приведенные ниже указания касаются только пропуска активных таблеток белого цвета.
Если опоздание в приеме таблетки не превышает 24 ч, противозачаточное действие препарата не снижается. Пропущенную таблетку следует принять сразу, как только вспомнили об этом.
Следующую таблетку из этой упаковки следует принимать в обычное время.
Если опоздание с приемом пропущенной таблетки превышает 24 ч, контрацептивная защита может уменьшиться. В таком случае необходимо руководствоваться двумя основными правилами:
1. Рекомендуемый перерыв в приеме гормональных таблеток составляет 4 дня; прием препарата нельзя прерывать более чем на 7 дней.
2. Адекватное угнетение системы гипоталамус-гипофиз-яичники достигается при непрерывном применении таблеток в течение 7 дней.
Согласно этому в повседневной жизни следует руководствоваться следующими рекомендациями:
Дни 1–7. Женщина должна принять последнюю пропущенную таблетку как можно скорее, даже если придется принять две таблетки одновременно. После этого она продолжает принимать таблетки в обычное время. Кроме того, в течение следующих 7 дней следует использовать барьерный метод контрацепции, например презерватив. Если в предыдущие 7 дней произошел половой акт, следует учитывать возможность наступления беременности. Чем больше таблеток пропущено и чем ближе этот пропуск к фазе таблеток плацебо, тем выше риск беременности.
Дни 8–14. Женщина должна принять последнюю пропущенную таблетку как можно скорее, даже если придется принять две таблетки одновременно. После этого она продолжает принимать таблетки в обычное время. Если женщина правильно принимала таблетки в течение 7 дней до пропуска, нет необходимости применять дополнительные противозачаточные средства. В противном случае или при пропуске более одной таблетки рекомендуется дополнительно использовать барьерный метод контрацепции в течение 7 дней.
Дни 15–24. Достоверность снижения контрацептивного эффекта значительна из-за приближения фазы таблеток плацебо. Однако при соблюдении схемы приема таблеток можно избежать снижения контрацептивной защиты. Если придерживаться одного из следующих вариантов, то нет необходимости применять дополнительные контрацептивные средства при правильном приеме таблеток в течение 7 дней до пропуска. В противном случае рекомендуется придерживаться первого из указанных ниже вариантов и использовать дополнительные методы контрацепции в течение 7 дней.
Женщина должна принять последнюю пропущенную таблетку как можно скорее, даже если придется принять две таблетки одновременно. После этого она продолжает принимать таблетки в обычное время, пока активные таблетки не закончатся, но 4 таблетки плацебо принимать не следует, нужно сразу начать прием таблеток со следующей блистерной упаковки. Маловероятно, что у женщины начнется менструальноподобное кровотечение до окончания приема таблеток из второй упаковки, хотя при приеме таблеток могут наблюдаться кровянистые выделения или прорывное кровотечение.
Женщине можно посоветовать прекратить прием активных таблеток из текущей блистерной упаковки. Вместо активных таблеток следует принять таблетки плацебо из последнего ряда в течение 4 дней, включая дни пропуска таблеток, а затем начать прием таблеток из следующей блистерной упаковки.
Если женщина пропустила прием таблеток и у нее отсутствует менструальноподобное кровотечение во время первого обычного перерыва в приеме препарата, следует рассмотреть вероятность беременности.
Рекомендации в случае нарушений со стороны ЖКТ. В случае тяжелых нарушений со стороны ЖКТ (рвота, диарея) возможно неполное всасывание препарата. В этом случае следует применять дополнительные средства контрацепции. Если в течение 3–4 ч после приема активной таблетки произошла рвота, необходимо как можно скорее принять новую таблетку (из другой упаковки), которая заменит предыдущую. Новую таблетку необходимо принять в течение 24 ч после обычного приема. Если прошло более 24 ч, необходимо соблюдать правила приема препарата, указанные в разделе Пропуск приёма таблетки. Если женщина не хочет изменять свою привычную схему приема препарата, ей необходимо принять дополнительную(ые) таблетку(и) из другой упаковки.
Как сместить время возникновения кровотечения «отмены». Чтобы задержать день начала менструации, женщине следует пропустить прием таблеток плацебо и начать прием активных таблеток Дарилия из новой упаковки. При желании срок приема можно продолжить вплоть до окончания второй упаковки. При этом могут наблюдаться прорывные кровотечения или кровянистые выделения. Регулярное применение препарата Дарилия восстанавливается после приема таблеток плацебо.
Чтобы сместить наступление менструации на другой день недели, рекомендуется сократить фазу плацебо на желаемое количество дней. Следует отметить, что чем короче будет перерыв, тем выше вероятность отсутствия менструальноподобного кровотечения и выше риск возникновения прорывного кровотечения или кровянистых выделений в течение периода приема таблеток из следующей упаковки (как в случае задержки наступления менструации).
Подготовка к использованию полосы недельного календаря-стикера. Для того чтобы помочь пациентке следить за приемом таблеток, в упаковку вложен недельный календарь-стикер, на котором обозначены 7 дней недели.
| → | Пн | Вт | Ср | Чт | Птн | Сб | Вс |
| → | Вт | Ср | Чт | Птн | Сб | Вс | Пн |
| → | Ср | Чт | Птн | Сб | Вс | Пн | Вт |
| → | Чт | Птн | Сб | Вс | Пн | Вт | Ср |
| → | Птн | Сб | Вс | Пн | Вт | Ср | Чт |
| → | Сб | Вс | Пн | Вт | Ср | Чт | Птн |
| → | Вс | Пн | Вт | Ср | Чт | Птн | Сб |
Женщина должна выбрать самоклеющуюся полоску календаря, обозначения на которой начинаются со дня недели, когда она начинает принимать таблетки. Например, если она начинает принимать таблетки в среду, выбирает наклейку-полоску, которая начинается с обозначения «Ср.» («Среда»).
Следует приложить символ → на полоске к такому же символу в блистерной упаковке и приклеить полоску на блистер на место, обведенное линией. Каждый день недели будет обозначен параллельно линии расположения таблеток в блистерной упаковке. Таким образом можно видеть, в какой день недели женщина принимает таблетку. Необходимо принимать таблетки в последовательности, указанной на блистерной упаковке, пока не будут приняты все 28 таблеток. В течение 4 дней, когда женщина принимает зеленые таблетки плацебо, должно начаться менструальноподобное кровотечение. Оно, как правило, начинается на 2-й или 3-й день после приема последней белой активной таблетки Дарилия. После того как женщина приняла последнюю зеленую таблетку, необходимо начать прием таблеток из новой блистерной упаковки и использовать следующую полоску 7-дневного календаря-стикера, несмотря на то, закончились кровотечение отмены, или нет. Это означает, что женщина начнет применение каждой полоски недельного календаря в тот же день недели и кровотечение отмены будет происходить в те же дни каждого месяца.
Противопоказания
КПК не следует применять при наличии одного из нижеприведенных состояний или заболеваний. В случае, если любое из этих состояний или заболеваний возникает впервые во время применения КПК, прием препарата следует немедленно прекратить.
- Повышенная чувствительность к действующим веществам или любому из вспомогательных веществ препарата.
- Повышенная чувствительность к арахису или сое.
- Наличие или риск возникновения венозной тромбоэмболии (ВТЭ):
- ВТЭ (применение антикоагулянтов) или наличие в анамнезе (например тромбоз глубоких вен или тромбоэмболия легочной артерии);
- наследственная или приобретенная предрасположенность к развитию ВТЭ, например резистентность к активированному протеину С (включая фактор V Лейдена), недостаточность антитромбина III, недостаточность протеина С, недостаточность протеина S;
- обширное хирургическое вмешательство с длительной иммобилизацией (см. ОСОБЫЕ УКАЗАНИЯ);
- высокий риск развития ВТЭ в связи с наличием многочисленных факторов риска (см. ОСОБЫЕ УКАЗАНИЯ).
- Наличие или риск возникновения артериальной тромбоэмболии:
- имеющаяся артериальная тромбоэмболия, в том числе в анамнезе (например инфаркт миокарда), или продромальное состояние (например стенокардия);
- нарушения мозгового кровообращения — инсульт в настояшее время или в анамнезе, продромальное состояние (например транзиторная ишемическая атака);
- наследственная или приобретенная предрасположенность к развитию артериальной тромбоэмболии, например гипергомоцистеинемия и наличие антифосфолипидных антител (антикардиолипиновые антитела, волчаночный антикоагулянт);
- мигрень с локальными неврологическими симптомами в анамнезе;
- высокий риск артериальной тромбоэмболии в связи с наличием многочисленных факторов риска (см. ОСОБЫЕ УКАЗАНИЯ) или наличие одного из таких серьезных факторов риска: сахарный диабет с сосудистыми осложнениями; тяжелая АГ; выраженная дислипопротеинемия.
- Тяжелые заболевания печени, в том числе в анамнезе, если показатели функции печени не вернулись к норме.
- Почечная недостаточность тяжелой степени или ОПН.
- Опухоли печени (доброкачественные или злокачественные), в том числе в анамнезе.
- Известные или предполагаемые злокачественные опухоли (например половых органов или молочных желез), которые зависят от половых гормонов.
- Вагинальное кровотечение невыясненной этиологии.
Препарат Дарилия противопоказано применять одновременно с лекарственными средствами, содержащими омбитасвир/паритапревир/ритонавир и дасабувир (см. ОСОБЫЕ УКАЗАНИЯ и ВЗАИМОДЕЙСТВИЯ).
Побочные эффекты
наиболее серьезные побочные эффекты, связанные с применением КПК, описаны в разделе ОСОБЫЕ УКАЗАНИЯ.
При одновременном применении дроспиренона и этинилэстрадиола сообщалось о следующих побочных реакциях:
| Система органов | Частота возникновения побочных реакций | |||
|---|---|---|---|---|
| Часто (≥1/100, <1/10) | Нечасто (≥1/1000, <1/100) | Редко (≥1/10 000, <1/1000) | Неизвестно (невозможно оценить по имеющимся данным) | |
| Инфекции и инвазии | Кандидоз | |||
| Со стороны кровеносной и лимфатической системы | Анемия, тромбоцитопения | |||
| Со стороны иммунной системы | Аллергические реакции | Гиперчувствительность | ||
| Со стороны эндокринной системы | Эндокринные нарушения | |||
| Обмен веществ | Повышенный аппетит, анорексия, гиперкалиемия, гипонатриемия | |||
| Со стороны психики | Эмоциональная лабильность | Депрессия, нервозность, сонливость | Аноргазмия, бессонница | |
| Со стороны нервной системы | Головная боль | Головокружение, парестезия | Вертиго, тремор | |
| Со стороны органа зрения | Конъюнктивит, синдром сухого глаза, заболевания глаз | |||
| Со стороны сердца | Тахикардия | |||
| Со стороны сосудистой системы | Mигрень, варикозная болезнь, АГ | ВТЭ, артериальная тромбоэмболия, флебит, заболевания сосудов, обморок, носовое кровотечение | ||
| Со стороны пищеварительной системы | Тошнота | Боль в животе, рвота, диспепсия, метеоризм, гастрит, диарея | Вздутие живота, желудочно-кишечные нарушения, запор, ощущение переполненности живота, грыжа пищеводного отверстия диафрагмы, кандидоз ротовой полости, сухость полости рта | |
| Со стороны печени и желчевыводящих путей | Боль в области желчного пузыря, холецистит | |||
| Со стороны кожи и подкожной клетчатки | Акне, зуд, высыпания | Хлоазма, экзема, алопеция, угревой дерматит, сухость кожи, узловатая эритема, гипертрихоз, нарушения со стороны кожи, кожные стрии, контактный дерматит, фотодерматит, «узлы» на коже | Мультиформная эритема | |
| Со стороны скелетно-мышечной системы и соединительной ткани | Боль в спине, боль в конечностях, мышечные судороги | |||
| Со стороны репродуктивной системы и молочных желез | Боль в молочных железах, метроррагия*, аменорея | Вагинальный кандидоз, тазовая боль, увеличение молочных желез, фиброкистозная мастопатия, маточное/вагинальное кровотечение*, выделения из гениталий, приливы, вагинит, менструальные нарушения, дисменорея, гипоменорея, меноррагия, сухость вагины, сомнительные результаты мазка по Папаниколау, снижение либидо | Болезненный половой акт, вульвовагинит, посткоитальное кровотечение, кровотечение отмены, киста молочной железы, гиперплазия молочной железы, неоплазия молочной железы, полипы шейки матки, атрофия эндометрия, киста яичника, увеличение матки | |
| Общие расстройства | Астения, повышенное потоотделение, отек (генерализованный, периферический и отек лица) | Дискомфорт | ||
| Исследования | Увеличение массы тела | Уменьшение массы тела | ||
*Нерегулярность менструаций обычно исчезает при продолжении применения препарата.
Описание отдельных нежелательных реакций. Повышенный риск развития артериальных и венозных тромботических и тромбоэмболических осложнений, включая инфаркт миокарда, инсульт, транзиторную ишемическую атаку, венозный тромбоз и тромбоэмболию легочной артерии, был отмечен у женщин, принимавших КПК. Более подробная информация указана в разделе ОСОБЫЕ УКАЗАНИЯ.
Следующие серьезные побочные реакции были зарегистрированы у женщин, принимающих противозачаточные средства (описаны в разделе ОСОБЫЕ УКАЗАНИЯ):
- венозные тромбоэмболические расстройства;
- артериальные тромбоэмболические расстройства;
- АГ;
- опухоли печени;
- появление или ухудшение состояний, связь которых с приемом КПК не доказана: болезнь Крона, неспецифический язвенный колит, эпилепсия, миома матки, порфирия, системная красная волчанка, герпес беременных, хорея Сиденгама, гемолитико-уремический синдром, холестатическая желтуха;
- хлоазмы;
- острые или хронические нарушения функции печени могут потребовать отмены КПК до нормализации лабораторных маркеров функции печени;
- у женщин с наследственным ангионевротическим отеком экзогенные эстрогены могут вызвать или усилить симптомы ангионевротического отека.
Частота диагностирования рака молочной железы среди применяющих КПК женщин повышена незначительно. Поскольку рак молочной железы у женщин в возрасте до 40 лет отмечают редко, повышение является небольшим по сравнению с общим риском развития рака молочной железы. Причинно-следственная связь с приемом КПК не доказана (см. ПРОТИВОПОКАЗАНИЯ и ОСОБЫЕ УКАЗАНИЯ).
Взаимодействия. Прорывные кровотечения и/или уменьшение выраженности контрацептивного действия может возникнуть вследствие взаимодействия других лекарственных средств (индукторов ферментов) с пероральными контрацептивами (см. ВЗАИМОДЕЙСТВИЯ).
Сообщение о подозреваемых побочных реакциях. Сообщение о подозреваемых побочных реакциях в период постмаркетингового наблюдения очень важны. Это дает возможность осуществлять контроль за соотношением польза/риск для лекарственных средств. Медицинские работники должны сообщать о подозреваемых побочных реакциях.
Особые указания
решение о назначении препарата Дарилия следует принимать с учетом индивидуальных факторов риска женщины, которые существуют на данный момент, в том числе факторов риска развития ВТЭ, а также риска ВТЭ, связанного с приемом препарата Дарилия по сравнению с другими КПК (см. ПРОТИВОПОКАЗАНИЯ и ОСОБЫЕ УКАЗАНИЯ).
Предупреждение. При наличии любых состояний или факторов риска, указанных ниже, следует обсудить с женщиной целесообразность применения препарата Дарилия.
При обострении или первом возникновении любого из указанных ниже состояний или факторов риска женщине рекомендуется обратиться к врачу, который может принять решение о необходимости прекращения применения препарата.
В случае подозреваемой или подтвержденной ВТЭ или артериальной тромбоэмболии следует прекратить применение КГК. Если начата антикоагулянтная терапия, следует обеспечить альтернативную адекватную контрацепцию ввиду тератогенного влияния антикоагулянтов (кумарины).
Нарушения со стороны системы кровообращения. Риск ВТЭ. Применение любых КГК повышает риск развития ВТЭ у женщин по сравнению с теми, которые их не применяют. Применение препаратов, содержащих левоноргестрел, норгестимат или норэтистерон, ассоциируются с более низким риском возникновения ВТЭ. Применение других препаратов, таких как Дарилия, может приводить к повышению риска вдвое. Решение о применении препаратов, кроме имеющих низкий риск развития ВТЭ, следует принимать только после обсуждения с женщиной. Необходимо убедиться, что она осознает риск развития ВТЭ, ассоциированный с применением препарата Дарилия, степень влияния имеющихся у нее факторов риска и тот факт, что вероятность возникновения ВТЭ является самой высокой в течение первого года применения. По некоторым данным, риск развития ВТЭ может возрастать при восстановлении применения КГК после перерыва в 4 нед или дольше.
Среди женщин, которые не применяют КГК и не беременны, частота возникновения ВТЭ составляет примерно 2 случая на 10 000 женщин в год. Однако у любой отдельно взятой женщины уровень риска может быть значительно выше в зависимости от имеющихся у нее основных факторов риска (см. ниже).
Согласно оценкам1 частота развития ВТЭ среди женщин, применяющих КГК, содержащие дроспиренон, в течение одного года, составляет 9–12 случаев на 10 000 женщин в год. Это сопоставимо с показателем 62 у женщин, применяющих КГК, содержащих левоноргестрел. В обоих случаях зарегистрированное количество случаев ВТЭ меньше, чем ожидаемое количество случаев ВТЭ в период беременности или послеродовой период.
Венозная тромбоэмболия приводит к летальному исходу в 1–2% случаев.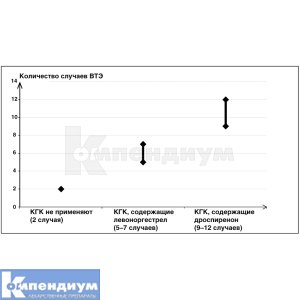
Рис. 1. Количество случаев ВТЭ на 10 000 женщин за один год.
1Эти показатели получены на основании всех данных эпидемиологических исследований с учетом относительных рисков, связанных с приемом различных КГК по сравнению с применением КГК, содержащих левоноргестрел.
2В среднем 5–7 случаев на 10 000 женщино-лет на основе расчета относительного риска применения КГК, содержащих левоноргестрел, по сравнению с таковым у женщин, которые не получают КГК (около 2,3–3,6 случаев).
Среди женщин, применяющих КГК, очень редко наблюдались тромбозы других кровеносных сосудов, например печеночных, мезентериальных, почечных, вен сетчатки и артерий.
Факторы риска развития ВТЭ. На фоне применения КГК риск развития венозных тромбоэмболических осложнений может значительно повышаться у женщин с дополнительными факторами риска, особенно при наличии множественных факторов риска (табл. 3).
Препарат Дарилия противопоказан женщинам со множественными факторами риска, в связи с чем пациентку можно отнести к группе высокого риска развития венозного тромбоза (см. ПРОТИВОПОКАЗАНИЯ). Если женщина имеет более одного фактора риска, его возрастание может быть выше, чем сумма рисков, ассоциированных с каждым отдельным фактором, поэтому следует принимать во внимание общий риск развития ВТЭ. КГК не следует назначать, если соотношение пользы/риска неблагоприятное (см. ПРОТИВОПОКАЗАНИЯ).
Таблица 3. Факторы развития ВТЭ
| Фактор риска | Примечание |
|---|---|
| Ожирение (индекс массы тела >30 кг/м2 | Риск значительно повышается при увеличении индекса массы тела пациентки. Особенно требует внимания наличие других факторов риска |
| Длительная иммобилизация, большое оперативное вмешательство, любая операция на нижних конечностях или в области малого таза, нейрохирургические вмешательства или обширная травма. Примечание: временная иммобилизация, включая воздушный перелет больше 4 ч, также может быть фактором риска возникновения ВТЭ, особенно для женщин с наличием других факторов риска развития ВТЭ | Рекомендуется прекратить применение препарата (в случае планового оперативного вмешательства, по крайней мере за 4 нед до него) и не начинать применение ранее чем через 2 нед после полного восстановления двигательной активности. Чтобы избежать нежелательной беременности, следует применять другие методы контрацепции. Антитромбическое лечение может быть целесообразным, если применение препарата Дарилия не было прекращено заранее |
| Семейный анамнез (ВТЭ у родного брата/сестры или родителей, особенно в относительно раннем возрасте, например до 50 лет) | При наличии наследственной предрасположенности перед применением любых КПК женщинам рекомендуется посоветоваться со специалистом |
| Другие медицинские состояния, связанные с ВТЭ | Рак, системная красная волчанка, гемолитико-уремический синдром, хроническая воспалительная болезнь кишечника (болезнь Крона или язвенный колит) и серповидно-клеточная анемия |
| Возраст | Особенно старше 35 лет |
Единого мнения относительно возможной роли варикозного расширения вен и поверхностного тромбофлебита в возникновении или прогрессировании венозного тромбоза нет.
Следует также учитывать, что риск тромбоэмболических осложнений повышается в период беременности и в первые 6 нед после родов (см. Применение в период беременности и кормления грудью).
Симптомы ВТЭ (тромбоза глубоких вен и тромбоэмболии легочной артерии). В случае возникновения соответствующих симптомов женщине следует срочно обратиться за медицинской помощью, а также проинформировать врача, что она принимает КПК.
Симптомы тромбоза глубоких вен могут включать:
- односторонний отек ноги и/или стопы или отек вдоль вены на ноге;
- боль или мучительная чувствительность в ноге, которая может ощущаться только при стоянии или ходьбе;
- ощущение жара в пораженной ноге; покраснение или изменение цвета кожи на ноге.
Симптомы эмболии легочной артерии могут включать:
- внезапный приступ одышки по неизвестной причине или учащенное дыхание;
- внезапный кашель, который может сопровождаться кровохарканьем;
- внезапная боль в грудной клетке;
- предобморочное состояние или головокружение;
- быстрое или нерегулярное сердцебиение.
Некоторые из этих симптомов (например одышка, кашель) являются неспецифическими и могут быть неправильно оценены как более распространенные или менее тяжелые симптомы (например инфекции дыхательных путей).
Другие признаки окклюзии сосудов могут включать внезапную боль, отек, острый живот и незначительный цианоз конечностей.
Если окклюзия происходит в сосудах глаза, симптомы могут варьировать от безболезненной нечеткости зрения до потери зрения. Иногда потеря зрения развивается почти мгновенно.
Риск возникновения артериальной тромбоэмболии. Эпидемиологические исследования показали, что КГК повышают риск развития артериальной тромбоэмболии (инфаркт миокарда) или нарушения мозгового кровообращения (например транзиторная ишемическая атака, инсульт). Артериальные тромбоэмболические осложнения могут приводить к летальному исходу.
Факторы риска развития артериальной тромбоэмболии. Риск развития артериальных тромбоэмболических осложнений или цереброваскулярных событий при применении КГК повышается у женщин с факторами риска, описанными в табл. 4. Препарат Дарилия противопоказан, если у женщины отмечают один серьезный или множественные факторы риска развития артериальной тромбоэмболии, на основании которых ее можно отнести к группе высокого риска развития артериального тромбоза (см. ПРОТИВОПОКАЗАНИЯ). Если у женщины выявлено более одного фактора риска, повышение риска может быть большим, чем сумма рисков, ассоциированных с каждым отдельным фактором, поэтому следует принимать во внимание общий риск развития артериальной тромбоэмболии. КГК не следует назначать, если соотношение пользы/риска неблагоприятное (см. ПРОТИВОПОКАЗАНИЯ).
Таблица 4. Факторы развития артериальной тромбоэмболии
| Фактор риска | Примечание |
|---|---|
| Возраст | Особенно старше 35 лет |
| Курение | Женщинам следует настойчиво рекомендовать отказаться от курения, если они хотят применять КПК. Женщинам в возрасте старше 35 лет, которые продолжают курить, следует настойчиво рекомендовать другой метод контрацепции |
| АГ | |
| Ожирение (индекс массы тела более 30 кг/м2) | Риск значительно повышается при увеличении индекса массы тела. Особенно требует внимания наличие других факторов риска |
| Семейный анамнез (артериальная тромбоэмболия у родного брата/сестры или родителей, особенно в относительно раннем возрасте, например до 50 лет) | При наличии наследственной предрасположенности перед применением любых КГК женщинам рекомендуется посоветоваться со специалистом |
| Мигрень | Повышение частоты или тяжести мигрени при применении КГК (что может быть продромальным состоянием перед цереброваскулярным событием) может требовать немедленного прекращения применения препарата |
| Другие медицинские состояния, связанные с побочными эффектами со стороны сосудов | Сахарный диабет, гипергомоцистеинемия, пороки клапанов сердца и фибрилляция предсердий, дислипопротеинемия и системная красная волчанка |
Симптомы артериальной тромбоэмболии. В случае возникновения соответствующих симптомов женщине следует срочно обратиться за медицинской помощью, а также проинформировать врача о том, что она принимает КГК.
Симптомы цереброваскулярного расстройства могут включать:
- внезапное онемение лица, руки или ноги, особенно с одной стороны тела;
- внезапные проблемы при ходьбе, головокружение, потеря равновесия или координации;
- внезапная спутанность сознания, проблемы с речью или ее восприятием;
- внезапные проблемы со зрением одного или обоих глаз;
- неожиданно выраженная или длительная головная боль без определенной причины;
- потеря сознания или обморок, с судорогами или без таковых.
Временный характер симптомов может свидетельствовать о транзиторной ишемической атаке.
Симптомы инфаркта миокарда могут включать:
- боль, дискомфорт, давление, тяжесть, ощущение сдавливания или распирания в груди, руке или ниже грудины;
- дискомфортное ощущение с иррадиацией в спину, челюсть, горло, руки, живот;
- ощущение переполненности желудка, нарушение пищеварения или удушье;
- усиленное потоотделение, тошнота, рвота и головокружение;
- выраженная слабость, беспокойство или одышка;
- учащенное или нерегулярное сердцебиение.
Опухоли. Результаты некоторых эпидемиологических исследований указывают на дополнительное повышение риска развития рака шейки матки при длительном (более 5 лет) применении КПК, однако окончательно не выяснено, насколько результаты исследований учитывают половое поведение и сопутствующие факторы риска, например инфицирование вирусом папилломы человека.
Метаанализ данных 54 эпидемиологических исследований свидетельствует о незначительном повышении относительного риска (ОР=1,24) развития рака молочной железы у женщин, применяющих КПК. Этот повышенный риск постепенно исчезает в течение 10 лет после окончания приема КПК.
Поскольку рак молочной железы у женщин в возрасте до 40 лет отмечается редко, увеличение количества случаев диагностирования рака молочной железы у женщин, применяющих или недавно применявших КПК, является незначительным по сравнению с общим риском развития рака молочной железы, а известные результаты исследований не подтверждают наличия причинно-следственной связи. Повышение риска может быть обусловлено как более ранней диагностикой рака молочной железы у женщин, применяющих КПК, так и биологическим действием КПК или сочетанием обоих факторов. Отмечена тенденция к тому, что рак молочной железы, выявленный у женщин, когда-либо принимавших КПК, клинически менее выражен, чем у тех, кто никогда не принимал КПК.
В редких случаях у женщин, применяющих КПК, отмечали доброкачественные, а еще реже — злокачественные опухоли печени. В отдельных случаях эти опухоли приводили к опасному для жизни внутрибрюшному кровотечению. В случае возникновения выраженной боли в эпигастральной области, увеличения печени или признаков внутрибрюшного кровотечения при дифференциальной диагностике следует учитывать возможность наличия опухоли печени у женщин, принимающих КПК.
Прием КПК в высоких дозах (50 мкг этинилэстрадиола) снижает риск развития рака эндометрия и яичника. Касается ли это КПК, окончательно не установлено.
Другие состояния. Депрессивное настроение и депрессия являются частыми побочными реакциями при применении гормональных контрацептивов (см. ПОБОЧНЫЕ ЭФФЕКТЫ). Депрессия может быть тяжелой и является известным фактором риска суицидального поведения и суицида. Женщин следует информировать о необходимости обратиться к врачу в случае перепадов настроения и симптомов депрессии, даже если они возникают вскоре после начала лечения.
Прогестероновый компонент препарата является антагонистом альдостерона с калийсберегающими свойствами. В большинстве случаев не отмечается увеличения содержания калия в плазме крови. Однако в клиническом исследовании у некоторых пациентов с легкими и умеренными нарушениями функции почек и в случае сопутствующего применения калийсберегающих лекарственных средств при приеме дроспиренона отмечено небольшое увеличение содержания калия в плазме крови. Таким образом, рекомендуется контролировать содержание калия в плазме крови во время первого цикла приема препарата у пациентов с почечной недостаточностью. Указанным пациенткам также рекомендовано перед началом применение препарата удерживать уровень калия сыворотки крови не выше верхнего предела нормы, особенно при одновременном применении калийсберегающих препаратов (см. ВЗАИМОДЕЙСТВИЯ).
Женщинам с гипертриглицеридемией или тем, кто имеет это нарушение в семейном анамнезе, следует учитывать возможный повышенный риск развития панкреатита при применении КПК.
Хотя незначительное повышение АД было описано у многих женщин, принимающих КПК, клинически значимое повышение АД является единичным явлением. Лишь в редких случаях необходимо немедленное прекращение приема КПК. Если во время применения КПК в случае существующей ранее АГ значения АД постоянно повышены или пациент с значительно повышенным АД адекватно не реагирует на гипотензивную терапию, прием КПК следует прекратить. В случае необходимости применение КПК может быть продлено, если с помощью антигипертензивной терапии достигнуты нормальные значения АД.
Сообщалось о возникновении или обострении указанных ниже заболеваний в период беременности и при применении КПК, но их взаимосвязь с применением КПК не является окончательно установленной: желтуха и/или зуд, связанный с холестазом; образование камней в желчном пузыре; порфирия; системная красная волчанка, гемолитико-уремический синдром; хорея Сиденгама; герпес беременных; потеря слуха, связанная с отосклерозом.
У женщин с наследственным ангионевротическим отеком экзогенные эстрогены могут вызвать или усилить симптомы ангионевротического отека.
При острых или хронических нарушениях функции печени может возникнуть необходимость в прекращении применения КПК, пока показатели функции печени не вернутся к норме.
При рецидиве холестатической желтухи и/или зуда, вызванного холестазом, которые впервые возникли в период беременности или предыдущего приема половых гормонов, применение КПК следует прекратить.
Хотя КПК могут влиять на периферическую инсулинорезистентность и толерантность к глюкозе, нет данных относительно необходимости изменять терапевтический режим для женщин с сахарным диабетом, принимающих низкодозированные КПК (содержащие ≤0,05 мг этинилэстрадиола). Однако женщины с сахарным диабетом должны быть под постоянным наблюдением в течение всего периода применения КПК.
Известны случаи возникновения болезни Крона и язвенного колита на фоне применения КПК. Также сообщалось об ухудшении состояния при эндогенной депрессии и эпилепсии на фоне применения КПК.
Иногда может возникать хлоазма, особенно у женщин с хлоазмой беременных в анамнезе. Женщины, склонные к возникновению хлоазмы, должны избегать длительного воздействия прямых солнечных лучей или ультрафиолетового облучения во время приема КПК.
Вспомогательные вещества. 1 активная таблетка содержит 48,53 мг лактозы моногидрата, 1 таблетка плацебо содержит 37,26 мг лактозы безводной. Пациенткам с редкой наследственной непереносимостью галактозы, лактазной недостаточностью Лаппа или нарушением всасывания глюкозы-галактозы, которые находятся на безлактозной диете, следует учитывать указанное количество лактозы.
Препарат Дарилия содержит соевый лецитин (0,07 мг в 1 таблетке), поэтому пациенткам с гиперчувствительностью к арахису или сое не следует принимать этот препарат.
Таблетки плацебо содержат краситель «желтый запад» (Е110), который может вызвать аллергические реакции.
Медицинское обследование. Перед началом применения или в случае повторного назначения препарата Дарилия необходимо тщательно изучить анамнез пациентки, включая семейный, провести медицинское обследование и исключить беременность. Следует измерить АД, провести объективное исследование, учитывая противопоказания (см. ПРОТИВОПОКАЗАНИЯ) и особенности применения (см. ОСОБЫЕ УКАЗАНИЯ). Важно обратить внимание женщин на риск возникновения венозного и артериального тромбоза, включая риск при приеме препарата Дарилия по сравнению с таковым при применении других КПК, относительно симптомов ВТЭ и артериальной тромбоэмболии, известных факторов риска и действий, которые необходимо осуществить при подозрении на тромбоз.
Пациенткам рекомендуется внимательно прочитать инструкцию по применению лекарственного средства и придерживаться рекомендаций, содержащихся в ней.
Частота и характер медицинских осмотров должны основываться на существующих нормах медицинской практики с учетом индивидуальных особенностей каждой женщины.
Следует предупредить пациентку, что гормональные контрацептивы не защищают от заражения ВИЧ-инфекцией (СПИД) и других заболеваний, передающихся половым путем.
Снижение эффективности. Эффективность КПК может снижаться в случае пропуска приема активных таблеток, расстройств со стороны ЖКТ в период приема активных таблеток (см. ПРИМЕНЕНИЕ) или при одновременном применении других лекарственных средств (см. ВЗАИМОДЕЙСТВИЯ).
Ухудшение контроля цикла. При применении КПК возможны межменструальные кровотечения (небольшие кровянистые выделения или прорывные кровотечения), особенно в первые месяцы применения препарата. Учитывая это, обследование на предмет появления любого нерегулярного кровотечения следует проводить только после периода адаптации к препарату, который составляет 3 менструальных цикла.
Если нерегулярные кровотечения продолжаются или случаются после нескольких нормальных циклов, необходимо рассмотреть вопрос о негормональных причинах и провести соответствующие диагностические мероприятия (при необходимости — кюретаж) для исключения злокачественных новообразований или беременности.
У некоторых женщин может не наступить кровотечение отмены во время перерыва в приеме препарата. Если КПК принимали согласно указаниям, описанным в разделе ПРИМЕНЕНИЕ, то беременность маловероятна. Однако если применение контрацептива осуществлялось нерегулярно или если кровотечение отмены отсутствует в течение 2 циклов, то перед продолжением приема КПК необходимо исключить беременность.
Повышение уровня АлАТ. Во время клинических исследований с участием пациентов, проходивших курс лечения по поводу вирусного гепатита С, с помощью лекарственных средств, содержащих омбитасвир/паритапревир/ритонавир и дасабувир, с рибавирином или без него, было отмечено значительное повышение уровня трансаминаз (АлАТ), что превышало верхнюю границу нормы в 5 раз. Это происходило со значительно большей частотой у женщин, получавших лекарственные средства, содержащие этинилэстрадиол, такие как КГК (см. ПРОТИВОПОКАЗАНИЯ и ВЗАИМОДЕЙСТВИЯ).
Применение в период беременности и кормления грудью.
Беременность. Препарат Дарилия противопоказан в период беременности.
В случае наступления беременности во время применения препарата Дарилия его прием следует немедленно прекратить. Однако результаты эпидемиологических исследований не указывают на повышение риска появления врожденных пороков у детей, рожденных женщинами, которые принимали пероральные контрацептивы до беременности, так же, как и на существование тератогенного действия при непреднамеренном приеме пероральных контрацептивов в течение беременности. В исследованиях на животных были выявлены побочные эффекты в период беременности и лактации (см. ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА). Основываясь на этих данных, нельзя исключить побочных эффектов, связанных с гормональным воздействием сочетания действующих веществ. Однако общий опыт применения КПК во время беременности не свидетельствует о существующем нежелательном воздействии у человека.
Данные по применению препарата Дарилия в период беременности слишком ограничены для того, чтобы можно было сделать выводы относительно негативного влияния препарата Дарилия на течение беременности, здоровье плода или новорожденного. В настоящее время нет никаких соответствующих эпидемиологических данных. При восстановлении применения препарата Дарилия следует учитывать повышение риска развития ВТЭ в послеродовой период (см. ПРИМЕНЕНИЕ, ОСОБЫЕ УКАЗАНИЯ).
Период кормления грудью. КПК могут влиять на кормление грудью, поскольку под их влиянием может уменьшаться количество грудного молока, а также изменяться его состав. Исходя из этого, КПК не рекомендуется принимать в период кормления грудью. Небольшое количество контрацептивных стероидов и/или их метаболиты могут проникать в грудное молоко во время применения КПК. Это количество может повлиять на ребенка.
Фертильность. Препарат Дарилия показан для предотвращения беременности. Информацию по восстановлению фертильности см. в разделе ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА.
Способность влиять на скорость реакции при управлении транспортными средствами или другими механизмами. Не проводили исследований влияния на способность управлять транспортными средствами или работать с другими механизмами. У женщин, принимающих КПК, не сообщалось о влиянии на способность управлять транспортными средствами или работать с другими механизмами.
Дети. Препарат показан для применения по назначению врача только после наступления устойчивых менструаций.
Взаимодействия
следует ознакомиться с информацией о лекарственном средстве, применяемом одновременно, для выявления потенциальных взаимодействий.
Фармакодинамические взаимодействия. Одновременное применение с лекарственными средствами, содержащими омбитасвир/паритапревир/ритонавир и дасабувир, с рибавирином или без него, может повысить риск повышения уровня АлАТ (см. ПРОТИВОПОКАЗАНИЯ и ОСОБЫЕ УКАЗАНИЯ). Поэтому прежде чем начать лечение с помощью этой комбинации лекарственных средств, лицам, принимающим препарат Дарилия, необходимо перейти на альтернативный метод контрацепции (например контрацепция с помощью препаратов, содержащих только прогестаген, или негормональных методов). Применение Дарилии можно восстановить через 2 нед после завершения лечения с помощью этой комбинации лекарственных средств.
Фармакокинетические взаимодействия
Влияние других лекарственных средств на препарат Дарилия. Взаимодействия возможны с лекарственными средствами, которые индуцируют микросомальные ферменты. Это приводит к увеличению клиренса половых гормонов, что, в свою очередь, изменяет характер менструального кровотечения и/или вызывает снижение эффективности контрацептива.
Терапия. Индукция ферментов может быть выявлена через несколько дней лечения. Максимальная индукция ферментов в целом наблюдается через несколько недель. После отмены лечения индукция ферментов может длиться около 4 нед.
Краткосрочное лечение. Женщины, которые принимают лекарственные средства, индуцирующие ферменты, должны временно использовать барьерный или другой метод контрацепции дополнительно к КПК. Барьерный метод следует применять в течение всего срока лечения соответствующим препаратом и еще в течение 28 дней после прекращения его применения.
Если терапия препаратом-индуктором начинается в период применения последних таблеток КПК из текущей упаковки, то прием активных таблеток из следующей упаковки КПК следует начать сразу после окончания активных таблеток в предыдущей упаковке, пропустив прием таблеток плацебо.
Долгосрочное лечение. Женщинам при долгосрочной терапии действующими веществами, которые индуцируют ферменты печени, рекомендуется барьерный или другой соответствующий негормональный метод контрацепции.
Нижеприведенные взаимодействия были зафиксированы согласно опубликованным данным.
Действующие вещества, увеличивающие клиренс КПК (снижение эффективности КПК через индукцию ферментов), например барбитураты, бозентан, карбамазепин, фенитоин, примидон, рифампицин; препараты, применяемые при ВИЧ-инфекции: ритонавир, невирапин и эфавиренз; также, возможно, фелбамат, гризеофульвин, окскарбазепин, топирамат и растительные лекарственные средства, содержащие экстракт зверобоя (Hypericum perfiratum).
Действующие вещества с непостоянным воздействием на клиренс КПК. При одновременном применении с КПК большое количество комбинаций ингибиторов протеазы ВИЧ и ненуклеозидных ингибиторов обратной транскриптазы, включая комбинации с ингибиторами вируса гепатита С, могут повышать или снижать концентрацию эстрогена или прогестинов в плазме крови. Совокупное влияние таких изменений может быть клинически значимым в некоторых случаях.
Поэтому для выявления потенциальных взаимодействий и получения любых других рекомендаций следует ознакомиться с информацией по медицинскому применению лекарственного средства для лечения ВИЧ/вирусного гепатита С, которое принимается одновременно. При наличии каких-либо сомнений женщинам дополнительно следует использовать барьерный метод контрацепции при терапии ингибиторами протеазы или ингибиторами ненуклеозидной обратной транскриптазы.
Субстанции, приводящие к снижению клиренса КПК (ингибиторы ферментов). Клиническая значимость возможных взаимодействий с ингибиторами ферментов все еще остается невыясненной.
Одновременное применение с сильными ингибиторами CYP 3A4 может повысить плазменные концентрации эстрогена или прогестина, или обоих действующих веществ.
В исследовании применение многократных доз дроспиренона (3 мг/сут)/этинилэстрадиола (0,02 мг) сочетанно с мощным ингибитором CYP 3A4 кетоконазолом в течение 10 дней приводило к повышению AUC (0–24 ч) дроспиренона и этинилэстрадиола в 2,7 и 1,4 раза соответственно.
При сочетанном применении эторикоксиба в дозе 60 и 120 мг/сут вместе с комбинированными гормональными контрацептивами, содержащими 0,035 мг этинилэстрадиола, наблюдалось повышение концентрации этинилэстрадиола в плазме крови в 1,4 и 1,6 раза соответственно.
Влияние препарата Дарилия на другие лекарственные средства. КПК могут влиять на метаболизм других препаратов. Учитывая это, КПК могут изменять концентрацию действующих веществ в плазме крови и тканях — как повышать (например циклоспорин), так и снижать (например ламотриджин).
На основании исследований in vivo у женщин-добровольцев, принимавших омепразол, симвастатин и мидазолам в качестве субстратов-маркеров, влияние дроспиренона в дозе 3 мг на метаболизм других лекарственных средств, опосредованных цитохромом Р450, маловероятно.
Клинические данные свидетельствуют о том, что этинилэстрадиол подавляет клиренс субстратов фермента CYP 1A2, что приводит к слабому (например теофиллин) или умеренному (например тизанидин) повышению их концентрации в плазме крови.
Другие формы взаимодействия. У пациентов без почечной недостаточности одновременное применение дроспиренона и ингибиторов АПФ или НПВП не оказывает существенного влияния на уровень калия в плазме крови. Однако одновременное применение препарата Дарилия и антагонистов альдостерона или калийсберегающих диуретиков не изучали. В этом случае необходимо исследование уровня калия в плазме крови в течение первого цикла приема препарата (см. ОСОБЫЕ УКАЗАНИЯ).
Лабораторные исследования. Применение контрацептивов может влиять на результаты отдельных лабораторных тестов, включая биохимические показатели функции печени, щитовидной железы, надпочечников и почек, а также уровни транспортных белков плазмы крови, таких как кортикостероидсвязывающий глобулин и фракции липидов/липопротеинов, показатели углеводного обмена, коагуляции и фибринолиза. Изменения обычно происходят в пределах лабораторных норм.
Обладая умеренной антиминералокортикоидной активностью, дроспиренон повышает активность ренина и альдостерона в плазме крови.
Передозировка
до настоящего времени нет никаких данных о передозировке препарата Дарилия. На основании общих данных о применении КПК выделяют такие симптомы, которые могут отмечать при передозировке: тошнота, рвота, кровотечение отмены. Каких-либо антидотов не существует, лечение симптоматическое.
Условия хранения
при температуре не выше 25 °C в оригинальной упаковке для защиты от воздействия света. Хранить в недоступном для детей месте.