Цебопим (Cebopime)
Цебопим инструкция по применению
Состав
Цефепим - 1 г
Фармакологические свойства
фармакодинамика. Цефепим действует путем угнетения синтеза ферментов стенки бактерии. Препарат обладает широким спектром действия относительно грамположительных и грамотрицательных бактерий, высокой резистентностью к гидролизу большинством β-лактамаз, имеет малое сродство к β-лактамазам, кодирующимся хромосомными генами, быстро проникает в грамотрицательные бактериальные клетки.
Цебопим активен относительно следующих микроорганизмов:
грамположительные аэробы: Staphylococcus aureus (включая штаммы, продуцирующие β-лактамазу); Staphylococcus epidermidis (включая штаммы, продуцирующие β-лактамазу); другие штаммы стафилококков, включая S. hominis, S. saprophyticus; Streptococcus pyogenes (стрептококки группы А); Streptococcus agalactiae (стрептококки группы В); Streptococcus pneumoniae (включая штаммы со средней резистентностью к пенициллину — МИК 0,1–1 мкг/мл); другие β-гемолитические стрептококки (группы C, G, F), S. bovis (группа D), стрептококки группы Viridans.
Большинство штаммов энтерококков, например Enterococcus faecalis, и стафилококки, резистентные к метициллину, резистентны к большинству цефалоспориновых антибиотиков, включая цефепим;
грамотрицательные аэробы: Pseudomonas sp., включая P. aeruginosa, P. putida, P. stutzeri; Escherichia coli, Klebsiella sp., включая K. pneumoniae, K. oxytoca, K. ozaenae; Enterobacter sp., включая E. cloacae, E. aerogenes, E. sakazakii; Proteus sp., включая P. mirabilis, P. vulgaris; Acinetobacter calcoaceticus (subsp. anitratus, lwoffi); Aeromonas hydrophila; Capnocytophaga sp.; Citrobacter sp., включая C. diversus, C. freundii; Campylobacter jejuni; Gardnerella vaginalis; Haemophilus ducreyi; Haemophilus influenzae (включая штаммы, продуцирующие β-лактамазу); Haemophilus parainfluenzae; Hafnia alvei; Legionella sp.; Morganella morganii; Moraxella catarrhalis (Branhamella catarrhalis) (включая штаммы, продуцирующие β-лактамазу); Neisseria gonorrhoeae (включая штаммы, продуцирующие β-лактамазу); Neisseria meningitidis; Providencia sp. (включая P. retigeri, P. stuartii); Salmonella sp.; Serratia (включая S. marcescens, S. liquefaciens); Shigella sp.; Yersinia enterocolitica.
Цефепим неактивен относительно некоторых штаммов Xanthamonas maltophilia (Pseudomonas maltophilia);
анаэробы: Bacteroides sp., включая B. melaninogenicus и другие микроорганизмы ротовой полости, относящиеся к Bacteroides; Clostridium perfringens; Fusobacterium sp.; Mobiluncus sp.; Peptostreptococcus sp.; Veillonella sp. (цефепим неактивен в отношении Bacteroides fragilis и Clostridium difficile).
Фармакокинетика. T½ препарата около 2 ч. У здоровых людей кумуляции препарата в организме не отмечали.
Метаболизируется цефепим в N-метилпирролидин, который быстро превращается в оксид N-метилпирролидина. Общий клиренс составляет 120 мл/мин. Препарат в основном выделяется почками (средний почечный клиренс составляет 110 мл/мин). В моче выявляют около 85% введенной дозы в виде неизмененного цефепима, 1% N-метилпирролидина, около 6,8% оксида N-метилпирролидина и около 2,5% эпимера цефепима. Связывание цефепима с белками плазмы крови не зависит от концентрации препарата в плазме крови и составляет <19%.
Цефепим хорошо распределяется в организме и достигает терапевтической концентрации в моче, желчи, перитонеальной жидкости, слизистом секрете бронхов, мокроте, предстательной железе, аппендиксе и желчном пузыре. Концентрации цефепима в плазме крови у взрослых здоровых мужчин после одноразового в/в или в/м введения приведены в табл. 1.
Таблица 1 Средние концентрации цефепима в плазме крови, мкг/мл
| Доза цефепима | Время, ч | |||||
|---|---|---|---|---|---|---|
| 0,5 | 1 | 2 | 4 | 8 | 12 | |
| В/в введение | ||||||
| 500 мг | 38,2 | 21,6 | 11,6 | 5,0 | 1,4 | 0,2 |
| 1 г | 78,7 | 44,5 | 24,3 | 10,5 | 2,4 | 0,6 |
| 2 г | 163,1 | 85,8 | 44,8 | 19,2 | 3,9 | 1,1 |
| В/м введение | ||||||
| 500 мг | 8,2 | 12,5 | 12,0 | 6,9 | 1,9 | 0,7 |
| 1 г | 14,8 | 25,9 | 26,3 | 16,0 | 4,5 | 1,4 |
| 2 г | 36,1 | 49,9 | 51,3 | 31,5 | 8,7 | 2,3 |
У пациентов с почечной недостаточностью T½ цефепима увеличивается. У пациентов с тяжелыми нарушениями функции почек, находящихся на диализе, T½ составляет 13 ч для гемодиализа и 19 ч — для перитонеального диализа.
Фармакокинетика цефепима при нарушении функции печени или муковисцидозе не изменяется. Для таких пациентов нет необходимости в коррекции дозы.
Дети. У детей в возрасте 2 мес–11 лет после однократной в/в инъекции общий клиренс и объем распределения в равновесном состоянии составляет 3,3±1,0 и 0,3±0,1 л/кг соответственно. Около 60,4±30,4% введенной дозы цефепима выделяется в неизмененном виде с мочой, почечный клиренс составляет 2,0±1,1 мл/мин/кг. После в/м введения Cmax цефепима в плазме крови в равновесном состоянии составляет в среднем 68 мкг/мл через 0,75 ч. Через 8 ч после в/м введения концентрация цефепима в плазме крови составляет 6 мкг/мл. Абсолютная биодоступность после в/м инъекции цефепима составляет в среднем 82%. Возраст и пол пациента не влияют на клиренс препарата (табл. 2).
Таблица 2 Концентрации препарата в СМЖ и в плазме крови у детей с бактериальным менингитом
| Время после введения, ч | Концентрация в плазме крови, мкг/мл* | Концентрация в СМЖ, мкг/мл* | Отношение концентрации в СМЖ/плазме крови* |
|---|---|---|---|
| 0,5 | 67,7±51,2 | 5,7±0,14 | 0,12±0,14 |
| 1 | 44,1±7,8 | 4,3±1,5 | 0,10±0,04 |
| 2 | 23,9±12,9 | 3,6±2,0 | 0,17±0,09 |
| 4 | 11,7±15,7 | 4,2±1,1 | 0,87±0,56 |
| 8 | 4,9±5,9 | 3,3±2,8 | 1,02±0,64 |
*Возраст 3,1 мес–12 лет со стандартным отклонением в возрасте ±3 года. Доза препарата 50 мг/кг массы тела при в/в введении на протяжении 5–20 мин каждые 8 ч. Концентрация в плазме крови и СМЖ определялась в конце введения на 2-й или 3-й день лечения препаратом.
Показания Цебопим
взрослые. Инфекции, вызванные чувствительной к препарату микрофлорой:
- дыхательных путей, в том числе пневмония, бронхит;
- кожи и подкожной клетчатки;
- интраабдоминальные инфекции, в том числе перитонит и инфекции желчевыводящих путей;
- гинекологические инфекции;
- септицемия.
Эмпирическая терапия нейтропенической лихорадки.
Профилактика послеоперационных осложнений в интраабдоминальной хирургии.
- Дети: пневмония;
- инфекции кожи и подкожной клетчатки;
- септицемия;
- эмпирическая терапия нейтропенической лихорадки;
- бактериальный менингит.
Применение Цебопим
перед применением препарата необходимо провести пробу на переносимость.
Дозы и путь введения варьируют в зависимости от чувствительности, локализации и вида микроорганизмов; степени тяжести инфекции, а также возраста и функционального состояния организма пациента. Обычно взрослым препарат вводят по 1 г в/в или в/м через каждые 12 ч. Курс лечения составляет 7–10 дней. При тяжелых инфекциях может быть необходимо более длительное лечение.
Рекомендации относительно дозирования препарата Цебопим для взрослых приведены в табл. 3.
Таблица 3 Рекомендации относительно дозирования препарата Цебопим для взрослых
| Инфекции мочевыводящих путей легкой и средней степени тяжести | 500 мг–1 г в/в или в/м | Каждые 12 ч |
| Другие инфекции легкой и средней степени тяжести | 1 г в/в или в/м | Каждые 12 ч |
| Тяжелые инфекции | 2 г в/в | Каждые 12 ч |
| Очень тяжелые и угрожающие жизни инфекции | 2 г в/в | Каждые 8 ч |
Пациентам в возрасте старше 65 лет с нормальной функцией почек нет необходимости в коррекции дозы препарата.
Профилактика возможного инфицирования при проведении хирургических операций. 2 г препарата вводят в/в капельно на протяжении 30 мин за 1 ч до начала хирургической операции. После окончания введения дополнительно вводят 500 мг метронидазола в/в. Р-р метронидазола не следует вводить одновременно с препаратом Цебопим. В случае сочетанного применения каждый антибиотик вводят в отдельных системах. При применении одной системы для двух препаратов перед инфузией метронидазола систему следует промыть.
Во время продолжительных (>12 ч) хирургических операций через 12 ч после первой дозы рекомендуют повторное введение равной дозы препарата Цебопим с последующим введением метронидазола.
Дети в возрасте 1–2 мес. Применяют только по жизненным показаниям. Вводят в дозе 30 мг/кг массы тела каждые 12 или 8 ч. При применении терапии Цебопимом у детей с массой тела <40 кг состояние этих пациентов требует постоянного наблюдения.
Дети в возрасте старше 2 мес. Максимальная доза для детей не должна превышать рекомендуемую для взрослых. У детей с массой тела <40 кг рекомендуемая доза составляет 50 мг/кг массы тела каждые 12 ч (при фебрильной нейтропении и бактериальном менингите — каждые 8 ч). Продолжительность терапии составляет 7–10 дней, тяжелые инфекции могут требовать более продолжительного лечения.
Детям с массой тела ≥40 кг Цебопим назначают, как и взрослым.
Нарушение функции почек. У пациентов с нарушением функции почек (клиренс креатинина <30 мл/мин) необходимо корректировать режим введения препарата. При этом начальная доза Цебопима равняется дозе для пациентов с нормальной функцией почек. Рекомендуемые поддерживающие дозы препарата Цебопим приведены в табл. 4.
Таблица 4 Рекомендуемые поддерживающие дозы препарата Цебопим
| Клиренс креатинина, мл/мин | Рекомендуемые поддерживающие дозы | |||
|---|---|---|---|---|
| Инфекции мочевыводящих путей легкой и средней степени | Другие инфекции легкой и средней степени | Тяжелые инфекции | Очень тяжелые и угрожающие жизни инфекции | |
| >50 | 500 мг каждые 12 ч | 1 г каждые 12 ч | 2 г каждые 12 ч | 2 г каждые 8 ч |
| Обычное дозирование с учетом тяжести инфекции, коррекции дозы не требуется | ||||
| 30–50 | 500 мг каждые 24 ч | 1 г каждые 24 ч | 2 г каждые 24 ч | 2 г каждые 12 ч |
| 11–29 | 500 мг каждые 24 ч | 500 мг каждые 24 ч | 1 г каждые 24 ч | 2 г каждые 24 ч |
| ≤10 | 250 мг каждые 24 ч | 250 мг каждые 24 ч | 500 мг каждые 24 ч | 1 г каждые 24 ч |
| Гемодиализ | 500 мг каждые 24 ч | 500 мг каждые 24 ч | 500 мг каждые 24 ч | 500 мг каждые 24 ч |
Клиренс креатинина определяют по формуле:
Мужчины:
Женщины: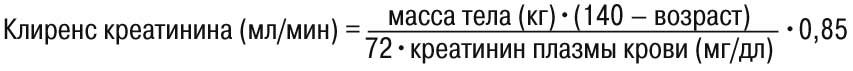
При гемодиализе в течение 3 ч из организма выводится около 68% введенной дозы препарата. После каждого сеанса гемодиализа необходимо вводить повторную дозу, равную начальной. При беспрерывном амбулаторном перитонеальном диализе препарат можно применять в обычных рекомендуемых дозах в зависимости от тяжести инфекции, с интервалом между введениями разовой дозы 48 ч.
При нарушении функции почек у детей рекомендуют снижение дозы или увеличение интервала между введениями, как указано в табл. 4.
Расчеты показателей клиренса креатинина у детей: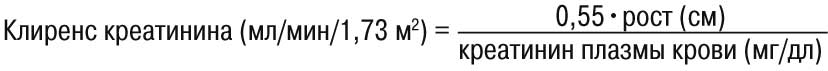
или
Введение препарата. Цебопим вводят в/в или глубоко в/м в большую мышечную массу (например в верхний наружный квадрант ягодицы).
В/в введение. Данный путь введения предпочтителен для пациентов с тяжелыми, угрожающими для жизни инфекциями.
При в/в введении Цебопим растворяют в 5 или 10 мл стерильной воды для инъекций, 5% р-ра глюкозы или 0,9% р-ра натрия хлорида, как указано в табл. 5. Готовый р-р вводят медленно на протяжении 3–5 мин или через систему для в/в введения.
В/м введение. Цебопим растворяют в стерильной воде для инъекций, 0,9% р-ре натрия хлорида, 5% р-ре декстрозы для инъекций, бактериостатической воде для инъекций с парабеном или бензиловым спиртом, 0,5% или 1% р-ре лидокаина гидрохлорида в концентрациях, указанных ниже (см. табл. 5).
При применении лидокаина как растворителя перед введением необходимо провести пробу на переносимость.
Таблица 5 Концентрации разведения Цебопима
| Концентрация | Объем р-ра для разведения, мл | Приблизительный объем полученного р-ра, мл | Приблизительная концентрация цефепима, мг/мл |
|---|---|---|---|
| В/в введение | |||
| 500 мг/флакон | 5 | 5,7 | 90 |
| 1 г/флакон | 10 | 11,4 | 90 |
| 2 г/флакон | 10 | 12,8 | 160 |
| В/м введение | |||
| 500 мг/флакон | 1,5 | 2,2 | 230 |
| 1 г/флакон | 3,0 | 4,4 | 230 |
Противопоказания
повышенная чувствительность к цефепиму или L-аргинину, к антибиотикам цефалоспоринового ряда, пенициллинам или другим β-лактамным антибиотикам.
Побочные эффекты
отмечают редко.
Аллергические реакции: сыпь, зуд, повышение температуры тела, анафилактические реакции (в том числе анафилактический шок, ангионевротический отек), повышение температуры тела.
Со стороны пищеварительной системы: диарея, тошнота, рвота, кандидоз слизистой оболочки ротовой полости, запор, боль в животе, диспепсия, псевдомембранозный колит.
Со стороны сердечно-сосудистой системы: боль в груди, вазодилатация, тахикардия.
Со стороны дыхательной системы: кашель, боль в горле, одышка.
Со стороны ЦНС: головная боль, головокружение, бессонница, парестезии, беспокойство, спутанность сознания, судороги, миоклония, эпилептиформные припадки, энцефалопатия (потеря сознания, галлюцинации, ступор, кома).
Изменения лабораторных показателей (транзиторные): повышение уровня АлАТ, АсАТ, ЩФ, общего билирубина, анемия, эозинофилия, увеличение протромбинового времени или активированного частичного тромбопластинового времени и положительный результат теста Кумбса без гемолиза. Транзиторное повышение уровня азота мочевины и/или креатинина в плазме крови, транзиторная тромбоцитопения, лейкопения и нейтропения.
Со стороны мочеполовой системы: вагинит, генитальный зуд, почечная недостаточность.
Другие: астения, вагинит, периферические отеки, боль в спине, гипергидроз.
Местные реакции: при в/в введении — флебит и воспаление; при в/м введении — воспаление или боль в месте инъекции.
Возможны побочные реакции, характерные для антибиотиков группы цефалоспоринов: синдром Стивенса — Джонсона, мультиформная эритема, токсический эпидермальный некролиз, токсическая нефропатия, апластическая анемия, гемолитическая анемия, кровотечения, нарушение функции печени, холестаз, панцитопения.
Особые указания
гиперчувствительность. Перед применением препарата необходимо установить, отмечались ли ранее у пациента реакции гиперчувствительности немедленного типа на цефепим, цефалоспорины, пенициллины или другие β-лактамные антибиотики. Антибиотики следует назначать с осторожностью всем больным с любыми формами аллергии, особенно на лекарственные препараты. При появлении аллергической реакции применение препарата следует прекратить. Серьезные реакции гиперчувствительности немедленного типа могут требовать применения эпинефрина и других видов терапии.
У пациентов с высоким риском развития тяжелых инфекций (например у лиц с трансплантацией костного мозга при снижении его активности в анамнезе, которая происходит на фоне злокачественной гемолитической патологии с тяжелой прогрессирующей нейтропенией) монотерапия может быть недостаточной, поэтому показана комплексная антибактериальная терапия.
Для идентификации микроорганизма-возбудителя (возбудителей) и определения чувствительности к цефепиму следует провести соответствующие тесты. Однако Цебопим можно применять в качестве монотерапии еще до идентификации микроорганизма-возбудителя, поскольку препарат обладает широким спектром антибактериального действия относительно грамположительных и грамотрицательных микроорганизмов. У пациентов с риском смешанной аэробно-анаэробной (Bacteroides fragilis включительно) инфекции до идентификации возбудителя можно начинать лечение Цебопимом в комбинации с препаратом, действующим на анаэробы.
Цефалоспорины склонны адсорбироваться на поверхности эритроцитов и вступать в реакцию с антителами, направленными против препаратов, результатом чего является положительный тест Кумбса. У пациентов, которые применяли цефепим 2 раза в сутки, описан положительный тест Кумбса при отсутствии признаков гемолиза.
При проведении анализа мочи на глюкозу возможен ложноположительный результат. По этой причине определение глюкозы в моче следует проводить глюкозооксидазным методом в период лечения препаратом.
При применении практически всех антибиотиков широкого спектра действия сообщали о случаях возникновения псевдомембранозного колита. Поэтому важно учитывать возможность развития этой патологии в случае возникновения диареи во время лечения препаратом Цебопим. Легкие формы колита могут проходить после отмены препарата; умеренные или тяжелые формы могут требовать специального лечения.
С осторожностью применять у пациентов с заболеваниями пищеварительной системы, особенно колитом, с почечной недостаточностью (с клиренсом креатинина <50 мл/мин). Необходимо осуществлять контроль протромбинового времени.
Применение Цебопима, как и других антибиотиков, может привести к колонизации резистентной микрофлоры. При развитии суперинфекции требуется соответствующее лечение.
При применении лидокаина в качестве растворителя следует учесть информацию по безопасности лидокаина.
Дети. Препарат применяют у детей в возрасте старше 1 мес.
Период беременности и кормления грудью. Адекватных и хорошо контролируемых исследований в период беременности не проводили, поэтому Цебопим в период беременности можно назначать только тогда, когда ожидаемая польза для матери превышает потенциальный риск для плода.
Цефепим проникает в грудное молоко в очень небольшом количестве, поэтому во время лечения Цебопимом грудное вскармливание следует прекратить.
Способность влиять на скорость реакции при управлении транспортными средствами и работе с другими механизмами. Не описана.
Взаимодействия
р-р цефепима совместим со следующими парентеральными р-рами: 0,9% р-ром натрия хлорида, 5% или 10% р-рами декстрозы, р-ром натрия лактата для инъекций, р-ром Рингера с лактатом и 5% р-ром декстрозы для инъекций.
Учитывая потенциальную нефротоксичность и ототоксичность аминогликозидных антибиотиков, высокие дозы данных препаратов применяют одновременно с Цебопимом под контролем функции почек.
Сочетанное применение цефалоспоринов с диуретиками (например фуросемидом) приводит к повышению нефротоксичности первых.
Во избежание возможного лекарственного взаимодействия с другими препаратами р-ры препарата Цебопим (как и большинства других β-лактамных антибиотиков) не вводят одновременно с р-рами метронидазола, ванкомицина, гентамицина, тобрамицина сульфата и нетилмицина сульфата. В случае назначения Цебопима с указанными препаратами вводят каждый антибиотик отдельно.
Передозировка
при передозировке возможно возникновение энцефалопатии, нарушение сознания, ступора, миоклонии, комы, эпилептического припадка, повышение порога судорожной готовности.
Лечение. Необходимо прекратить введение препарата, провести симптоматическую терапию. Гемодиализ (особенно у пациентов с нарушением функции почек). Перитонеальный диализ малоэффективен. При тяжелых аллергических реакциях немедленного типа необходимо применение адреналина и других видов интенсивной терапии.
Условия хранения
в защищенном от света месте при температуре не выше 30 °С. Приготовленные р-ры препарата для в/м и в/в инъекций стабильны на протяжении 24 ч при комнатной температуре или 7 дней при хранении в холодильнике (2–8 °С).

