Зарсіо® розчин для ін'єкцій та інфузій 48 млн МО шприц 0.5 мл №1

Допоміжні речовини: кислота глутамінова, сорбіт (Е420), полісорбат 80, вода для ін’єкцій.
Філграстим - 48 млн МО
фармакодинаміка. Активною речовиною препарату є філграстим — рекомбінантний людський гранулоцитарний колонієстимулюючий фактор (Г-КСФ). Філграстим виявляє таку саму біологічну активність, як і ендогенний людський Г-КСФ, і від останнього відрізняється лише тим, що являє собою неглікозильований білок з додатковим N-кінцевим залишком метіоніну. Філграстим, який одержують за технологією рекомбінантної ДНК, виділяють із клітин бактерії Esherichia coli, до складу генетичного апарату яких введено ген, що кодує білок Г-КСФ.
Людський гранулоцитарний колонієстимулюючий фактор — глікопротеїн — регулює створення функціонально активних нейтрофільних гранулоцитів та їх вихід у кров з кісткового мозку. Філграстим значно збільшує кількість нейтрофільних гранулоцитів у периферичній крові вже протягом перших 24 год після введення та одночасно призводить до деякого збільшення кількості моноцитів. Збільшення кількості нейтрофільних гранулоцитів при застосуванні препарату в діапазоні рекомендованих доз залежить від величини дози. Їх функціональні властивості нормальні або посилені, про що свідчать результати дослідження хемотаксису і фагоцитозу. Після закінчення лікування препаратом кількість нейтрофільних гранулоцитів у периферичній крові знижується на 50% протягом 1–2 днів і до нормального рівня — протягом 1–7 днів.
Застосування філграстиму значно знижує частоту, тяжкість та тривалість нейтропенії у хворих після хіміотерапії цитостатиками або мієлоаблативної терапії з подальшою пересадкою кісткового мозку. Застосування філграстиму, як первинне, так і після хіміотерапії, активує клітини — попередники гемоцитів периферичної крові (КПГПК). Ці аутологічні КПГПК можна забирати у хворого і вводити йому після лікування цитостатиками у високих дозах або замість пересадки кісткового мозку, або як доповнення до неї. Введення КПГПК прискорює відновлення кровотворення, знижує небезпеку геморагічних ускладнень і потребу в переливанні тромбоцитарної маси. У дітей та дорослих з тяжкою спадковою, періодичною або ідіопатичною нейтропенією філграстим стабільно збільшує кількість нейтрофільних гранулоцитів у периферичній крові та знижує частоту інфекційних ускладнень.
Фармакокінетика. Як при в/в, так і при п/ш введенні препарату відмічається позитивна лінійна залежність його концентрації у плазмі крові від дози. Після п/ш введення рекомендованих доз препарату концентрація в сироватці крові перевищує 10 нг/мл протягом 8–16 год; об’єм розподілу в крові становить близько 150 мл/кг. Як після п/ш, так і після в/в введення елімінація препарату з організму відповідає кінетиці 1-го порядку. Середнє значення Т½ філграстиму із сироватки крові становить близько 3,5 год, а швидкість кліренсу — близько 0,6 мл/хв на 1 кг. Безперервне введення шляхом інфузії протягом 28 днів хворим, які одужують після аутологічної пересадки кісткового мозку, не супроводжувалося ознаками кумуляції і збільшення Т½ препарату.
зменшення тривалості і тяжкості нейтропенії у пацієнтів, які отримують інтенсивну мієлосупресивну хіміотерапію цитотоксичними препаратами з приводу злоякісних новоутворень (за винятком хронічного мієлолейкозу та мієлодиспластичного синдрому), та зменшення тривалості нейтропенії у хворих, які отримують високодозову хіміотерапію цитотоксичними препаратами з наступною аутологічною або алогенною трансплантацією кісткового мозку.
Безпека та ефективність застосування філграстиму подібні у дорослих і дітей, які одержують хіміотерапію цитотоксичними засобами.
— Препарат показаний з метою мобілізації периферичних стовбурових клітин крові (ПСКК).
— Довготривале застосування показане дітям і дорослим з тяжкою вродженою, циклічною або ідіопатичною нейтропенією та нейтропенією з абсолютною кількістю нейтрофілів <0,5·109/л з метою збільшення кількості нейтрофілів і зниження частоти інфекцій.
— Лікування стійкої нейтропенії (абсолютною кількістю нейтрофілів ≤1,0·109/л) у пацієнтів з розгорнутою стадією ВІЛ-інфекції для зниження ризику бактеріальних інфекцій, коли інші методи лікування нейтропенії недоречні.
терапію препаратом Зарсіо можна проводити в лікувальних закладах, де є необхідне діагностичне устаткування. Лікарі повинні мати досвід застосування лікарських засобів, що містять Г-КСФ та лікування хворих із гематологічними захворюваннями.
Процедури мобілізації та аферезу слід проводити при взаємодії з лікарями, які мають відповідний досвід і можливість необхідного моніторингу клітин — попередників гемопоезу.
Нейтропенія у хворих, які отримують цитотоксичну хіміотерапію з приводу злоякісних захворювань. Рекомендована добова доза препарату становить 0,5 млн ОД/кг (5 мкг/кг) маси тіла 1 раз на добу. Першу дозу препарату слід вводити не раніше ніж через 24 год після курсу цитотоксичної хіміотерапії. Препарат застосовувати, поки загальна кількість нейтрофілів у клінічному аналізі крові не перевищить очікуваний рівень і не досягне норми. Після хіміотерапії з приводу солідних пухлин, лімфом і лімфолейкозу тривалість лікування до досягнення вказаних значень становить до 14 днів. Після індукційної і консолідаційної терапії гострого мієлоїдного лейкозу тривалість лікування може бути значно збільшена (до 38 днів) залежно від виду, дози та схеми застосованої цитотоксичної хіміотерапії.
У пацієнтів, які отримують цитотоксичну хіміотерапію, минуще збільшення кількості нейтрофілів зазвичай відмічають через 1–2 доби після початку лікування препаратом Зарсіо. Але для досягнення стабільного терапевтичного ефекту необхідно продовжувати терапію, поки кількість нейтрофілів не перевищить очікуваний мінімум і не досягне норми. Не рекомендується передчасно відміняти лікування препаратом до переходу кількості нейтрофілів через очікуваний мінімум.
Спосіб введення. Препарат Зарсіо застосовувати у вигляді п/ш ін’єкцій або в/в інфузій протягом 30 хв 1 раз на добу. У більшості випадків переважає п/ш шлях введення. При в/в введенні одноразової дози тривалість ефекту препарату може зменшуватися. Клінічна значущість цих даних щодо застосування багаторазових доз препарату не встановлена. Вибір способу введення залежить від особливостей конкретної клінічної ситуації і визначається для кожного хворого окремо.
Хворі, які отримують мієлоаблативну терапію з подальшою трансплантацією кісткового мозку. Рекомендована початкова доза препарату Зарсіо — 1 млн ОД/кг (10 мкг/кг) маси тіла на добу. Першу дозу слід вводити не раніше ніж через 24 год після проведення цитотоксичної хіміотерапії, і не пізніше ніж через 24 год після трансплантації кісткового мозку.
Після максимального зниження числа нейтрофілів (надира) добову дозу препарату Зарсіо необхідно скоригувати залежно від зміни кількості нейтрофілів (див. таблицю).
Підбір дози препарату Зарсіо у відповідь на досягнення надири
| Абсолютна кількість нейтрофілів (АКН) | Корекція дози препарату Зарсіо |
| АКН >1·109/л протягом 3 діб поспіль | Зниження дози до 0,5 млн ОД/кг (5 мкг/кг) маси тіла на добу |
| АКН >1·109/л протягом наступних 3 діб поспіль | Відміна препарату |
| Якщо під час лікування АКН знижується до рівня <1·109/л, дозу препарату Зарсіо підвищувати відповідно до вищезазначеної схеми | |
Спосіб введення. Препарат розчиняти у 20 мл 5% р-ну глюкози і застосовувати у вигляді нетривалої в/в інфузії протягом 30 хв або тривалої п/ш або в/в інфузії протягом 24 год.
Мобілізація периферичних стовбурових клітин крові (ПСКК) у пацієнтів, які одержують мієлосупресивну або мієлоаблативну терапію з подальшою аутологічною трансфузією ПСКК. Хворі, які отримують мієлосупресивну або мієлоаблативну терапію з подальшою аутологічною трансплантацією ПСКК. Для мобілізації ПСКК при застосуванні препарату Зарсіо як монотерапії рекомендована доза становить 1 млн ОД/кг (10 мкг/кг) маси тіла на добу протягом 5–7 діб поспіль у вигляді тривалої п/ш інфузії протягом 24 год. Проводити 1–2 сеанси лейкаферезу на 5-ту та 6-ту добу. У деяких випадках додатково проводити 1 сеанс лейкаферезу. Не слід змінювати дозу препарату до завершального лейкаферезу.
Для мобілізації ПСКК після мієлосупресивної хіміотерапії рекомендована доза препарату Зарсіо становить 0,5 млн ОД/кг (5 мкг/кг) маси тіла на добу щодня, починаючи з першого дня після завершення курсу хіміотерапії, поки кількість нейтрофілів не перейде очікуваний мінімум і не досягне норми. Лейкаферез слід проводити протягом періоду зростання АКН з <0,5·109/л до >5·109/л. Хворим, які не отримували інтенсивної хіміотерапії, проводити 1 сеанс лейкаферезу. В окремих випадках рекомендується проводити додаткові сеанси лейкаферезу.
Мобілізація ПСКК у здорових донорів перед алогенною трансплантацією ПСКК. Для мобілізації ПСКК перед алогенною трансплантацією ПСКК для здорових донорів рекомендована доза препарату Зарсіо становить 1 млн ОД/кг (10 мкг/кг) маси тіла на добу протягом 4–5 діб поспіль. Лейкаферез проводити з 5-ї доби у разі необхідності продовжувати до 6-ї доби з метою отримання 4·106 CD34+ клітин/кг маси тіла реципієнта.
Спосіб введення. Перед інфузією препарат розчиняти у 20 мл 5% р-ну глюкози.
Довготривала терапія для збільшення кількості нейтрофілів і зниження частоти та тривалості інфекційних ускладнень у дітей та дорослих з тяжкою спадковою, періодичною або ідіопатичною нейтропенією (ТХН)
Спадкова нейтропенія. Рекомендована початкова доза — 1,2 млн ОД/кг (12 мкг/кг) маси тіла на добу шляхом одноразової п/ш ін’єкції або дрібними дозами.
Ідіопатична і періодична нейтропенія. Рекомендована початкова доза — 0,5 млн ОД/кг (5 мкг/кг) маси тіла на добу одноразово або дрібними дозами.
Підбір дози. Препарат Зарсіо вводити щоденно до досягнення і стабільного перевищення показника кількості нейтрофілів 1,5·109/л. Після досягнення терапевтичного ефекту визначати мінімальну ефективну дозу для підтримання цього рівня. Для підтримання необхідної кількості нейтрофілів потрібне тривале щоденне введення препарату. Через 1–2 тиж лікування початкову дозу можна подвоїти або наполовину знизити залежно від ефективності терапії. Надалі кожні 1–2 тиж проводити індивідуальну корекцію дози для стабілізації середньої кількості нейтрофілів у діапазоні від 1,5·109/л до 10·109/л. У хворих з тяжкими інфекціями можна застосувати схему з більш швидким підвищенням дози. Безпека застосування філграстиму при тривалому лікуванні хворих дозами Зарсіо, вищими за 2,4 млн ОД (24 мкг/кг маси тіла) на добу, не встановлена.
Зниження ризику бактеріальних інфекцій та лікування стійкої нейтропенії у пацієнтів з розгорнутою стадією ВІЛ-інфекції
Відновлення кількості нейтрофілів. Рекомендована початкова доза препарату — 0,1 млн ОД/кг (1 мкг/кг) маси тіла на добу з підвищенням дози до 0,4 млн ОД (4 мкг/кг) маси тіла на добу шляхом одноразової п/ш ін’єкції до нормалізації кількості нейтрофілів (АКН >2,0·109/л). Нормалізація кількості нейтрофілів зазвичай настає через 2 доби. У рідкісних випадках (<1% пацієнтів) для відновлення кількості нейтрофілів доза препарату може бути підвищена до 1 млн ОД/кг (10 мкг/кг маси тіла на добу).
Підтримання нормальної кількості нейтрофілів. Після досягнення терапевтичного ефекту підтримувальна доза становить 300 мкг/добу 2–3 рази на тиждень за альтернативною схемою (через добу). Надалі може бути необхідна індивідуальна корекція дози і тривале застосування препарату для підтримання середньої кількості нейтрофілів >2·109/л.
Особливі категорії хворих. Корекція дози не потрібна пацієнтам з тяжкою печінковою або нирковою недостатністю, тому що фармакокінетичні та фармакодинамічні показники виявилися подібними до таких у здорових добровольців.
Особливих рекомендацій щодо застосування препарату Зарсіо у пацієнтів літнього віку немає.
Рекомендації перед застосуванням. Перед застосуванням препарату проводити візуальний контроль вмісту попередньо заповненого шприца. Р-н повинен бути прозорим, без частинок. Короткочасний вплив низьких температур не впливає негативно на стабільність препарату. Препарат не містить консервантів. Щоб уникнути мікробної контамінації, слід враховувати, що препарат Зарсіо в попередньо заповненому шприці призначений тільки для одноразового застосування. При зберіганні та для амбулаторного використання можна дістати засіб із холодильника та зберігати при кімнатній температурі (не вище 25 °C) одноразово протягом 72 год. Після завершення цього часу не слід знову ставити в холодильник, а необхідно знищити.
Рекомендації щодо розведення препарату. Препарат Зарсіо можна вводити в розведеному вигляді в 5% р-ні глюкози. Розведення до концентрації <0,2 млн ОД/мл (2 мкг/мл) не рекомендується. При розведенні в концентрації 1,5 млн ОД/мл (15 мкг/мл) необхідно додатково ввести людський альбумін до досягнення концентрації 2 мг/мл. Наприклад, для досягнення об’єму р-ну 20 мл і загальної дози препарату Зарсіо 30 млн ОД (300 мкг/мл) необхідно додаткове введення р-ну альбуміну в об’ємі 0,2 мл (20% р-н).
При розведенні в р-ні глюкози препарат поглинається склом та іншими матеріалами, що використовуються для інфузійного введення. Заборонено використовувати р-н хлориду натрію для розведення препарату.
Переважні ділянки тіла для п/ш введення Зарсіо показані на рисунку: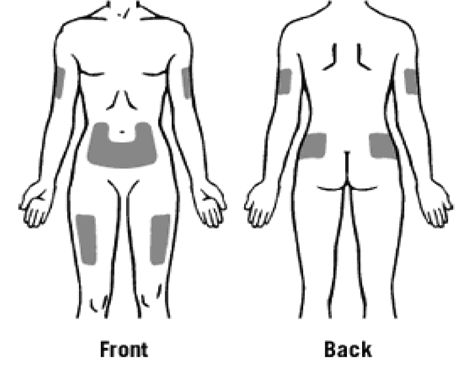
Діти. При застосуванні в дитячій практиці у пацієнтів з ТХН і онкологічними захворюваннями профіль безпеки Зарсіо не відрізнявся від таких у дорослих. Безпека та ефективність застосування препарату у новонароджених не встановлені.
Рекомендації щодо дозування для хворих дитячого віку такі самі, як для дорослих, які отримують мієлосупресивну цитотоксичну хіміотерапію.
— підвищена чутливість до філграстиму, колонієстимулюючих факторів, Escherichia coli або будь-яких допоміжних речовин.
— Тяжка спадкова нейтропенія (синдром Костмана) з цитогенетичними порушеннями та автоімунна нейтропенія.
— Термінальна стадія хронічної ниркової недостатності (ХНН).
— Хронічний мієлолейкоз та мієлодиспластичний синдром.
частота виникнення побічних реакцій класифікується таким чином: дуже часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); рідко (≥1/10 000, <1/1000); дуже рідко (<1/10 000).
Найбільш серйозні побічні реакції, які можуть виникнути під час лікування філграстимом, включають анафілактичні реакції, серйозні легеневі побічні ефекти (включаючи інтерстиціальну пневмонію та гострі респіраторні захворювання), мієлодиспластичний синдром або лейкемію у пацієнтів з тяжкою вродженою нейтропенією, реакція відторгнення трансплантату у пацієнтів, які отримують алогенну трансплантацію кісткового мозку або трансплантацію клітин — попередників периферичної крові.
Найчастішими побічними явищами на тлі терапії із застосуванням філграстиму є пірексія, біль у кістках та м’язах від низького до середнього ступеня тяжкості (спостерігається у 10% пацієнтів). Біль у кістках та м’язах, як правило, усувається при прийомі стандартних знеболювальних засобів.
При мобілізації ПСКК у здорових донорів найчастішою побічною реакцією був скелетно-м’язовий біль.
Лейкоцитоз відмічали у донорів. Також після прийому філграстиму у донорів відзначалися тромбоцитопенія та лейкаферез. Повідомлялося про збільшення та розрив селезінки. Деякі випадки розриву селезінки були летальними.
У пацієнтів із ТХН найчастішими побічними реакціями на тлі терапії із застосуванням філграстиму були біль у кістках, загальний скелетно-м’язовий біль, збільшення та розрив селезінки. Мієлодиспластичний синдром (МДС) або лейкоз відмічали у пацієнтів із вродженою нейтропенією, які застосовували філграстим.
Синдром підвищеної проникності капілярів, який становить загрозу для життя за відсутності негайного лікування, фіксувався нечасто (≥1/1000 до <1/100) у пацієнтів зі злоякісними пухлинами, які проходили курс хіміотерапії, та у здорових донорів, які проходили процедуру мобілізації периферичних стовбурових клітин крові після застосування Г-КСФ людини.
У клінічних дослідженнях у пацієнтів з ВІЛ-інфекцією побічними реакціями, які були розцінені як такі, що пов’язані із застосуванням філграстиму, були тільки скелетно-м’язовий біль, біль у кістках та міалгія.
Алергічні реакції у пацієнтів відмічали при першому або наступних введеннях філграстиму, частіше при в/в введенні препарату. У деяких випадках симптоми з’являлися знову при проведенні провокаційної проби, що свідчить про причинно-наслідковий зв’язок. У випадках серйозних алергічних реакцій у подальшому філграстим у пацієнта застосовувати не слід.
Інфекції та інвазії: часто — сепсис, бронхіт, інфекції верхніх дихальних шляхів, інфекції сечовивідних шляхів.
Порушення з боку крові і лімфатичної системи: часто — зниження рівня гемоглобіну.
Порушення з боку психіки: часто — безсоння.
Порушення з боку судинної системи: часто — АГ; рідко — аортит.
З боку кістково-м’язової системи та сполучних тканин: часто — м’язовий спазм.
Загальні порушення та реакції у місці введення: дуже часто — пірексія; часто — нездужання, периферичні набряки.
Травма, отруєння та процедурні ускладнення: часто — трансфузійна реакція.
Побічні реакції, що спостерігалися у пацієнтів з онкологічними захворюваннями
Порушення з боку крові і лімфатичної системи: нечасто — розрив селезінки, збільшення селезінки, кризи серпоподібних клітин.
З боку імунної системи: часто — алергічні реакції, у тому числі анафілактичні реакції, висип на шкірі, кропив’янка, ангіоневротичний набряк, задишка та артеріальна гіпотензія; нечасто — реакції «трансплантат проти хазяїна»
З боку обміну речовин та харчування: дуже часто — збільшення вмісту сечової кислоти в крові, підвищення рівня ЛДГ в крові, зниження апетиту; нечасто — псевдоподагра.
З боку нервової системи: дуже часто — головний біль.
З боку судинної системи: часто — артеріальна гіпотензія; нечасто — порушення судин, у тому числі захворювання, спричинені оклюзією вен, та порушення балансу рідини в організмі, синдром підвищеної проникності капілярів.
З боку шкіри та підшкірних тканин: дуже часто — висип, алопеція; нечасто — синдром Світа, шкірний васкуліт.
З боку респіраторної системи, органів грудного та медіастинального відділів: дуже часто — біль у ротоглотці, кашель, диспное; часто — кровохаркання; нечасто — гострий респіраторний дистрес-синдром, дихальна недостатність, набряк легень, інтерстиціальне захворювання легень, формування інфільтратів у легенях, легенева кровотеча.
З боку ШКТ: дуже часто — діарея, блювання, запор, нудота.
З боку кістково-м’язової системи та сполучних тканин: дуже часто — біль у м’язах та кістках; нечасто — загострення ревматоїдного артриту.
З боку нирок та сечовивідних шляхів: часто — дизурія; нечасто — патологічні зміни в аналізі сечі, гломерулонефрит.
Лабораторні показники: дуже часто — підвищення концентрації в крові ЛФ, ЛДГ, гамма-глутамілтрансферази (ГГТ), сечової кислоти (зворотне, дозозалежне, легкого або середнього ступеня тяжкості).
Загальні порушення та реакції у місці введення: дуже часто — астенія, слабкість, запалення слизових оболонок, біль; часто — біль у грудях.
Введення філграстиму не підвищувало частоти побічних явищ, зумовлених цитотоксичною хіміотерапією. До побічних явищ, що відмічалися з однаковою частотою у пацієнтів, які отримували філграстим/хіміотерапію, та пацієнтів, які отримували плацебо/хіміотерапію, належать нудота та блювання, алопеція, діарея, втомлюваність, анорексія, мукозити, головний біль, кашель, висип на шкірі, біль у грудях, загальна слабкість, біль у горлі, запор та невизначений біль.
У пацієнтів, яким проводили хіміотерапію із введенням високих доз препаратів з подальшою трансплантацією аутологічного кісткового мозку, відмічали порушення з боку судинної системи. Причинно-наслідкового зв’язку реакції із застосуванням філграстиму не встановлено. Є повідомлення про окремі випадки синдрому Світа (гострий лихоманковий непрофільний дерматоз) у пацієнтів з онкологічними захворюваннями. Однак з урахуванням того, що у більшості з цих пацієнтів відмічали лейкемію, захворювання, яке часто призводить до синдрому Світа, причинно-наслідкового зв’язку із застосуванням філграстиму не підтверджено.
Побічні реакції, що спостерігалися у пацієнтів з ТХН
З боку системи кровотворення та лімфатичної системи: дуже часто — анемія, спленомегалія в окремих випадках прогресуюча; часто — розрив селезінки, тромбоцитопенія; нечасто — порушення функцій селезінки, кризи серпоподібних клітин.
З боку нервової системи: дуже часто — головний біль.
З боку респіраторної системи: дуже часто — носові кровотечі.
З боку травного тракту: часто — діарея.
З боку гепатобіліарної системи: дуже часто — гепатомегалія.
З боку шкіри та підшкірних тканин: дуже часто — висип; часто — шкірний васкуліт (при тривалому застосуванні), алопеція.
З боку кістково-м’язової системи та сполучних тканин: дуже часто — скелетно-м’язевий біль, включаючи біль у кістках, біль у спині, артралгія, біль у м’язах, біль у кінцівках, кістково-м’язовий біль, скелетно-м’язовий біль у грудях, біль у шиї; часто — остеопороз.
З боку нирок та сечовивідних шляхів: часто — гематурія, гломерулонефрит; нечасто — протеїнурія.
Загальні порушення та порушення у місці введення: часто — біль у місці введення.
Лабораторні показники: дуже часто — підвищення концентрації в крові ЛФ, ЛДГ, сечової кислоти, глюкози (тимчасове, середньої тяжкості).
Побічні реакції, що спостерігалися у здорових донорів, яким проводили мобілізацію ПСКК
З боку імунної системи: нечасто — алергічні реакції високого ступеня тяжкості: анафілактичні реакції, ангіоневротичний набряк, кропив’янка, висип на шкірі.
З боку системи кровотворення та лімфатичної системи: дуже часто — лейкоцитоз (концентрація лейкоцитів >50·109/л), тромбоцитопенія (концентрація тромбоцитів <100·109/л; тимчасова); часто — спленомегалія (як правило, безсимптомна, відмічається також і в пацієнтів з онкологічними захворюваннями); нечасто — порушення функції селезінки, розрив селезінки, кризи серпоподібних клітин.
З боку нервової системи: дуже часто — головний біль.
З боку дихальної системи: часто — задишка; нечасто — кровохаркання, легеневі кровотечі, легеневий інфільтрат, киснева недостатність.
З боку кістково-м’язової системи та сполучних тканин: дуже часто — біль у м’язах та кістках (від низького до середнього ступеня тяжкості, тимчасовий); нечасто — загострення ревматоїдного артриту та симптомів артриту.
Лабораторні показники: часто — підвищення концентрації в крові ЛФ та ЛДГ (тимчасове, незначне); нечасто — підвищення концентрації в крові АсАТ та сечової кислоти (тимчасове, незначне).
З боку судинної системи: нечасто — синдром капілярної втрати.
З боку нирок та сечовивідних шляхів: нечасто — гломерулонефрит.
У деяких випадках відмічали побічні явища з боку легень, що призводило до дихальної недостатності або респіраторного дистрес-синдрому дорослих (РДСД), інколи летальних. Надходили повідомлення про дуже рідкісні випадки побічних явищ з боку легень (кровохаркання, легеневі кровотечі, інфільтрація легень, задишка та киснева недостатність) у здорових донорів.
Побічні реакції, що спостерігалися у пацієнтів з ВІЛ-інфекціями
З боку системи кровотворення та лімфатичної системи: часто — порушення функції селезінки, спленомегалія; нечасто — кризи серпоподібних клітин.
З боку кістково-м’язової системи та сполучних тканин: дуже часто — біль у м’язах та кістках (від низького до середнього ступеня тяжкості).
З боку нирок та сечовивідних шляхів: дуже рідко — гломерулонефрит.
У всіх випадках ступінь збільшення селезінки у пацієнтів з ВІЛ-інфекцією був від низького до середнього за результатами лікарського обстеження, клінічний перебіг порушення мав доброякісний характер; у жодного з пацієнтів не діагностовано гіперспленізм, жодному з пацієнтів не проведено спленектомії. Оскільки збільшення селезінки є частим ускладненням у пацієнтів з ВІЛ-інфекцією та відмічається з різним ступенем тяжкості в більшості пацієнтів із СНІДом, причинно-наслідковий зв’язок із застосуванням філграстиму залишається нез’ясованим.
Імуногенність. Згідно з даними 4 клінічних досліджень за участю здорових добровольців та пацієнтів з онкологічними захворюваннями у жодного з них внаслідок введення препарату Зарсіо не відмічено утворення анти-рГ-КСФ антитіл.
Опис окремих побічних реакцій. Реакції «трансплантат проти хазяїна» та летальні випадки відмічали серед пацієнтів, які застосовували Г-КСФ, після алогенної трансплантації кісткового мозку.
У постмаркетинговий період повідомлялося про випадки синдрому капілярної втрати на тлі прийому Г-КСФ людини. Вони зазвичай відзначалися у хворих з пізніми стадіями захворювання, сепсисом, у пацієнтів, які отримували багатокомпонентну хіміотерапію або проходили процедуру аферезу.
Діти з ТХН. Повідомлялося про випадки зниження мінеральної щільності кісткової тканини та остеопорозу у дітей з тяжкою хронічною нейтропенією, які отримували тривале лікування філграстимом. Частота виникнення цього небажаного явища в рамках клінічних досліджень оцінювалася як поширена.
препарат Зарсіо містить сорбіт, тому пацієнтам з рідкісною спадковою непереносимістю фруктози не слід застосовувати даний препарат.
Препарат Зарсіо не слід застосовувати у пацієнтів з тяжкою вродженою нейтропенією, у яких розвинутий лейкоз, та хворим, які мають ознаки лейкемічної трансформації.
Реакції гіперчутливості, включаючи анафілактичні реакції, що відмічалися на початку або під час лікування, зафіксовані у пацієнтів, які приймали філграстим. Слід припинити прийом препарату Зарсіо у пацієнтів з клінічно значущими реакціями гіперчутливості.
Не слід застосовувати препарат Зарсіо у пацієнтів з підвищеною чутливістю до філграстиму або пегфілграстиму в анамнезі.
Як і при застосуванні всіх терапевтичних білків, існує імовірність розвитку імуногенності. Швидкість виникнення антитіл до філграстиму зазвичай низька. Зв’язуючі антитіла були виявлені, як і при застосуванні всіх біопрепаратів; однак наразі вони не асоціюються із нейтралізуючою дією.
Були повідомлення про аортит після введення філграстиму як у здорових, так і в онкологічно хворих. Відзначалися наступні симптоми: лихоманка, біль у животі, нездужання, біль у спині та підвищені запальні маркери (наприклад підвищений рівень С-реактивного білка та лейкоцитоз). У більшості випадків аортит діагностували шляхом КТ-сканування та як правило, він зникав після відміни філграстиму.
Нейтропенія у хворих, які отримують цитотоксичну хіміотерапію з приводу злоякісних захворювань. Оскільки відомо, що Г-КСФ сприяють росту мієлоїдних клітин in vitro, аналогічні ефекти можуть відмічати in vivo.
Безпека та ефективність застосування препарату Зарсіо у хворих з мієлодиспластичним синдромом і хронічним мієлолейкозом не встановлені, тому при цих захворюваннях застосування препарату не показано. Особливої уваги потребує проведення диференційного діагнозу між бласт-трансформацією хронічного мієлолейкозу і гострим мієлолейкозом.
Оскільки дані щодо безпеки та ефективності препарату Зарсіо для хворих із вторинним гострим мієлоцитарним лейкозом обмежені, препарат слід призначати з обережністю.
Безпека та ефективність введення філграстиму в de novo хворих із гострим мієлоцитарним лейкозом віком <55 років зі сприятливим цитогенетичним прогнозом [t(8;21), t(15;17), та inv(16)] не встановлені.
Особливі застереження щодо хворих на злоякісні новоутворення. Після прийому філграстиму рідко відмічали випадки спленомегалії та розриву селезінки. Деякі випадки розриву селезінки були летальними. Пацієнтів, які приймають філграстим і скаржаться на біль у верхній лівій частині живота та/або в лівому плечі, слід перевірити на наявність збільшення розмірів селезінки або розриву селезінки.
Лейкоцитоз. Кількість лейкоцитів у крові досягає або перевищує 100·109/л менше ніж у 5% хворих, які отримують добову дозу препарату >0,3 млн ОД/кг (3 мкг/кг) маси тіла. Немає відомостей щодо будь-яких побічних дій, безпосередньо зумовлених розвитком лейкоцитозу такого ступеня тяжкості. Однак враховуючи можливий ризик, пов’язаний з тяжким лейкоцитозом, під час лікування препаратом Зарсіо необхідно регулярно контролювати кількість лейкоцитів. Якщо кількість лейкоцитів перевищить 50·109/л після досягнення очікуваного рівня, слід негайно відмінити препарат. У випадку застосування препарату для мобілізації ПСКК його необхідно відмінити або зробити корекцію дози при збільшенні кількості лейкоцитів до >70·109/л.
Ризик, пов’язаний з підвищенням дози хіміотерапії. Слід дотримуватися особливої обережності при лікуванні хворих зі злоякісними новоутвореннями, які отримують високі дози цитостатиків, оскільки в цих випадках результативність лікування не встановлена. Відомо, що підвищені дози хіміопрепаратів зумовлювали більш виражену токсичність, призводячи до розвитку серцево-судинних, легеневих, неврологічних і дерматологічних побічних реакцій.
Монотерапія препаратом Зарсіо не запобігає розвитку тромбоцитопенії та анемії, зумовлених мієлосупресивною хіміотерапією. У випадку застосування більш високих доз хіміопрепаратів (наприклад повні дози відповідно до призначених схем) ризик тяжкої тромбоцитопенії та анемії підвищується.
Рекомендується регулярно контролювати такі показники клінічного аналізу крові, як гематокрит і кількість тромбоцитів. Слід дотримуватися особливої обережності при застосуванні однокомпонентних або комбінованих хіміотерапевтичних препаратів, які можуть спричинити тяжку тромбоцитопенію.
При застосуванні препарату Зарсіо для мобілізації ПСКК виявлено зниження ступеня тяжкості і тривалості тромбоцитопенії, зумовленої мієлосупресивною або мієлоаблативною хіміотерапією.
Інші заходи безпеки. Ефективність препарату для хворих зі значно зниженою кількістю мієлоїдних клітин-попередників не вивчалася. Зарсіо підвищує кількість нейтрофілів шляхом впливу перш за все на клітини — попередники нейтрофілів. Тому у хворих зі зниженою кількістю клітин-попередників (наприклад у результаті інтенсивної променевої терапії, хіміотерапії або внаслідок інфільтрації кісткового мозку пухлинними клітинами) кількість утворюваних нейтрофілів може бути знижена.
Іноді у пацієнтів, які одержували високодозову хіміотерапію з наступною трансплантацією аутологічного кісткового мозку, відзначали судинні порушення, наприклад оклюзію вен і порушення водного обміну.
Існують дані щодо розвитку реакції «трансплантат проти хазяїна» і летальних випадків у хворих, які отримують Г-КСФ після алогенної трансплантації кісткового мозку.
Посилення гемопоезу в кістковому мозку у відповідь на терапію ростовими факторами асоціюється з появою минущих патологічних змін, що виявляються при остеосцинтиграфії. Це слід враховувати при тлумаченні діагностичних зображень кісток.
Мобілізація периферичних стовбурових клітин крові (ПСКК). Немає жодного рандомізованого порівняння двох рекомендованих методів мобілізації (філграстим окремо або в поєднанні з мієлосупресивною хіміотерапією) в межах однієї популяції пацієнтів. Ступінь варіації між окремими пацієнтами та між лабораторними аналізами CD34+ клітин означає, що безпосереднє порівняння різних досліджень ускладнене. Тому важко рекомендувати оптимальний метод. Вибір методу мобілізації слід розглядати у зв’язку із загальними цілями лікування для окремого пацієнта.
Попереднє лікування цитотоксичними засобами. У хворих, яким раніше проводили інтенсивну мієлосупресивну терапію, на тлі застосування препарату Зарсіо для мобілізації ПСКК може не відмічатися збільшення кількості ПСКК до рекомендованого мінімального рівня (≥2,0·106 CD34+ клітин/кг) або підвищення швидкості відновлення тромбоцитів.
Деякі цитотоксичні засоби виявляють особливу токсичність відносно клітин — попередників гемопоезу та негативно впливають на їх мобілізацію. Тривале застосування препаратів мелфалан, карбоплатин або кармустин (BCNU) перед мобілізацією клітин-попередників може призвести до погіршення результатів. Однак одночасне застосування мелфалану, карбоплатину або BCNU з філграстимом ефективне при мобілізації ПСКК. Якщо планується трансплантація ПСКК, рекомендується провести мобілізацію стовбурових клітин на ранній стадії лікування хворого. Особливу увагу слід звернути на кількість клітин-попередників, активованих у таких хворих, до застосування препаратів хіміотерапії у високих дозах. Якщо результати мобілізації відповідно до вищенаведених критеріїв недостатні, слід розглянути застосування альтернативних методів лікування, які не потребують використання клітин-попередників.
Оцінка кількості мобілізованих периферичних стовбурових клітин крові. При проведенні оцінки кількості ПСКК, мобілізованих у хворих, які отримали терапію із застосуванням філграстиму, особливу увагу слід приділяти методу кількісного визначення. Результати проточного цитометричного аналізу кількості CD34+-клітин значно відрізняються залежно від застосованої методології визначення, отже, слід з обережністю ставитися до результатів визначення їх кількості, отриманих в інших лабораторіях.
Результати статистичного аналізу взаємозв’язку кількості введених CD34+-клітин та швидкості нормалізації кількості тромбоцитів після проведення хіміотерапії із застосуванням високих доз хіміопрепаратів свідчать про складну, але постійну залежність. Рекомендації стосовно необхідності забезпечення мінімального вмісту на рівні ≥2,0·106 CD34+ клітин/кг ґрунтуються на опублікованих даних про досвід адекватного відновлення гематологічних показників. При рівні, що перевищує мінімальний рекомендований, відмічається швидша нормалізація, при рівні, нижчому за рекомендований, — триваліша.
Особливі заходи безпеки для здорових донорів, які проходять мобілізацію ПСКК. Мобілізація ПСКК здорових донорів впливає на стан їхнього здоров’я і застосовується винятково для отримання алогенних стовбурових клітин для трансплантації.
Донори, яким проводять мобілізацію ПСКК для трансплантації, повинні відповідати стандартним вимогам за клінічними показниками та результатами лабораторних аналізів, що висуваються до донорів стовбурових клітин. Особливу увагу слід звертати на показники аналізів крові та наявність інфекційних захворювань. Безпека та ефективність введення філграстиму здоровим донорам віком молодше 16 та старше 60 років не оцінювали.
Дуже часто відмічалася тромбоцитопенія у пацієнтів, які приймали препарат Зарсіо. Тому слід ретельно контролювати кількість тромбоцитів.
Транзиторна тромбоцитопенія (кількість тромбоцитів <100·109/л) після введення філграстиму та лейкаферезу спостерігалася у 35% пацієнтів. Серед них про два випадки зниження кількості тромбоцитів <50·109/л було повідомлено та віднесено до процедури лейкаферезу.
При необхідності проведення більш ніж однієї процедури лейкаферезу особливу увагу слід приділяти донорам, вміст тромбоцитів у яких до початку лейкаферезу становить <100·109/л; як правило, проведення лейкаферезу не рекомендовано при вмісті тромбоцитів <75·109/л.
Лейкаферез не слід проводити донорам, які потребують антикоагулянтної терапії або з порушеннями гемостазу.
Подальше введення філграстиму слід відмінити або знизити його дозу у випадках зростання лейкоцитів до рівня, що перевищує 70·109/л.
Моніторинг стану донорів, які отримують Г-КСФ для мобілізації ПСКК, слід продовжувати до нормалізації гематологічних показників.
У здорових донорів після введення Г-КСФ відмічали тимчасові цитогенні зміни. Значення цих змін не визначене.
Визначення довготривалої безпеки препарату при введенні донорам триває. Ризик утворення злоякісних клонів мієлоїдних клітин не виключений. Центрам аферезу рекомендовано проводити систематичні обстеження донорів стовбурових клітин у період щонайменше 10 років для забезпечення моніторингу показників довготривалої безпеки.
Частими є випадки безсимптомної спленомегалії. Випадки розриву селезінки у здорових донорів та пацієнтів внаслідок введення Г-КСФ відмічали дуже рідко. Зафіксовано кілька випадків летального розриву селезінки. Отже, необхідним є ретельний моніторинг розміру селезінки (клінічне та ультразвукове обстеження). Слід виключити діагноз розриву селезінки у донорів та/або пацієнтів, які скаржаться на біль у лівій верхній частині живота або в лівому плечі.
У період постмаркетингових досліджень надходили повідомлення про дуже рідкісні випадки побічних явищ з боку легень (кровохаркання, легеневі кровотечі, інфільтрація легень, задишка та киснева недостатність). У випадку підозри або підтвердження побічного явища з боку легень подальше застосування філграстиму слід припинити та надати пацієнту відповідну медичну допомогу.
У здорових донорів зазвичай відмічали диспное та інші побічні реакції з боку дихальної системи (кровохаркання, легенева кровотеча, інфільтрати в легенях та гіпоксія), які реєструвалися доволі рідко. У разі передбачуваних або підтверджених побічних ефектів потрібно припинити лікування філграстимом та надати необхідну медичну допомогу.
Трансплантація алогенних ПСКК, мобілізованих введенням філграстиму. Дані свідчать про те, що імунологічній взаємодії алогенних ПСКК і реципієнта властивий більший ступінь ризику розвитку гострої та хронічної реакції «трансплантат проти хазяїна» порівняно з трансплантацією кісткового мозку.
Особливі заходи безпеки для пацієнтів з ТХН
Дослідження складу крові. Необхідним є ретельний моніторинг кількості тромбоцитів, особливо протягом перших тижнів терапії із застосуванням філграстиму. У випадках розвитку тромбоцитопенії у пацієнтів, тобто стійкого зниження вмісту тромбоцитів до рівня <100 000/мм3, подальшу терапію із застосуванням філграстиму слід тимчасово відмінити або знизити його дозу.
Можливі й інші зміни формули крові, у тому числі анемія та тимчасове підвищення вмісту мієлоїдних клітин-попередників; необхідний ретельний моніторинг формули крові.
Трансформація у лейкоз або передлейкоз. Особлива обережність необхідна при діагностиці тяжкої хронічної нейтропенії, щоб диференціювати її від інших гематологічних захворювань, таких як апластична анемія, мієлодисплазія та мієлолейкоз. До початку лікування слід провести розгорнутий аналіз крові з визначенням лейкоцитарної формули і кількості тромбоцитів, а також визначити морфологічну картину кісткового мозку і каріотип.
Виникнення мієлодиспластичного синдрому (МДС) або лейкемії у пацієнтів з тяжкою хронічною нейтропенією, які брали участь у клінічних дослідженнях результатів застосування філграстиму, відмічається рідко (приблизно у 3% випадків). Вказані порушення виявлені лише у пацієнтів з вродженою нейтропенією. МДС та лейкемія є частими ускладненнями захворювання, їх зв’язок із терапією із застосуванням філграстиму є непевним. Приблизно у 12% пацієнтів (без цитогенетичних порушень до початку терапії) за результатами наступних аналізів відмічали відхилення, у тому числі моносемію 7. У випадках виникнення у пацієнта з тяжкою хронічною нейтропенією цитогенетичних порушень слід уважно зважити співвідношення користі та ризику подальшого застосування філграстиму. Подальше введення філграстиму пацієнтам у разі розвитку МДС або лейкемії слід відмінити. Невідомо, чи підвищує довготривала терапія із застосуванням філграстиму у пацієнтів з тяжкою хронічною нейтропенією ризик цитогенетичних порушень, МДС або трансформації захворювання на лейкемію. Морфологічне та цитогенетичне обстеження кісткового мозку пацієнтів слід проводити регулярно, з інтервалом приблизно кожні 12 міс.
Інші особливі запобіжні заходи. Слід виключити інші причини виникнення нейтропенії, наприклад вірусні інфекції.
Збільшення селезінки є безпосереднім наслідком введення філграстиму. У 31% пацієнтів, які брали участь у дослідженні, відмічалася спленомегалія, визначена за результатами пальпації. Збільшення об’єму, визначене за результатами радіографічного обстеження, відбувається на початку терапії із застосуванням філграстиму, без подальшого зростання. Зниження дози гальмує або зупиняє прогресування збільшення селезінки, 3% пацієнтів була потрібна спленектомія. Обстеження для визначення розмірів селезінки слід проводити регулярно. Пальпація живота є достатнім методом для визначення аномального збільшення об’єму селезінки.
Гематурія/протеїнурія відмічалася в невеликої кількості пацієнтів. Для своєчасного визначення цих явищ необхідне регулярне проведення аналізу сечі.
Показники безпеки та ефективності при застосуванні у новонароджених та пацієнтів з автоімунною нейтропенією не визначено.
ВІЛ-інфекція. Відмічалися часті випадки спленомегалії після застосування філграстиму. Тому пацієнтів, які застосовували філграстим та почали скаржитися на біль у лівій верхній частині живота та/або в плечі, потрібно обстежити з приводу збільшення або розриву селезінки.
Формула крові. Необхідний ретельний моніторинг значення абсолютної кількості нейтрофілів (АНК), особливо в період перших тижнів терапії із застосуванням філграстиму. У деяких пацієнтів виникає дуже швидка реакція зі значним підвищенням кількості нейтрофілів у відповідь на першу дозу філграстиму. Рекомендується щоденне визначення АНК протягом перших 2–3 днів введення філграстиму. У подальшому, протягом перших 2 тиж, визначення АНК рекомендовано проводити щонайменше 2 рази на тиждень, надалі — 1 раз на тиждень та через кожні 2 тиж в період проведення підтримувальної терапії. У період чергового введення філграстиму індивідуально визначеною дозою та дозою 30 млн ОД/добу (300 мкг/добу) можливі більші коливання значення АНК пацієнта. Для визначення мінімальних (найнижчих значень АНК) рекомендується отримувати зразки крові пацієнта для аналізу вмісту АНК безпосередньо перед плановим введенням філграстиму.
Ризик, зумовлений застосуванням лікарських препаратів мієлосупресивної дії підвищеними дозами. Введення філграстиму окремо не виключає можливості виникнення тромбоцитопенії та анемії, зумовлених мієлосупресивною хіміотерапією. Внаслідок отримання хіміопрепаратів у вищих дозах або застосування більшої кількості таких препаратів у комбінації з філграстимом ризик розвитку тромбоцитопенії та анемії у пацієнта може зростати. Рекомендується регулярно контролювати показники формули крові.
Інфекційні та злоякісні захворювання, що спричиняють мієлосупресію. Розвиток нейтропенії може бути наслідком інфільтрації в кістковий мозок збудників опортуністичних інфекцій, таких як представники бактерій Mycobacterium avium, або ураження його злоякісними новоутвореннями, наприклад лімфомою. У разі наявності у пацієнта інфекційних захворювань або злоякісних новоутворень, що уражують кістковий мозок, для усунення нейтропенії, крім введення філграстиму, необхідно провести відповідну терапію для лікування захворювання. Вплив філграстиму на усунення нейтропенії, спричиненої інфекційними захворюваннями або злоякісними новоутвореннями, що уражують кістковий мозок, не визначався.
Інші застережні заходи. Необхідно виключити такі причини транзиторної нейтропенії, як вірусні інфекції. Збільшення селезінки є вірогідним ефектом, пов’язаним з лікуванням препаратом Зарсіо. Під час клінічних досліджень у 31% хворих при пальпації виявляли спленомегалію. При рентгенографії збільшення розмірів селезінки виявляється одразу після початку лікування філграстимом і має тенденцію до стабілізації. Відзначено, що зниження дози препарату Зарсіо уповільнює або зупиняє збільшення розміру селезінки; у 3% хворих може виникнути необхідність у спленектомії. Необхідно регулярно контролювати розміри селезінки при клінічному огляді.
У невеликої кількості хворих відмічалися гематурія/протеїнурія. Для виключення цих проявів слід регулярно проводити контроль загального аналізу сечі.
Безпека та ефективність застосування препарату у новонароджених і хворих з автоімунною нейтропенією не встановлені.
Зниження ризику бактеріальних інфекцій та лікування стійкої нейтропенії у пацієнтів з розгорнутою стадією ВІЛ-інфекції
Кількість клітин крові. Необхідно ретельно контролювати абсолютну кількість нейтрофілів (АКН), особливо протягом перших тижнів терапії препаратом Зарсіо. У деяких хворих може відзначатися дуже швидке і значне збільшення АКН при початковій дозі Зарсіо. Протягом перших 2–3 діб застосування препарату рекомендується щодня визначати АКН. У подальшому АКН слід перевіряти мінімум 2 рази на тиждень протягом перших 2 тиж і потім кожного тижня або через тиждень протягом усього курсу підтримувальної терапії. У разі перерви в застосуванні препарату Зарсіо в дозі 30 млн ОД/добу (300 мкг/добу) у хворих під час лікування може відмічатися значне коливання АКН. З метою визначення мінімального рівня АКН (надира) рекомендується проводити контроль загального аналізу крові перед кожним введенням препарату Зарсіо.
Ризик, зумовлений застосуванням високих доз мієлосупресивних лікарських засобів. Монотерапію препаратом Зарсіо не застосовувати для запобігання розвитку тромбоцитопенії і анемії на тлі прийому мієлосупресивних препаратів. У випадку застосування більш високих доз або одночасно декількох мієлосупресивних лікарських засобів у поєднанні з терапією Зарсіо ризик розвитку тромбоцитопенії та анемії підвищується. Рекомендується регулярний контроль загального аналізу крові.
Розвиток мієлосупресії внаслідок інфекцій або пухлинних новоутворень. Нейтропенія може бути зумовлена ураженням кісткового мозку при опортуністичних інфекціях, спричинених збудниками Mycobacterium avium complex або злоякісними новоутвореннями, наприклад лімфомою. При виявленні інфільтративного ураження кісткового мозку запального походження або злоякісного новоутворення одночасно із застосуванням препарату Зарсіо для лікування нейтропенії необхідно призначити відповідну терапію діагностованих захворювань. Ефективність застосування Зарсіо при лікуванні нейтропенії, зумовленої ураженням кісткового мозку інфекційного генезу або пухлинними новоутвореннями, не встановлена.
Інші застережні заходи. Є дані щодо рідкісних випадків небажаного впливу на органи дихання, зокрема щодо розвитку інтерстиціальної пневмонії на тлі застосування Г-КСФ. Хворі, які нещодавно перенесли інфільтративне захворювання легень або пневмонію, можуть мати високий ризик. Поява таких симптомів, як кашель, підвищення температури тіла і задишка в поєднанні з виявленим інфільтративним ураженням легень при рентгенологічному дослідженні та ознаки прогресуючої дихальної недостатності дають змогу припустити наявність респіраторного дистрес-синдрому дорослих (РДСД). У разі виявлення РДСД застосування препарату Зарсіо слід припинити і призначити відповідне лікування.
У хворих із супутньою кістковою патологією та остеопорозом при тривалому (більше 6 міс) застосуванні препарату Зарсіо рекомендується регулярно контролювати щільність кісткової тканини.
Пацієнти, які є носіями серпоподібних клітин, та пацієнти з серпоподібно-клітинною анемією. У хворих із серпоподібно-клітинною анемією відзначаються випадки розвитку гострого гемолітичного кризу (збільшення кількості змінених клітин), іноді з летальним наслідком. Таким хворим необхідно з обережністю призначати препарат Зарсіо і в ході терапії пильно контролювати відповідні клінічні і лабораторні показники, звертаючи особливу увагу на можливе збільшення селезінки та розвиток тромбозу кровоносних судин.
При рентгенографії кісткової тканини в динаміці виявлено підвищення гемопоетичної активності кісткового мозку у відповідь на терапію фактором росту. Ці дані слід враховувати при аналізі результатів рентгенографії кісток.
Повідомлялося про випадки синдрому підвищеної проникності капілярів після застосування Г-КСФ, який характеризується гіпотензією, гіпоальбумінемією, набряками та гемоконцентрацією. Пацієнти, у яких з’явилися ознаки синдрому підвищеної проникності капілярів, потребують ретельного нагляду, симптоматичної терапії, включаючи реанімаційні заходи.
Гломерулонефрит зареєстровано у пацієнтів, які отримують філграстим. Як правило, гломерулонефрит минає після зниження дози або відміни філграстиму. Рекомендується періодично проводити аналіз сечі.
З метою поліпшення простежуваності Г-КСФ, назва лікарського засобу, що вводиться, повинна бути чітко зазначена у файлі пацієнта.
Пацієнти з підвищеною чутливістю до латексу. Захисний ковпачок містить похідне натурального каучукового латексу. Хоча у самому лікарському засобі не міститься натурального каучукового латексу, безпека застосування продукту у пацієнтів, чутливих до латексу, не проводилося.
Застосування у період вагітності або годування грудьми. Безпека філграстиму у вагітних не встановлена. Існують дані про проникнення філграстиму крізь плацентарний бар’єр. Даних про тератогенність філграстиму в ході досліджень на тваринах не отримано. За результатами досліджень на тваринах виявлена репродуктивна токсичність. У тварин, які одержували філграстим, виявлена підвищена частота викиднів.
Препарат Зарсіо не рекомендується застосовувати в період вагітності.
Невідомо, чи проникає філграстим та його метаболіти у грудне молоко людини, отже, ризик для немовлят не можна виключити. Тому необхідно прийняти рішення стосовно припинення грудного вигодовування або застосування філграстиму з врахуванням користі грудного вигодовування для дитини і користі терапії для жінки.
У дослідженнях на тваринах встановлено, що філграстим не впливає на їх репродуктивну систему або фертильність.
Здатність впливати на швидкість реакції при керуванні транспортними засобами або іншими механізмами. Філграстим може чинити незначний вплив на реакції при керуванні транспортними засобами або іншими механізмами, а саме — можливе запаморочення.
безпека та ефективність введення препарату Зарсіо в той же день, що і мієлосупресивних цитотоксичних хіміопрепаратів, не встановлені. Через чутливість мієлоїдних клітин, що швидко діляться, до мієлосупресивної цитотоксичної хіміотерапії призначати препарат Зарсіо в інтервалі 24 год до або після введення цих препаратів не рекомендується.
При одночасному призначенні препарату Зарсіо і 5-флуороурацилу тяжкість нейтропенії може посилитися. Взаємодія з іншими гемопоетичними факторами росту і цитокінами невідома.
Оскільки літій стимулює вивільнення нейтрофілів, можливе посилення дії препарату Зарсіо при комбінованому введенні, але таких досліджень не проводили.
З огляду на фармацевтичну несумісність, не можна змішувати препарат з 0,9% р-ном натрію хлориду.
симптоми передозування Зарсіо невідомі. Через 1–2 дні після припинення лікування препаратом кількість циркулюючих нейтрофільних гранулоцитів зазвичай знижується на 50%, а через 1–7 днів повертається до норми.
2–8 °С в оригінальній упаковці. Не заморожувати.
Зберігати у недоступному для дітей місці.
Після розведення р-н стабільний протягом 24 год при температурі 2–8 °С. З мікробіологічної точки зору, р-н слід використати негайно.