Актуальность проблемы стратификации риска пациентов с сердечно-сосудистыми заболеваниями, и, в первую очередь, с ИБС, обусловлена тем, что сегодня эта нозологическая группа продолжает оставаться ведущей причиной смерти в большинстве развитых стран. Важным для прогноза фактором является электрическая нестабильность миокарда, что отражает уязвимость миокарда для развития угрожающих жизни аритмий. Составляющие электрической нестабильности таковы: аритмогенный субстрат (стойкий, нестойкий), который провоцируют факторы, триггеры (желудочковая экстрасистолия, ишемия миокарда). Негомогенная волна деполяризации миокарда, возникающая вследствие нарушения проведения импульса в зонах с выраженной ишемией миокарда, приводит к возможной многократной циркуляции волны и развитию опасных для жизни нарушений ритма сердца. В последнее время большое внимание уделяется разработке таких неинвазивных и простых маркеров аритмогенеза, как продолжительность интервала Q–T, величина его дисперсии (dQ–T) и их производные.
Интервал Q–T отражает продолжительность ПД клеток миокарда (электрическая систола желудочков), включая как деполяризацию, так и реполяризацию, а его удлинение — замедленную и асинхронную реполяризацию миокарда желудочков. ЭКГ записывается в состоянии покоя на скорости 50 мм/с, интервал Q–T измеряется не меньше чем в 3 последовательных циклах с расчетом средних значений. Не анализируют ЭКГ с нечеткой дифференциацией зубца Т, с блокадой ножек пучка Гиса, частичным и полным нарушением внутрижелудочковой проводимости, фибрилляцией предсердий. Не оценивают величины интервала Q–T в комплексах экстрасистол, комплексах перед экстрасистолами и следующих за экстрасистолами. Оптимальным для измерения на стандартной ЭКГ покоя считают II стандартное отведение, а в случае выраженной волны U или сглаженности зубца Т — I стандартное или грудное отведение V5. В общем виде данный интервал определяют как расстояние между началом зубца Q (или точкой отклонения кардиограммы от изолинии после окончания зубца P) и окончанием зубца Т и измеряют в миллисекундах. При измерении «вручную», наиболее часто окончание зубца Т определяют как место пересечения изоэлектрической линии ТР и касательной, проведенной по максимальному наклону нисходящего колена зубца Т (классический метод E. Lepeshkin и B. Surawicz). Продолжительность интервала Q–T изменяется в зависимости от ЧСС, пола, возраста, состояния нейрогормональной регуляции, психоэмоционального и физического напряжения.
Электрофизиологической основой, предопределяющей продолжительность конечной части ПД, является состояние ионных каналов мембраны кардиомиоцита (преимущественно медленные калиевые каналы IK, менее значимые — IK1 и ICa).
У всех клеток по обе стороны их мембран существуют электрические потенциалы. Существование мембранных потенциалов обусловлено тем, что концентрация ионов в цитоплазме значительно отличается от таковой в интерстициальной жидкости и ионы, двигающиеся против градиента концентрации путем диффузии на полупроницаемых мембранах, способствуют возникновению разности потенциалов. Необходимо учитывать три наиболее важные иона: натрий (Na+), кальций (Са2+), концентрация которых в интерстициальной жидкости выше, чем внутри клеток, и калий (К+), распределение которого противоположно. Диффузия ионов через мембрану клетки происходит через каналы, специфические для определенных ионов. На рис. 2.1 показано, как в ответ на электрический синусовый или другой импульс генерируется ПД, создаваемый направленным по градиенту концентрации ионным током через ионные каналы.
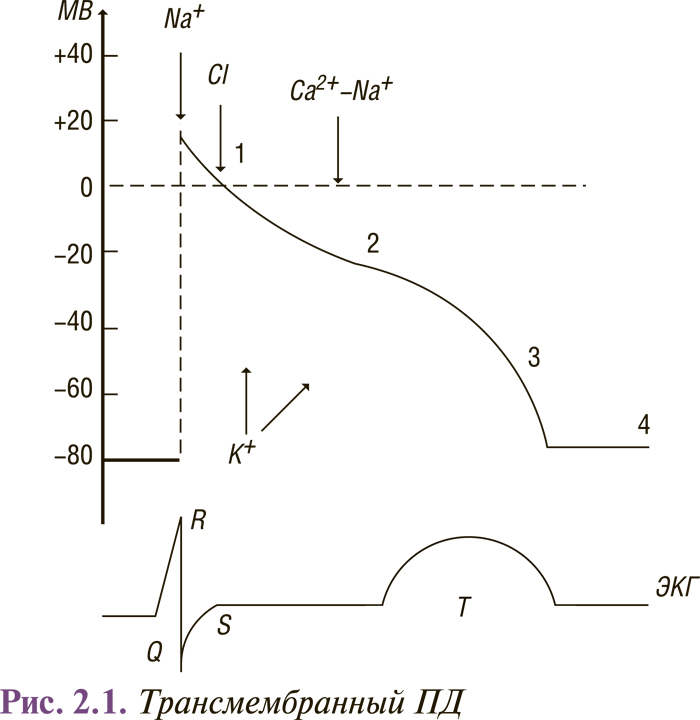
Фазы ПД:
0 — фаза быстрой деполяризации (10 мс): начальная фаза возбуждения, активация быстрых Na-каналов (ионы Na+ направляются внутрь клетки).
1 — фаза ранней быстрой реполяризации: восстановление начальной полярности мембраны кардиомиоцита (перенесение ионов хлора Cl внутрь клетки).
2 — фаза плато: медленной реполяризации (200 мс): внутрь клетки поступают ионы Са2+ и Na+.
3 — конечная часть быстрой реполяризации кардиомиоцитов: ионы К+ из клетки поступают во внеклеточную жидкость).
4 — потенциал покоя — диастола на ЭКГ. В последней фазе концентрация ионов К+ в 30 раз больше внутри клетки, чем во внеклеточной жидкости, а во внеклеточной жидкости концентрация ионов Na+ больше в 20 раз, Са2+ — в 25 раз, благодаря чему происходит поддержка активной функции ионных каналов.
При нарушении работы ионных каналов (причинами могут быть, в частности, гипертрофия или ишемия мышечного волокна, нарушение электролитного состава как внутри, так и вне клетки, направленное действие внешних химических агентов), длительность электрической систолы может увеличиваться, причем в ряде случаев продолжительность ПД может в разных кардиомиоцитах увеличиваться по-разному, что создает условия для возникновения аритмий по типу «повторного входа». Однако на том уровне исследований, который доступен в клинической практике, мы сталкиваемся не с показателями электрофизиологического состояния отдельных кардиомиоцитов, а с комбинированным ПД от целого участка сердечной мышцы (а в случае с дискордантными отведениями — с проекцией глобального вектора электрической оси сердца, которая практически исключает топографическую избирательность в отражении электрической активности сердца). Итак, показатели негомогенной реполяризации лишь частично отражают электрофизиологический статус кардиомиоцитов, большое влияние на них оказывает состояние магистральных отделов проводящей системы сердца и автономной нервной системы сердца, удельный вес фиброзной соединительной ткани в структуре участка миокарда (что особенно актуально при наличии рубцовых изменений в миокарде) и масса участка фиброза сердечной мышцы. Результаты проведенных исследований демонстрируют связь поверхностно определенной негомогенной реполяризации с разной миокардиальной патологией. Исходя из изложенного, можно считать, что в разных ситуациях этот показатель может быть или причиной, или сопутствующим маркером, или следствием патологического состояния миокарда.
Корригированный интервал Q–T (Q–Tc) — производный показатель от интервала Q–T. Корректное измерение этого интервала является обязательным компонентом исследования, необходимым для установления диагноза, определения тактики лечения, оценки эффективности проводимой терапии.
Попытки найти точное математическое соотношение ЧСС и Q–T ведут свою историю с 1920 г., когда почти одновременно и независимо друг от друга L. Fridericia и H. Bazett предложили использовать практически одинаковый способ вычисления должного значения интервала Q–T. Исторически «выжили» две формулы H. Bazett, полученные на основании результатов ЭКГ обследования 39 молодых здоровых мужчин. Одну используют для расчета должного интервала Q–Tд и рассчитывают по формуле: Q–Tд=k√R–R, где k — эмпирически найденный коэффициент, составляет 0,37 для мужчин и 0,40 — для женщин. Удлинением считается превышение должного значения интервала Q–Tд более чем на 0,02 с. Другую формулу H. Bazett используют для определения корригированного интервала Q–Tc, рассчитанного по формуле:
Q–Tc=Q–T/√R–R,
где Q–T и R–R — интервалы, измеренные на ЭКГ, Q–Tc — корригированный интервал Q–T. Смысл этого преобразования заключается в следующем: продолжительность интервала Q–T математически приравнивается к таковой при частоте 60 сокращений в минуту. При данном методе расчета Q–Tc в норме у взрослых не должен превышать 440 мс.
В мировой кардиологии до определенного времени также использовали разные методы оценки интервала Q–T, тем не менее в конце 50-х годов ХХ в. основным клиническим стандартом стала оценка корригированного интервала Q–Tc, рассчитанного по формуле: Q–Tc=Q–T/√R–R, которая получила статус «закона Базетта» (в 1947 г. L. Taran и N. Szilagy доказали клиническую информативность использования оценки Q–Tc у больных с ревматическим поражением миокарда). В дальнейшем, в 1985 г. P. Schwartz с использованием вышеприведенной формулы (Q–Tc=Q–T/√R–R), предложил большие и малые клинико-ЭКГ-критерии для установления диагноза синдрома удлиненного интервала Q–T (табл. 2.2).
Таблица 2.2
Диагностические критерии синдрома удлиненного интервала Q–T согласно бальной системе (Schwartz P., 1985)
| Критерий | Балл |
| Электрокардиографический | |
| Q–Tc >480 мс | 3 |
| Q–Tc >460–470 мс | 2 |
| Q–Tc >450 мс | 1 |
| Тахикардия типа «пируэт» | 1 |
| Альтернация зубца Т | 1 |
| Двугорбый зубец Т как минимум в 3 отведениях | 1 |
| Брадикардия (соответственно возрасту) | 0,5 |
| Клинический | |
| Синкопальные состояния, провоцируемые стрессом | 2 |
| Синкопальные состояния без стресса | 1 |
| Врожденная глухота | 0,5 |
| Случаи регистрации синдрома удлиненного интервала Q–T в семье | 1 |
| Случаи внезапной смерти неустановленной этиологии у членов семьи в возрасте младше 30 лет | 0,5 |
Относительно единиц измерения этого показателя и других интервалов ЭКГ, которые корригируются формулой H. Bazett, существует несколько разных точек зрения. Согласно вышеуказанной формуле, были предложены измерения в единицах с-1, тем не менее измерение в секундах и миллисекундах намного удобнее в практическом плане и имеет логическое обоснование.
В научных исследованиях, кроме ранних уравнений коррекции (формула H. Bazett), используют другие способы и формулы, основанные на уравнениях линейной регрессии (приложения 4–6).
Дисперсия интервала Q–T (dQ–T) показывает неоднородность желудочковой реполяризации миокарда. Ее определяют как разность между наибольшим и наименьшим значениями интервала Q–T в 12 стандартных отведениях ЭКГ:
dQ–T=Q–Tmax—Q–Tmin.
Стандартные 12 отведений ЭКГ рекомендуется записывать в покое, в дневное время, при скорости 50 мм/c на 12-канальном электрокардиографе, а интервалы Q–T измерять во всех 12 (минимум 8) отведениях, не менее 2 в каждом. Единицы измерения — миллисекунды (мс).
Корригированная дисперсия интервала Q–T (dQ–Tc) — величина, которая вычисляется при применении формулы определения dQ–T к корригированным интервалам Q–T:
dQ–Tc=Q–Tcmax—Q–Tcmin.
При исследовании 4866 лиц разных возрастных групп установлено, что и у здоровых людей, и у пациентов с разной кардиальной патологией при использовании автоматического метода обработки ЭКГ верхняя граница нормального значения dQ–T — 50 мс является достаточно достоверным критерием. Пороговое значение 50 мс, по данным D. Dabar и соавторов (1996), предусматривает внезапную сердечную смерть с 92% чувствительностью и 43% специфичностью.
Стандартизованная дисперсия Q–T (dQ–Tadj) — дисперсия Q–T, которая делится на квадратный корень из использованных в подсчете отведений (N):
dQ–Tadj=dQT/√N.
Смысл этой формулы заключается в том, чтобы иметь возможность сравнивать между собой результаты анализов ЭКГ, при которых использовали разное количество отведений. Авторы метода считают, что чем меньше отведений использовалось в вычислениях (по техническим или каким-либо другим причинам), тем большая вероятность получения заниженного значения dQ–T. Формула тем значительнее уменьшает результат подсчета, чем больше отведений используют в анализе. Так же эту формулу применяют и по отношению к частотно корригированным показателям (dQ–Tadj).
Следует отметить, что вместе с этим наиболее распространенным и наиболее простым с математической точки зрения маркером негомогенной реполяризации были предложены и другие более сложные показатели, такие как коэффициент вариации и стандартное отклонение значений продолжительности интервала Q–T от его среднего значения. Одним из перспективных подходов к анализу негомогенной реполяризации можно считать исследование неоднородности морфологии конечной части зубца Т, но данный метод требует наличия соответствующего аппаратно-программного обеспечения.
Интервал J–T — современный показатель, который характеризует исключительно процессы реполяризации миокарда желудочков. В отличие от интервала Q–T, точкой отсчета этого интервала является точка J (место перехода конечной части комплекса QRS в сегмент ST).
Корригированный интервал J–T (J–Tc) — производная от интервала J–T, полученная по формуле: J–Tc = J–T/√R–R, где J–T и R–R — интервалы, измеренные на ЭКГ, J–Tc — корригированный интервал J–T.
Корригированная дисперсия интервала J–T (dJ–Tc) исчисляется по формуле:
dJ–Tc=J–Tcmax—J–Tcmin.
МЕТОДИКА ОПРЕДЕЛЕНИЯ ИНТЕРВАЛА Q–Т И ЕГО ДИСПЕРСИИ. НОРМАЛЬНЫЕ ЗНАЧЕНИЯ
Интервал Q–T и его дисперсию могут определять при анализе:
- 8–12 отведений поверхностной ЭКГ;
- ортогональных отведений X, Y, Z по Франку ЭКГ высокого разрешения;
- данных суточного холтеровского мониторирования ЭКГ.
Интервал Q–T, его дисперсия при поверхностной ЭКГ
В основе диагностики любых форм синдрома удлиненного интервала Q–T лежит корректное измерение точности оценки продолжительности интервала Q–T. Основные трудности обычно возникают при определении начала зубца Q и конца зубца Т, а также при необходимости дифференциации зубцов T и U, в случае наличия последнего.
Проблема дисперсии начала комплекса QRS, которая проявляется в неодновременном начале электрической систолы желудочков в разных отведениях, решается использованием следующего стандарта: началом интервала Q–T считают самую раннюю точку комплекса QRS, которая соответствует переходу изоэлектрической линии сегмента PQ (R) в зубец Q (R).
Следующей технической проблемой является необходимость корректного определения окончания зубца Т. При синусовой брадикардии, гипокалиемии, синдромах удлиненного Q–T и при некоторых других состояниях зубец U, обычно не выраженный на ЭКГ, достигает амплитуды, равной амплитуде зубца Т. В ряде случаев эти два зубца настолько близко расположены один к другому, что интервал T–U не успевает достичь изолинии — случаи так называемого слияния T и U. В наиболее неблагоприятном варианте такого слияния отсутствует даже впадина между зубцами T и U, что практически исключает возможность определить истинное окончание зубца Т по морфологии конечной части электрической систолы в одном кардиоцикле. На сегодня эта проблема имеет несколько вариантов решения. При наличии разделительной выемки между зубцами T и U окончание зубца T может быть определено как наиболее углубленное место разделительной выемки и пересечение с изолинией, касательной к наиболее отвесному участку нисходящей части зубца Т (классический метод Лепешкина), или отрезка, который совмещает вершину и наиболее отвесный участок нисходящей части зубца Т (модифицированный метод Лепешкина), математическое продолжение нисходящей части зубца Т до пересечения с изолинией в виде экспоненциальной или параболической кривой, результат комбинированного анализа разбитого на сегменты кардиоцикла.
В случае необходимости дифференцировать двухфазный зубец Т или расщепленный зубец Т с апикальной выемкой от неполного слияния зубцов Т и U, используют следующие критерии (Pinsky D. и соавт.):
1) зубец U имеет наибольшую амплитуду в отведениях V2–V3;
2) при многоканальной регистрации амплитуда зубца U в 98% случаев находится в пределах 25% от наибольшего значения амплитуды зубца Т во всех отведениях и, как правило, не превышает 50% амплитуды зубца Т в этом же отведении;
3) амплитуда зубца U колеблется согласно колебаниям зубца Т;
4) при сравнении сопредельных отведений зубцы U в них практически не отличаются по амплитуде и продолжительности;
5) для разделительного углубления между зубцами Т и U типичным является резкое изменение амплитуды;
6) продолжительность разделительной выемки между зубцами Т и U обычно превышает 0,15 с, тогда как расстояние между вершинами расщепленного зубца Т меньше этой величины.
В случае изоэлектрического зубца Т определить настоящую продолжительность интервала Q–T практически невозможно, поэтому в анализ отведения с подобными комплексами QRST не включаются.
Еще одна проблема связана с логическим обоснованием выбора отведений стандартной ЭКГ для дальнейшего анализа, поскольку возникает закономерный вопрос: правомерно ли сопоставлять результаты, полученные при анализе 12 отведений и, скажем, 7? Не занижается ли значение дисперсии при анализе неполного набора отведений? Компромиссным можно считать решение, предложенное участниками Роттердамского исследования, которые доказали, что в комплект исследуемых отведений необходимо включение лишь 8 из 12 стандартных отведений (6 прекардиальных отведений по Вильсону и I, II по Эйнтховену), поскольку остальные отведения по Эйнтховену и Голдбергеру могут быть получены математическим путем из двух вышеуказанных: III=II—I; aVR=(I+II):2; aVL=(I—III):2; aVF=(II+III):2. Согласно приведенному выше математическому обобщению в качестве двух стандартных отведений по Эйнтховену могут быть использованные любые два — I, II и III.
Источником погрешности при измерении дисперсии Q–T в отведениях является также использование в анализе неодновременно полученных записей по отведениям. В случае регистрации ЭКГ на одно-, двух- или трехканальном электрокардиографе происходит смешивание показателей дисперсии и вариабельности Q–T, что может изменить результат измерения в непредвиденную сторону.
Использование автоматизированных систем обработки ЭКГ для оценки продолжительности реполяризации миокарда и ее негомогенности
Для более точной оценки реполяризации рекомендуется использовать динамическую ЭКГ (холтеровское мониторирование).
Можно использовать 3 псевдоортогональных отведения по Франку: X, Y, Z ЭКГ высокого разрешения, которые позволяют проводить более адекватную автоматическую калькуляцию продолжительности интервала Q–T, избегать дополнительных препятствий, использовать другие возможности для анализа сердечного цикла (оценка дисперсии реполяризации и ППЖ).
Из-за ограниченного числа отведений, постуральных изменений, дислокации электродов, артефактов и малоизученного влияния суточных колебаний вегетативной регуляции ритма сердца на динамику интервала Q–T, его оценка при холтеровском мониторировании более сложна, чем на ЭКГ покоя. Тем не менее, многими авторами показано преимущество этого метода, связанное с возможностью автоматического анализа около 100 тыс. интервалов R–R и Q–T (Q–Tmax, Q–Tmin, Q–Tc), измеренных в основном в отведении СМ5 (V5).
В ряде исследований продемонстрирована высокая корреляция между продолжительностью интервала Q–T, измеренного одновременно на стандартной ЭКГ и при холтеровском мониторировании ЭКГ. Так, в работе J. Christiansen и соавторов измерения проводили «вручную» двумя независимыми экспертами в отведениях V1 и V5 у 14 больных в возрасте 4–36 лет при скорости записи 25 мм/с. Всего было проанализировано 100 пар измеренных интервалов Q–T. При сравнении двух методов измерения, особенно в отведении V5, отмечена высокая корреляция: r от 0,872 до 0,988. При анализе результатов холтеровского мониторирования ЭКГ интервал Q–T максимальный (Q–Tmax), минимальный (Q–Tmin), корригированный (Q–Tc), измеряют в основном в отведении СМ1 (V5). Анализируя результаты 650 измерений Q–T с 18 холтеровских лент, P. Laguna и соавторы получили различия между значениями интервала Q–T при автоматическом и «ручном» измерении в среднем на 2,417 мс. R. Baranowski с соавторами, анализируя результаты автоматического определения длительности Q–T интервала при холтеровском мониторировании ЭКГ у здоровых и пациентов с кардиальной патологией, изучили воспроизводимость измерения данного показателя. Оказалось, что она наиболее выражена в диапазонах ЧСС 75–80 и 95–100 уд./мин.
При холтеровском мониторировании ЭКГ многие исследователи применяют оценку dQ–T по анализу двух стандартных каналов записи — СМ1 и СМ5. К сожалению, сегодня отсутствуют единые критерии оценки допустимых значений dQ–Tc у пациентов с ИБС при анализе записей холтеровского мониторирования ЭКГ. N. McLaughlin и соавторы (1996) сравнили в своей работе четыре наиболее часто используемых алгоритма для автоматизированных систем: простой и дифференциальный пороговый (threshold) методы, метод перехвата нисходящей кривой зубца Т (slope intercept) и метод продолжения отрезка между верхушкой и точкой соприкосновения нисходящей кривой зубца Т с изолинией (peak slope intercept). Первые два метода определяют конец волны Т как место ее последнего пересечения с некоторым пороговым уровнем, который подбирается эмпирически в зависимости от уровня шумов и степени усиления сигнала. Остальные два алгоритма являются модификациями тангенциального метода. В результате установлено, что погрешность при использовании этих алгоритмов у пациентов с кардиальной патологией была вдвое выше, чем у здоровых лиц, что авторы объясняют более низким средним значением амплитуды зубца Т в 1-й группе. Также получена более высокая достоверность при использовании тангенциального метода.
I. Savelieva и соавторы (1998) при исследовании у здоровых добровольцев, больных, перенесших ИМ, и пациентов с ГКМП пороговый метод использовали только для исключения из анализа отведений с недостаточной амплитудой зубца Т. В дальнейшем окончание зубца Т определяли алгоритмом подбора наименьшего квадрата (least-square fitting), а верхушку зубца Т — методом регионального центрирования (regional centering). При анализе подобным методом серий ЭКГ от одного и того же пациента и дальнейшей статистической обработке результатов всех пациентов получен достаточно низкий коэффициент вариабельности (до 2%) как проявление высокой воспроизводимости метода. Этими же авторами проведено сравнение результатов автоматического и мануального анализа ЭКГ.
Представляют интерес данные о суточных ритмах дисперсии dQ–T, полученные при холтеровском мониторировании ЭКГ. Выявлено достоверное увеличение дисперсии интервала dQ–T ночью и в утренние часы, что, вероятно, и повышает риск внезапной смерти в настоящее время у лиц с различными сердечно-сосудистыми заболеваниями (ишемия и ИМ, СН и др.).
Физиологические факторы (возраст, пол, нейроэндокринная система, физическая нагрузка, масса тела, охлаждение), влияющие на процессы реполяризации желудочков
Клинические и экспериментальные работы свидетельствуют о том, что величина интервала Q–T и его дисперсия зависят от пола обследуемого. По данным стандартной ЭКГ покоя у женщин длиннее интервал Q–Tc, меньшая дисперсия данного интервала dQ–Tc, меньшая амплитуда и продолжительность зубца Т, чем у мужчин. Во время физической нагрузки при повышении ЧСС Q–T-интервал становится более длинным у женщин по сравнению с мужчинами, то есть является более постоянной величиной. Возможно, именно этим можно объяснить более высокий риск возникновения torsade de pointes на фоне приема антиаритмических препаратов, способных удлинять этот интервал, и более частые проаритмогенные эффекты этой группы препаратов у женщин. Подобные отличия могут быть связаны с влиянием эстрогена и прогестерона, а также особенностями вегетативной нервной системы у лиц женского пола.
Половые различия в продолжительности и дисперсии интервала Q–T становятся заметными в пубертатный период, максимально выражены в возрасте 24–25 лет и снова нивелируются к 70-летнему возрасту. Изменение тонуса нейроэндокринной регуляции сердца выявляют при холтеровском мониторировании ЭКГ, когда в суточном цикле происходит постоянное изменение уровня физической и эмоциональной активности, осуществляются сложные перестройки функциональных систем организма при переходе от сна к активности.
Значение дисперсии dQ–T в период беременности сроком 36–40 нед превышают показатели здоровых женщин. Отмечено наличие достоверной положительной корреляции между дисперсией Q–T и массой тела. Хотя повышение этого показателя у тяжелоатлетов связывают с физиологической гипертрофией миокарда ЛЖ, характерной для спортсменов.
Установлено влияние охлаждения организма на негомогенность процессов реполяризации желудочков в сторону значительного повышения данного показателя.
СИНДРОМ УДЛИНЕННОГО ИНТЕРВАЛА Q–T: КЛАССИФИКАЦИЯ, ЭТИОЛОГИЯ, ПАТОГЕНЕЗ, ДИАГНОСТИКА
Классификация синдрома удлиненного интервала Q–T. История открытия
Установлено, что как врожденные, так и приобретенные формы удлинения интервала Q–T являются предикторами фатальных нарушений ритма, которые, в свою очередь, приводят к внезапной смерти больных. Существует несколько критериев, положенных в основу классификации удлинения интервала Q–T:
Приобретенное удлинение интервала Q–T
1. Острое:
а) отравление веществами, оказывающими кардиотоксическое действие (фосфор, мышьяк, ртуть) и замедляющими процесс реполяризации желудочков:
- антиаритмическими препаратами (хинидина сульфат, дизопирамид, прокаинамид, амиодарон, соталол, аймалин);
- психотропными средствами (амитриптиллин, хлорпромазин);
- β-адреномиметиками (сальбутамол, фенотерол);
- артериальными вазодилататорами (дигидропиридины, фентоламин);
- антибиотиками (эритромицин, галофантрин, хлороквин);
- антигистаминными средствами (астемизол, терфенадин);
- диуретиками (фуросемид);
- прокинетиками (метоклопрамид, цизаприд);
б) острое нарушение электролитного баланса (гипокалиемия, гипокальциемия, гипомагниемия) вследствие применения диуретиков;
в) нарушения со стороны ЦНС:
- травма головного мозга;
- субарахноидальное кровоизлияние;
- опухоль;
- тромбоз;
- эмболия;
г) острый ИМ;
д) инфекционный или аллергический миокардит.
Согласно рекомендациям Ассоциации кардиологов Украины по внезапной кардиальной смерти неинвазивными предвестниками пируэт-тахикардии вследствие проаритмогенного действия препаратов является длительность интервала Q–T >600 мс, удлинение интервала Т–U, наличие T-alternans (колебание конфигурации и амплитуды зубца Т), изменение конфигурации T–U в постэкстрасистолическом комплексе, а также наличие маленьких пируэтов (torsadelets).
2. Хроническое:
а) хронические заболевания сердечно-сосудистой системы (разные формы ИБС, АГ, ДКМП, ГКМП, застойная СН, пролапс митрального клапана, врожденные пороки сердца);
б) патологические состояния, не связанные с первичным поражением сердца (сахарный диабет, ХОБЛ, терминальная стадия ХПН, болезнь Бехчета, неврогенная анорексия, низкобелковая диета, хронический алкоголизм, остеогенная саркома, карцинома легкого, семейный периодический паралич, яд скорпионов, синдром Конна, феохромоцитома, гипотермия, ваготония).
Врожденное удлинение интервала Q–T
1. По этиологии: наследственные формы: синдром Джервелл —Ланге-Нильсена (сочетание приступов потери сознания и внезапной смерти с врожденной глухонемотой) и синдром Романо — Уорда (без врожденной глухонемоты).
2. По клиническим проявлениям:
- синкопе + удлинение интервала Q–T (38%);
- изолированное удлинение интервала Q–T (40%);
- синкопе без удлинения интервала Q–T (11%);
- скрытая форма — латентное течение синдрома (11%).
3. Молекулярно-генетические варианты синдрома удлиненного интервала Q–T (табл. 2.1).
Таблица 2.1
Молекулярно-генетические варианты синдрома удлиненного интервала Q–T
| Вариант | Локализация | Ген | Белковый продукт |
| LQ–T1 | 11p15.5 | KCNQ1 (KvLQ–T1) | α-субъединица калиевого канала |
| LQ–T2 | 7q35–36 | HERG | α-субъединица калиевого канала |
| LQ–T3 | 3p21–24 | SCN5A | натриевый канал |
| LQ–T4 | 4q25–27 | ? | ? |
| LQ–T5 | 21q22.1–22 | KCNE1 (MinK) | β-субъединица калиевого канала |
| LQ–T6 | 21q22.1–22 | KCNE2 (MiRP 1) | β-субъединица калиевого канала |
| JLN1 | 11p15.5 | KCNQ1 | α-субъединица калиевого канала |
| JLN2 | 21q22.1–22 | KCNE1 | β-субъединица калиевого канала |
История открытия синдрома, наиболее вероятно, начинает отсчет с 1856 г., когда T. Meissner описал внезапную смерть во время стрессовой ситуации молодого человека, в семье которого еще двое детей умерли при аналогичных обстоятельствах. Только через 100 лет, в 1957 г. A. Jervell и F. Lange-Nielsen представили полное клиническое описание синдрома удлиненного интервала Q–T у четверых членов одной семьи с врожденной глухотой, частыми приступами потери сознания и стойким удлинением интервала Q–T на ЭКГ. Вскоре C. Romano (1963) и O. Ward (1964) предоставили наблюдение аналогичного синдрома, но без врожденной глухоты. С того времени известны два варианта наследственного синдрома удлиненного интервала Q–T: Романо — Уорда (аутосомно-доминантный и аутосомно-рецессивный) и Джервелла — Ланге-Нильсена. В последнем случае удлинение Q–T сочетается с врожденной глухотой.
Распространенность
Установлено, что синдром Романо — Уорда определяют в популяции с частотой 1:1 0000, а в детском возрасте 1:5000-1:7000. Синдром Джервелла — Ланге-Нильсена — редчайшая патология. Согласно данным G. Fraser, данный синдром отмечали в популяции 4-10 пожилых людей Соединенного Королевства с частотой 1,6 на 1 млн. По данным J. Bricker (1984), синдром удлиненного интервала Q–T с высокой частотой выявляют у лиц с пароксизмальными состояниями, а у детей с врожденной глухотой — около 0,8%. При обследовании групп пациентов с кардиогенными синкопальными состояниями синдром отмечали в 36% случаев. Есть указания на высокую частоту выявления патологического удлинения интервала Q–T при сопутствующем ЭКГ-обследовании.
Этиология и патогенетические механизмы наследственного синдрома удлиненного интервала Q–T
Этиология синдрома до недавнего времени оставалась до конца не изученной, хотя выявление заболевания у нескольких членов одной семьи позволило практически с момента первого описания рассматривать его как наследственную патологию. В патогенезе синдрома удлиненного интервала Q–T ведущая роль принадлежит нескольким основным гипотезам. Одна из них — гипотеза симпатического дисбаланса предполагает нарушение правосторонней симпатической иннервации сердца с преобладанием левосторонних симпатических влияний. Но в качестве основной существует гипотеза внутрисердечных аномалий, которая согласуется с теорией о патологии ионных каналов. Мутации в генах, ответственных за развитие синдрома удлиненного интервала Q–T, приводят к нарушению функционирования ионных каналов (калиевого или натриевого) и увеличению продолжительности ПД в кардиомиоците, что облегчает появление ранних или поздних последеполяризаций и, таким образом, полиморфной желудочковой тахикардии типа пируэт (torsades de pointes). По механизму развития желудочковых тахикардий все врожденные синдромы удлиненного интервала Q–T выделяют в группу адренергически зависимых (желудочковая тахикардия у таких больных развивается на фоне повышенного симпатического тонуса), тогда как синдромы приобретенного удлинения интервала Q–T составляют группу паузозависимых (желудочковая тахикардия, преимущественно пируэтная, возникает после удлиненного интервала R–R в виде нескольких повторений патерна, который ускоряется, «длинный R–R — короткий R–R»). Распределение это довольно условно, поскольку есть данные о наличии, например идиопатического паузозависимого синдрома удлиненного Q–T. Кроме того, зарегистрированы случаи, когда прием медикаментов приводит к манифестации бессимптомного прежде врожденного синдрома удлиненного интервала Q–T.
Критерии диагностики
В 1985 г. P. Schwartz предложил применять диагностические критерии, которые были дополнены в 1993 г.
Большие:
- удлинение Q–Tc >440 мс на ЭКГ покоя;
- синкопе;
- случаи выявления удлинения Q–T в семье.
Малые:
- врожденная глухота;
- альтернация зубца Т;
- низкая ЧСС;
- нарушение процесса реполяризации миокарда желудочков.
Синдром удлиненного интервала Q–T диагностируют при наличии двух больших или одного большого и двух малых критериев. Существует также балльная система для установления диагноза синдрома удлиненного интервала Q–T (см. табл. 2.2). При сумме <1 балл диагноз маловероятен; 2–3 балла — средняя достоверность синдрома удлиненного интервала Q–T; >4 баллов — высокая достоверность данного диагноза.
При отсутствии возможности проведения молекулярно-генетических исследований до настоящего времени клиническая диагностика остается наиболее точной и надежной. При этом наиболее труден именно первый шаг — подтверждение наличия наследственного синдрома удлиненного интервала Q–T у пробанда. Дальнейшая диагностика в сомнительных клинических случаях облегчена в связи с высокой вероятностью повторных случаев в пораженных семьях. Синкопе — наиболее общее проявление синдрома, впервые возникает в возрасте 5–15 лет, у мужчин чаще, чем у женщин. Возраст, в котором появляется первый синкопе, имеет прогностическое значение — если в возрасте до 5 лет, — то предопределяет тяжелую форму болезни, а если синкопе регистрируют на 1-м году жизни, то это ассоциируется с чрезвычайно плохим прогнозом. Наличие остановки сердца в анамнезе повышает в 13 раз риск остановки сердца или внезапной коронарной смерти в дальнейшем, что является жесткой мотивацией для использования кардиовертера-дефибриллятора у такой категории больных. При анализе факторов, провоцирующих синкопе, установлено, что практически у 40% больных их регистрируют на фоне сильного эмоционального возбуждения (гнев, страх). Приблизительно в 50% случаев приступы провоцируются физической нагрузкой (исключая плавание), у 20% детей — плаванием, у 15% они происходят во время пробуждения от ночного сна, у 5% — как реакция на резкие звуковые раздражители (телефонный звонок, звонок в дверь и др.). Таким образом, эмоциональное возбуждение и физическая активность в равной степени являются аритмогенными факторами для детей с синдромом удлиненного интервала Q–T.
ЭКГ имеет нередко определяющее значение в диагностике основных клинических вариантов синдрома. Увеличение длительности интервала Q–T более чем на 50 мс по отношению к нормальным значениям для данной ЧСС должно насторожить исследователя в плане исключения синдрома удлиненного интервала Q–T. Практика показывает, что за исключением детей раннего возраста, при наследственном синдроме удлиненного интервала Q–T этот интервал, как правило, всегда >400 мс. В сомнительных случаях необходимо дифференцировать первичное и вторичное удлинение Q–T с помощью анализа других маркеров ранней коронарной смерти. Величина интервала Q–T на ЭКГ покоя у больных с синкопальной формой заболевания колеблется от 400 до 650 мс. У больных с бессинкопальной формой синдрома продолжительность этого интервала достоверно меньше и в среднем составляет 440–450 мс.
Холтеровское мониторирование позволяет установить значение максимальной продолжительности интервала Q–T, которая не должна превышать:
- 400 мс — у детей раннего возраста;
- 460 мс — у детей дошкольного возраста;
- 480 мс — у детей школьного возраста;
- 500 мс — у взрослых.
Следует отметить, что критерии удлинения интервала Q–T (по данным холтеровского мониторирования ЭКГ) не входят в диагностические критерии, предложенные P. Schwartz (1985; 1993).
Анализ предикторов синкопе и внезапной смерти у больных с синдромом удлиненного интервала Q–T показал, что в детском возрасте маркеры риска несколько отличаются от таковых у взрослых. Так, если риск внезапной смерти при синдроме выше среди женщин, то по данным клиники Федерального детского центра диагностики и лечения нарушений ритма сердца (Россия, Москва), наиболее злокачественное течение синдрома в детском возрасте отмечают именно у мальчиков. Неинформативным у детей является Q–Tc >460 мс, поскольку отмечают не только у всех детей с синкопе, но и у 90% — без синкопе. Кроме того, относительная редкость выявления у детей желудочковой экстрасистолии на ЭКГ покоя затрудняет использование этого признака как предиктора внезапной смерти при данном способе регистрации.
До настоящего времени стратификация риска главным образом основана на наличии в анамнезе синкопальных эпизодов, torsade de pointes (мерцание-трепетание желудочков) или остановки сердца. Продолжительность корригированного интервала Q–T >600 мс — более слабый предиктор возникновения основных проявлений. Таким образом, мониторирование основных клинико-электрофизиологических маркеров риска ранней коронарной смерти при синдроме удлиненного интервала Q–T позволяет своевременно назначить лечение и избежать осложнений, проводить профилактику угрожающих жизни аритмий у лиц с латентной и бессинкопальной формами заболевания.
СИНДРОМ УКОРОЧЕННОГО ИНТЕРВАЛА Q–T
На протяжении последних 10 лет укорочение интервала Q–Tc рассматривают у больных с идиопатической желудочковой тахикардией. Существует две формы данного синдрома:
1) постоянная, ЧСС не влияет;
2) транзиторная, определяющаяся в связи с замедлением ритма сердца. Обусловлена:
- генетическими нарушениями;
- гипертермией;
- повышением содержания кальция или калия в плазме крови;
- ацидозом;
- нарушением тонуса автономной нервной системы.
Клинические проявления этого синдрома таковы: сердцебиение, перебои в работе сердца, головокружение, потеря сознания, наличие в семье случаев внезапной смерти в молодом возрасте, начиная с самого раннего детского возраста. Заболевание отмечают у лиц мужского и женского пола, наследуется по аутосомно-доминантному типу.
Молекулярно-генетические нарушения у таких больных регистрируют в миокарде желудочков и предсердии. Поэтому у них выявляют как желудочковые, так и наджелудочковые нарушения ритма.
Критерии диагностики синдрома укороченного интервала Q–T:
- продолжительность интервала Q–Tc <300 мс;
- семейные случаи внезапной смерти в молодом возрасте;
- наличие укороченного интервала Q–Tc у некоторых членов семьи;
- укорочение рефрактерных периодов предсердий и желудочков, которые выявляют с помощью внутрисердечной электрокардиостимуляции;
- снижение порога фибрилляции предсердий и желудочков во время программированной электрокардиостимуляции.
На сегодня обоснованным методом лечения считается лишь имплантация кардиовертера-дефибриллятора.
ИНТЕРВАЛ Q–T, ДИСПЕРСИЯ Q–Т У ПАЦИЕНТОВ С ИБС С ЖЕЛУДОЧКОВЫМИ АРИТМИЯМИ
Ишемия и Q–T
В исследовании по изучению диагностического и прогностического значения интервала Q–T, его дисперсии (dQ–T) у лиц с ИБС (Сычев О.С., Епанчинцева О.А., 2005) было показано, что у больных стенокардией напряжения II–III ФК увеличение дисперсии корригированного интервала Q–T >50 мс может служить маркером ишемии миокарда с достоверно высокой специфичностью. Увеличение dQ–Tc при стрессовом тестировании на высоте нагрузки >50% начального уровня является диагностическим признаком ИБС. А в случае, если положительными оказываются 2 критерия теста (депрессия сегмента ST >1 мм и повышение dQ–Tc при нагрузке >50%) специфичность теста резко возрастает (96,6%). A. Demir и соавторы (2001) выявили, что между количеством пораженных коронарных артерий у лиц с ИБС и значением dQ–Tc существует положительная корреляция (r=0,49; p<0,0001). Кроме того, по данным работы О. Швеца (1998), при катетеризации сердца больным с установкой биполярного водителя ритма отмечено, что степень изменения dQ–T связана со степенью тяжести ИБС.
Интервал Q–T и нестабильная стенокардия
В исследовании B. Sredniawa и соавторов (2000) показано, что у лиц с ИБС с нестабильным течением анализ неоднородности желудочковой реполяризации позволил выделить пациентов с высоким риском ранней коронарной смерти. При этом не выявлена высокая ассоциация dQ–Tc с развитием ИМ и необходимостью ургентной реваскуляризации миокарда у обследуемых больных.
По данным работы О.С. Сычева, О.А. Епанчинцевой (2005), у лиц с ИБС с желудочковыми аритмиями (n=193) предвестником ее неблагоприятного течения (нестабильной стенокардии) может быть интервал Q–Tc >440 мс, а предикторами развития больших кардиальных событий (кардиальной смерти, включающей внезапную кардиальную смерть, нефатальный ИМ) у таких больных может быть удлинен корригированный интервал Q–Tc (>440 мс) и увеличена дисперсия dQ–Tc (>50 мс). Эти данные подтверждаются результатами исследования связи увеличения негомогенной реполяризации с наличием ишемии при нестабильной стенокардии, причем показатель dQ–T коррелировал в данной работе с уровнем специфического для ишемии миокарда тропонина Т в плазме крови (Ashikaga T., 1998).
Интервал Q–T, его дисперсия у больных ИМ
В исследовании Н. Parikka и соавторов (1999) показано быстрое уменьшение dQ–T и частоты желудочковых аритмий на фоне внутривенной инфузии сульфата магния в острой фазе ИМ. Авторы не выявили влияния на вышеуказанные изменения локализации инфаркта, разности в частоте ишемических эпизодов и в показателях вариабельности сердечного ритма между пациентами, у которых применяли магний, и контрольной группой. Это позволяет предположить, что одной из основных причин негомогенной реполяризации и наличия желудочковых аритмий у данной категории больных является электролитный дисбаланс, который развивается местно в зоне инфаркта. В исследованиях, проведенных с участием большого количества больных ИМ с нормальными и сниженными значениями ФВ ЛЖ (<40%) не установлено четкой связи между повышенными значениями dQ–T в ранние сроки инфаркта и кардиальной смертностью, тем не менее такая связь выявлена для показателей dQ–T в подострый период (1 мес с момента развития заболевания). Установлено достоверное уменьшение dQ–T на 10-е сутки ИМ при проведении эффективной тромболитической терапии, причем этот показатель был значительно выше при поражении передней межжелудочковой ветви левой коронарной артерии, то есть при передней локализации ИМ.
В работе А.Н. Пархоменко, А.В. Шумакова (2003) получены данные об отсутствии подобной динамики относительно продолжительности самого интервала Q–T, не выявлена достоверная связь между dQ–T в подострый период ИМ и локализацией нарушений коронарного кровотока. На основании анализа негомогенной реполяризации по данным стандартной ЭКГ и усредненной ЭКГ высокого разрешения в псевдоортогональных отведениях Франка X, Y, Z у больных на протяжении первых 2 нед острого ИМ, были предложены диагностические критерии неблагоприятного течения острого периода ИМ (табл. 2.3).
Таблица 2.3
Диагностические критерии, полученные на основании анализа негомогенной реполяризации по данным стандартной ЭКГ и усредненной ЭКГ высокого разрешения (ВР) в псевдоортогональных отведениях Франка X, Y, Z в динамике первых 2 нед острого ИМ
| Критерий | Позволяет выявить | Показатель диагностической значимости, % | p | |||
| Чувствительность | Специфичность | Положительная прогностическая значимость | Отрицательная прогностическая значимость | |||
| dJ–Tc ортогональное отведение ЭКГ ВР >52 мс (3-и сутки острого ИМ) |
Риск продолжительного персистирования острой левожелудочковой недостаточности | 71 | 59 | 19 | 94 | <0,05 |
| dJ–T ортогональное отведение ЭКГ ВР >38 мс (3-и сутки острого ИМ) |
Риск развития ранней (до 10 сут после острого ИМ) постинфарктной стенокардии | 100 | 51 | 14 | 100 | <0,01 |
| dQ–T ортогональное отведение ЭКГ ВР >50 мс (конец 2-й недели острого ИМ) |
Наличие электрической нестабильности миокарда (риск развития стойкой желудочковой тахикардии при проведении программированной стимуляции желудочков сердца) | 67 | 82 | 40 | 93 | <0,05 |
| dQ–Tc ортогональное отведение ЭКГ ВР >31 мс (10-е сутки острого ИМ) |
Наличие резидуальной ишемии в инфарктной зоне до конца 2-й недели острого ИМ | 81 | 58 | 61 | 79 | <0,01 |
Интервал Q–T, его дисперсия у больных с постинфарктным кардиосклерозом
При анализе дисперсии в разные сроки после перенесенного ИМ выявили, что низкие значения dQ–Tc связаны с сохраненной функцией ЛЖ, тогда как прогрессирующее повышение показателя негомогенной желудочковой реполяризации ассоциируется с дилатацией ЛЖ, нарушением систолической и диастолической функций ЛЖ. Таким образом, у лиц с ИБС, которые перенесли ИМ, отмечают увеличение dQ–Tc как в острый период, так и через 1 год, что свидетельствует о нарушении процессов реполяризации у данной категории больных.
Исследование С. Schneider и соавторов (1997) dQ–T <70 мс с чувствительностью 83% и специфичностью 71% позволила выделить больных, у которых восстановление коронарного кровотока в постинфарктный период приводило к выраженному улучшению насосной функции ЛЖ.
В исследованиях продемонстрировано значительное снижение негомогенной реполяризации как в ближайшие, так и в отдаленные сроки после реваскуляризации миокарда, отмечены значительно более высокие начальные показатели и более выраженная динамика уменьшения dQ–T у больных, проведение ангиопластики у которых было осложнено развитием летальных аритмий. Рестенозирование ассоциировалось с повышением, а повторная ангиопластика — со снижением значений dQ–T.
Желудочковые аритмии и процессы реполяризации в миокарде
Негомогенность процессов реполяризации в миокарде желудочков является причиной его электрической нестабильности. Отдельные участки миокарда находятся в разных фазах как де-, так и реполяризации, создавая условия для появления дополнительных очагов возбуждения, что и служит субстратом для возникновения опасных для жизни аритмий и ранней коронарной смерти. Данные о достоверной связи между индукцией желудочковой тахикардии и удлинением интервала Q–T с повышением его дисперсии, полученные в исследованиях, подтверждают ценность этих показателей как неинвазивных маркеров желудочковых аритмий.
Установлено, что у лиц с желудочковой экстрасистолией II–IV класса по B. Lown согласно данным суточного мониторирования ЭКГ значения интервалов Q–Tmax, Q–Tmin, Q–Tc и dQ–Tc были достоверно большими по сравненю с больными без желудочковых нарушений ритма. Частота возникновения эпизодов неустойчивой желудочковой тахикардии выше у лиц с удлиненным интервалом Q–Tc (Сычев О.С., Епанчинцева О.А., 2005). В отличие от пациентов с хронической формой ИБС, у лиц с острым ИМ предикторная ценность временных параметров интервала Q–T по распознаванию потенциально опасных нарушений ритма сердца значительно возрастала. Чувствительность и специфичность увеличенной dQ–T при ее пороговом значении >50 мс составили 82,2 и 85,8% соответственно. При пороговом значении данного показателя >70 мс чувствительность возрастала до 88,1%, а специфичность — до 94,5%.
Установлено, что у лиц с ИБС удлинение корригированного интервала Q–Tc >440 мс в комбинации со снижением вариабельности сердечного ритма <100 мс можно рассматривать как предикторы развития желудочковых аритмий и кардиоваскулярных событий.
Диагностическая ценность удлинения интервала Q–Tc >440 мс и увеличение dQ–Tc >50 мс для оценки риска выявления желудочковых аритмий IV класса по B. Lown на протяжении 4 лет соответственно составляет: чувствительность 24 и 23%, специфичность — 86 и 91%, положительная прогностическая значимость — 37 и 74%, отрицательная прогностическая значимость — 77% и 50%.
ИНТЕРВАЛ Q–Т И СОПУТСТВУЮЩИЕ ЗАБОЛЕВАНИЯ (АГ, САХАРНЫЙ ДИАБЕТ)
Много работ указывают на прогностическую ценность удлиненного интервала Q–Tc и увеличенной dQ–Tc по чувствительности относительно желудочковых аритмий и ранней коронарной смерти пациентов с ИБС и АГ. Прогрессирование АГ ассоциируется с увеличением продолжительности интервала Q–Tc, степенью вариабельности ритма сердца. Наличие повышенного АД, включая начальный период АГ «белого халата», сопровождается рядом неблагоприятных электрофизиологических сдвигов в миокарде ЛЖ, которые ассоциируются с гипертрофией миокарда и дисфункцией регуляции вегетативной нервной системы, имеют достоверную связь с возрастом и со степенью тяжести заболевания. L. Oikarinen и соавторы (2001) показали, что рост индекса массы миокарда ЛЖ, независимо от типа гипертрофии, ассоциировался с высокими значениями продолжительности и дисперсии интервала Q–T. Таким образом, установлена высокая частота возникновения желудочковых аритмий III–IV класса по B. Lown и высокая частота ранней коронарной смерти среди пациентов с увеличенной массой тела и измененной геометрией ЛЖ.
Мониторирование интервала Q–T рекомендуется как дополнительный специфический тест диагностики диабетической вегетативной кардиальной нейропатии. В работе И.Э. Сапожниковой с соавторами (2001) наибольшие показатели дисперсии интервала Q–T отмечены у больных сахарным диабетом II типа. С нарастанием выраженности метаболических нарушений расширяется спектр факторов, влияющих на усиление гетерогенности реполяризации, достигая максимума при сочетании АГ и сахарного диабета. Была выявлена четкая корреляция нарушений ритма сердца с дисперсией интервала Q–Tc, а увеличение дисперсии интервала Q–T у пациентов с сахарным диабетом как I, так и II типа ассоциируется только с дисфункцией автономной нервной системы. Это подтверждается корреляцией между увеличением негомогенной реполяризации и наличием автономной нейропатии по данным радиоизотопных исследований.
C. Cardoso и соавторами (2003) установлено, что удлиненный Q–Tc (>470 мс) является независимым предиктором острого нарушения мозгового кровообращения у больных сахарным диабетом II типа (HR=2,2–2,9; 95% ДИ=1,1–6,0).
Q–T, ХСН И ДКМП
На основании проспективного исследования больных СН (Barr C., 1994) сделан вывод, который dQ–T >79 мс достоверно выделяет из общей группы пациентов с высоким риском ранней коронарной смерти. У больных СН и ГЛЖ существует взаимосвязь между увеличением dQ–T и склонностью к развитию желудочковых аритмий. Работа М. Galinier и соавторов (1998) показала достоверную связь увеличения dQ–T с общей и внезапной кардиальной смертью, аритмическими эпизодами у больных ДКМП, тогда как при СН, обусловленной ИБС, увеличение dQ–T не позволило выделить пациентов высокого риска из общей группы. Кроме того, было отмечено уменьшение dQ–T при лечении СН антагонистами альдостерона.
Sakabe и соавторы (2001), сравнивая прогностическую значимость увеличения дисперсии Q–T и измененной морфологии зубца Т относительно развития опасных для жизни желудочковых аритмий у пациентов с ДКМП, предлагают использовать измененную морфологию зубца Т как ценный маркер аритмогенной готовности (чувствительность — 100%, специфичность — 35%, положительная прогностическая значимость — 54%, отрицательная прогностическая значимость — 100%).
Q–T И ГКМП
По данным многих исследований выявлено, что большие значения Q–T, dQ–T ассоциировались с неблагоприятным прогнозом у больных ГКМП; тем не менее четкой корреляции между dQ–T и ранней коронарной смертью не установлено. Большие значения dQ–T (как абсолютные, так и корригированные) отмечают у больных с ГКМП по сравнению со здоровыми, а также у пациентов с наличием тяжелых желудочковых нарушений ритма по сравнению с лицами без аритмий. В исследовании H. Elming (2001) у пациентов с СН IIA стадии и более и сниженной систолической функцией ЛЖ было проведено проспективное наблюдение 1319 больных на протяжении 18 мес. Пороговое значение dQ–T составляло 70 мс. При этом анализ выживаемости не выявил прогностического значения dQ–Tc по отношению к общей (OR=1,0; 95% ДИ=1,00–1,00; p=0,74), кардиальной (OR=1,0; 95% ДИ=1,00–1,01; p=0,55) или аритмической смертности (OR=1,0; 95% ДИ=0,99–1,01; p=0,38). Несмотря на это, отличие в величине показателя dQ–T между больными с ГКМП и здоровыми лицами подтверждается результатами разных авторов, тем не менее не установлено, является ли дисперсия интервала Q–T только электрофизиологическим феноменом, сопровождающим данную патологию, или же маркером, на основании которого можно прогнозировать возможные аритмические осложнения у таких пациентов.
ПРОГНОСТИЧЕСКАЯ ЗНАЧИМОСТЬ ИНТЕРВАЛА Q–T И ЕГО ДИСПЕРСИИ
В целом ряде проспективных исследований показана прогностическая роль значения интервала Q–T (440 мс). В Нидерландах в проспективном исследовании лиц без кардиальной патологии (1991) установлена взаимосвязь между продолжительностью интервала Q–T и риском ранней коронарной или сердечно-сосудистой смерти в течение 28-летнего наблюдения. В другом нидерландском исследовании (1994) выявлено, что мужчины с интервалом Q–T >420 мс имели более высокий риск сердечно-сосудистой смертности по сравнению с мужчинами, у которых Q–T <420 мс. В дальнейшем 28-летнее наблюдение нидерландских государственных служащих показало, что при Q–T >440 мс существенно повышалась сердечно-сосудистая смертность с OR=2,1 (1998). Результаты исследования итальянских ученых (2002), включавшего 1357 пациентов с ИБС с сахарным диабетом II типа, свидетельствуют, что Q–Tc >440 мс и dQ–Tc >80 мс могут использовать для стратификации риска лиц с ИБС. Так, в исследовании H. Elming (1998) длительностью 11 лет участвовали 3455 пациентов. При этом выявлено, что корригированный интервал Q–Tc >440 мс указывал на повышение риска смерти от сердечно-сосудистых заболеваний в 8 раз. Дальнейшие работы подтвердили наличие увеличенной dQ–T у реанимированных больных по сравнению с адекватной контрольной группой. Также было отмечено, что циркадный ритм, описывающий вариабельность интервала Q–T и его дисперсии в контрольной группе, был нарушен у пациентов с ранней коронарной смертью в анамнезе. Данные субанализа Роттердамского (1998) исследования общей популяции свидетельствуют, что увеличение dQ–T >60 мс у людей пожилого возраста является достоверным предиктором кардиальной смерти.
Исследователями отдела аритмий сердца Института кардиологии им. Н.Д. Стражеско АМН Украины в 2005 г. установлено прогностическое значение интервала Q–T и его дисперсии dQ–T у 193 больных со стенокардией напряжения, прошедших проспективное 4-летнее наблюдение. У пациентов с развитием больших кардиальных событий (кардиальной смерти, ИМ) на протяжении длительного 4-летнего наблюдения значения Q–Tc и dQ–Tc значительно превышали нормальный пороговый уровень и достоверно отличались от группы пациентов с относительно благоприятным течением ИБС. Также установлено, что доля больных с Q–Tc ≥440 мс и dQ–Tc ≥50 мс была достоверно больше в группе с развитием кардиальной смерти и/или нелетального ИМ. Частота развития больших кардиальных событий нарастала с повышением показателя корригированного интервала Q–Tc: при значении Q–Tc <440 мс большие кардиальные события развились только у 8,3% больных, при Q–Tc=440–449 мс — у 17,4% больных, при Q–Tc=450–469 мс — у 33,3%, а при Q–Tc >470 мс — у 62,5% пациентов (p<0,005).
Проранжированы общеизвестные факторы риска развития неблагоприятного прогноза у больных обследованных групп. Для измерения значения независимых предикторов вычисляли величину соотношения шансов (OR) с 95% доверительным интервалом (ДИ) (табл. 2.4). Показатели расположены в порядке снижения их информативности. Интервал Q–Tc ≥440 мс не является самым прогностически значимым.
Таблица 2.4
Независимые факторы развития кардиальных событий (кардиальной смерти, нефатального ИМ) у лиц с ИБС (по данным однофакторного анализа)
| Фактор | OR с 95% ДИ |
| Конечносистолический объем ЛЖ ≥90 мл | OR=13,88 (3,45–56,43) р=0,0013 |
| Суммарная продолжительность ишемии миокарда за сутки при холтеровском мониторировании ЭКГ ≥30 мин | OR=10,13 (2,06–49,92) p=0,0049 |
| ИМ в анамнезе | OR=7,4 (2,29–23,68) p=0,0009 |
| КДО ЛЖ ≥160 мл | OR=5,86 (1,37–25,08) p=0,0177 |
| Немая ишемия миокарда при холтеровском мониторировании ЭКГ | OR=5,80 (1,40–23,58) p=0,0157 |
| ФВ ЛЖ ≤55% | OR=5,26 (1,45–19,49) p=0,05 |
| Продолжительность интервала Q–Tc ≥440 мс | OR=4,95 (1,89–12,98) p=0,0013 |
| Пороговая нагрузка по данным ВЭМ (≤50 Вт) | OR=4,0 (1,19–13,46) p=0,0257 |
| Класс желудочковых экстрасистол по B. Lown | OR=3,49 (0,84–14,46) p=0,054 |
В работе J. Perkiomaki и соавторов (2001) на протяжении 10-летнего проспективного наблюдения 330 пациентов в возрасте старше 65 лет увеличение дисперсии Q–Tc >70 мс обусловливало рост общей смертности (OR=1,38; 95% ДИ=1,02–1,86), ранней коронарной смерти (OR=2,7; 95% ДИ=1,29–5,73), а в комбинации с показателями ГЛЖ риск развития ранней коронарной смерти резко возрастал (OR=16,52; 95% ДИ=3,37–80,89).
Результаты 6-летнего исследования AIREX (1999), включавшего 605 пациентов в острый период ИМ, осложненного СН, свидетельствуют, что увеличенная дисперсия интервала dQ–Tc (>100 мс) при однофакторном (OR=1,07; 95% ДИ=1,03–1,10; p=0,001) и многофакторном (OR=1,05; 95% ДИ=1,01–1,09; p=0,022) анализах может быть независимым предиктором риска общей смертности, но с низкой чувствительностью данного ЭКГ-маркера, что ограничивает его применение для стратификации риска пациентов с разными формами ИБС с желудочковыми аритмиями.
В табл. 2.5 показана прогностическая значимость интервала Q–Tc ≥440 мс и dQ–Tc ≥50 мс для оценки вероятности развития больших коронарных событий на протяжении 4 лет.
Таблица 2.5
Чувствительность, специфичность, прогностическая значимость Q–Tc и dQ–Tc для оценки вероятности развития больших кардиальных событий (кардиальной смерти, ИМ) на протяжении 4 лет
| Показатель | Чувствительность, % | Специфичность, % | Положительная прогностическая значимость, % | Отрицательная прогностическая значимость, % |
| Q–Tc ≥440 мс | 31 | 92 | 56 | 80 |
| dQ–Tc ≥50 мс | 18 | 91 | 70 | 46 |
Полученные результаты свидетельствуют о необходимости наиболее раннего выявления факторов риска, использования интервала Q–Tc и его дисперсии для стратификации риска больных стенокардией напряжения I–III ФК с желудочковыми аритмиями.
ИНТЕРВАЛ Q–T, ЕГО ДИСПЕРСИЯ И ВАРИАБЕЛЬНОСТЬ СЕРДЕЧНОГО РИТМА
Снижение адаптации интервала Q–T к суточным изменениям ЧСС рассматривается как патология и ассоциируется с повышенным риском развития фибрилляции желудочков. Следует отметить, что у больных с трансплантированным сердцем и редуцированием вегетативных влияний на сердце разницы между дневной и ночной динамикой интервала Q–T не выявлено. Информация относительно длительности адаптации Q–T к ЧСС (Q–T/R–R) может также служить неинвазивным маркером нарушений автономной регуляции сердца. Увеличение Q–T/R–R у больных в постинфарктный период отражает склонность к желудочковой тахикардии. У пациентов с фибрилляцией желудочков в анамнезе без органической патологии, несмотря на нормальные показатели вариабельности сердечного ритма, отмечают увеличение dQ–T и Q–T/R–R, особенно ночью и утром.
Сниженная вариабельность ритма сердца является индикатором изменения вегетативной иннервации сердца, что может обусловливать внезапное начало желудочковых аритмий, но не является специфическим маркером аритмогенного субстрата. И наоборот, удлиненный Q–Tc, отражающий замедленную и асинхронную реполяризацию миокарда желудочков, и увеличенная дисперсия dQ–Tc, отражающая негомогенную желудочковую реполяризацию, является электрофизиологическим субстратом появления триггерной активности вследствие ранних следовых деполяризаций и возникновения механизма re-entry, и, как следствие, появления желудочковых аритмий.
РОЛЬ ЛЕКАРСТВЕННЫХ СРЕДСТВ В ВОЗНИКНОВЕНИИ ПРИОБРЕТЕННОГО СИНДРОМА УДЛИНЕННОГО ИНТЕРВАЛА Q–T
Объем потребления лекарственных средств в экономически развитых странах постоянно увеличивается, вместе с тем появляется все больше сообщений о кардиотоксичности препаратов разных фармакотерапевтических групп. Список лекарственных препаратов, применение которых может привести к удлинению интервала Q–T, представлен в табл. 2.6.
Таблица 2.6
Лекарственные средства, способны вызвать удлинением интервала Q–T
| Антиаритмические | IA класс — хинидин, прокаинамид, дизопирамид, аймалин
IB класс — лидокаин, априндин, мексилетин IC класс — флекаинид, энкаинид, пропафенон III класс — соталол, амиодарон, бретилия тозилат, дофетилид, сематилид, ибутилид, азимилид IV класс — бепридил |
| Сердечно-сосудистые | Эпинефрин, эфедрин, винпоцетин |
| Антигистаминные | Астемизол, терфенадин, дифенгидрамин, эбастин, гидроксизин |
| Антибиотики и сульфаниламиды | Эритромицин, кларитромицин, азитромицин, спирамицин, клиндамицин, котримоксазол, антрамицин, даунорубицин, эпирубицин, пентамидин (внутривенно), тролеандомицин |
| Антималярийные | Галофантрин |
| Три- и тетрациклические антидепрессанты | Амитриптиллин, нортриптиллин, имипрамин, доксепин, мапротилин, фенотиазин, хлорпромазин, флювоксамин |
| Нейролептики | Галоперидол, хлоралгидрат, дроперидол, пимозид |
| Антагонисты серотонина | Кетансерин, зимелидин |
| Гастроэнтерологические | Цизаприд |
| Диуретики | Индапамид, фуросемид |
| Противогрибковые | Кетоконазол, флуконазол, итраконазол |
| Другие препараты | Кокаин, пробукол, папаверин, аденозина фосфат, лидофлазин, теродилин, бепридил, будипин, вазопрессин, препараты лития |
| Отравление | Ртуть, органотропные инсектициды |
В ходе современных исследований выявлено наличие 3 типов клеток в миокарде желудочков: эпи-, эндокардиальных и М-клеток, которые отличаются продолжительностью ПД. В отличие от других видов, М-клетки характеризуются небольшим замедлением позднего К+ тока и значительным замедлением тока ионов Na+ и натрий-кальциевого обмена. Эти отличия ионных потоков лежат в основе удлинения ПД и появления поздних деполяризаций, особенно во время терапии антиаритмическими средствами III класса, в то время как проаритмогенное действие препаратов IA класса ассоциировалось с увеличением дисперсии dQ–T. Увеличение продолжительности ПД М-клеток приводит к появлению дисперсии реполяризации в миокарде желудочков, которые C. Antzelevitch и J. Fish предлагают оценивать по поверхностной ЭКГ как интервал между вершиной и окончанием зубца Т.
Довольно часто используемый в клинической практике антиаритмический препарат дизопирамид в высоких дозах угнетает быстрые калиевые каналы, которые кодируются геном HERG, что может являться молекулярной основой приобретенного синдрома удлиненного интервала Q–T. Аналогично аймалин, производное раувольфии, применяемый для купирования тахикардии с широкими комплексами QRS, способен удлинять интервал Q–T и провоцировать желудочковую тахиаритмию. Повышенная чувствительность HERG к антиаритмическим препаратам III класса, противогрибковым или антигистаминным средствам, антибиотикам группы макролидов также ответственна за возникновение аритмий.
Женский пол является дополнительным фактором риска появления желудочковых тахиаритмий. Экспериментально установлена способность женских половых гормонов (эстрогена и прогестерона) моделировать процессы реполяризации in vivo. Удлинение корригированного Q–Tc на фоне инфузии ибутилида выявлено именно в первую фазу менструального цикла. Предполагается, что заместительная терапия прогестинами в период менопаузы может нормализовать реполяризацию разных отделов желудочка.
Особую опасность представляет наличие нескольких факторов риска развития приобретенного синдрома удлиненного интервала Q–T. Одновременное применение антибиотиков, антигистаминных и противогрибковых препаратов (см. табл. 2.6) значительно повышает риск развития опасных для жизни аритмий. В табл. 2.7 представлены предикторы проаритмогенного действия антиаритмических препаратов.
Таблица 2.7
Предикторы аритмогенного действия антиаритмических препаратов (ААП) (возникновение препаратзависимой желудочковой проаритмии)
| ААП IА и III класса | ААП IС класса |
| Удлиненный Q–T (Q–T >460 мс)
Синдром удлиненного интервала Q–T Структурные заболевания сердца, ГКМП Дисфункция ЛЖ Гипокалиемия/гипомагниемия Женский пол Дисфункция почек Синусовая брадикардия:
Быстрое повышение дозы Высокие дозы (соталол, дофетилид) Кумуляция препаратов Добавление препаратов:
Проаритмии в анамнезе Значительное удлинение интервала Q–T после приема (введения) препарата |
Широкий комплекс QRS (>120 мс)
Чрезмерное (больше чем на 150%) увеличение комплекса QRS по сравнению с первоначальным (на момент назначения терапии) Желудочковые тахиаритмии, ассоциированные со структурными заболеваниями сердца Дисфункция ЛЖ Высокая ЧСС:
Быстрое повышение дозы Дополнительные препараты в высоких дозах Препараты, оказывающие отрицательное инотропное действие |
ЛЕЧЕНИЕ БОЛЬНЫХ С СИНДРОМОМ УДЛИНЕННОГО ИНТЕРВАЛА Q–T
Существуют основные направления терапии больных с синдромом удлиненного интервала Q–T:
- предотвращение приступов желудочковой тахиаритмии;
- купирование данных приступов;
- реанимационные мероприятия при возникновении фибрилляции желудочков или асистолии.
Для осуществления такой терапии используют лекарственные средства; хирургические методы; электролечение.
Существуют особенности ведения пациентов с полиморфной желудочковой тахиаритмией в зависимости от продолжительности интервала Q–T (пируэт-тахикардия) (схема 2.1).
Схема 2.1
Особенности ведения пациентов с полиморфной желудочковой тахиаритмией в зависимости от продолжительности интервала Q–T (по Kowey P.R. et al., 1999)
| Полиморфная желудочковая тахиаритмия | |
| Удлиненный Q–T | Нормальный Q–T |
|
|
Общепризнанной считается терапия блокаторами β-адренорецепторов в высоких дозах (у детей до 2 мг/кг/сут). Положительный эффект этих препаратов обусловлен блокадой симпатических влияний на сердце и снижением степени дисперсии реполяризации миокарда желудочков, что предупреждает приступы опасных для жизни аритмий.
Сегодня разрабатывается генспецифическая терапия синдрома удлиненного интервала Q–T. Так, блокаторы β-адренорецепторов наиболее эффективны при 1-м типе синдрома удлиненного интервала Q–T, при 2-м — препараты калия, при 3-м — блокаторы натриевых каналов (мексилетин). Новым лекарственным средством для лечения больных с 1-м и 2-м типом врожденного синдрома удлиненного интервала Q–T является никорандил, который способствует открытию АТФ-чувствительных калиевых каналов кардиомиоцитов. Но, к сожалению, реальных возможностей обследовать больных с помощью методов генетической диагностики для подбора генспецифической терапии нет.
Используют комбинации блокаторов β-адренорецепторов с препаратами магния (сульфат магния), калия и блокаторами натриевых каналов (мексилетин, флекаинид).
При наличии у больного, перенесшего синкопе или состояние клинической смерти, тревожности, склонности к акцентированию внимания на своих ощущениях, иппохондрическим страхам, можно добавить к лечению короткие курсы (не более 1 мес) терапии транквилизаторами (диазепам, феназепам).
При неэффективности медикаментозного лечения прибегают к имплантации таким больным электрокардиостимуляторов (минимальная эффективная частота кардиостимуляции для предотвращения torsade de pointes составляет >70 уд./мин), которые работают в режимах АА1К, VVIR, DDDR, или кардиовертеров-дефибрилляторов в сочетании с приемом блокаторов β-адренорецепторов (табл. 2.8). Показанием для имплантации электрокардиостимулятора является выраженная брадикардия в межприступный период, чаще при 3-м типе врожденного синдрома удлиненного интервала Q–T (при этом генетическом варианте врожденного синдрома удлиненного интервала Q–T с повышением ЧСС интервал Q–T укорачивается и снижается риск развития опасных для жизни аритмий).
Таблица 2.8
Предупреждение ранней коронарной смерти у больных с синдромом удлиненного интервала Q–T
| Способ | Очень важно | Важно | Менее важно |
| Стратификация риска | Остановка сердца
Фибрилляция желудочков Тахикардия по типу torsade de pointes Синкопе JLN LQ–ТЗ-генетический вариант |
Q–T корригированный — 600 мс
Кардиособытия у новорожденных Период после родов АV-блокада Альтернация зубца Т Женский пол |
Семейный анамнез ранней коронарной смерти
Увеличение дисперсии интервала Q–T |
| Первичная профилактика | Избегать средств, удлиняющих интервал Q–T
Избегать физических нагрузок# Блокаторы β-адренорецепторов# |
Денервация левого сердечного симпатического узла
Пейсмейкер |
|
| Вторичная профилактика | Имплантированный кардиовертер-дефибриллятор*
Блокаторы β-адренорецепторов# Избегать средств, удлиняющих интервал Q–T# |
Блокаторы β-адренорецепторов |
#эффективный у пациентов без синкопе или носителей гена без клинических проявлений; *можно рекомендовать больному
У больных с врожденным синдромом удлиненного интервала Q–T при непереносимости или неэффективности блокаторов β-адренорецепторов, отсутствии эффекта от электрокардиостимулятора и невозможности имплантирования кардиовертера-дефибриллятора выполняют левую шейно-грудную симпатическую ганглийэктомию, что устраняет симпатический дисбаланс иннервации сердца. Рекомендованный уровень симпатэктомии: Т1–Т4 и звездчатый ганглий или его нижняя треть. Однако существуют сведения о том, что этот метод при высокой эффективности в ранние сроки после операции приводит к рецидиву заболевания в отдаленный период.
Согласно рекомендациям Ассоциации кардиологов Украины блокаторы β-адренорецепторов являются препаратами выбора для профилактики (первичной и вторичной) ранней коронарной смерти у больных с синдромом удлиненного интервала Q–T.
Неотложная помощь при внезапной остановке кровообращения проводится по общепринятым методикам.
ЛИТЕРАТУРА
- Antzelevitch C., Dumaine R. (2002) Electrical heterogeneity in the heart: physiological, pharmacological and clinical implications. Handbook of electrophysiology: The Heart. Eds. E. Page, H. Fozzard, R.G. Solaro. N.Y.: Oxford University press, р. 654–692.
- Antzelevitch C., Fish J. (2001) Electrical heterogeneity within the ventricular wall. Basic Res Cardiol., 96 (6): 517–527.
- Balser J.R. (1998) The Long QT Syndrom: Basic Cardiac Electrophysiology: What the Fellow and Practicing Clinical Electrophysiologist Should Know I: Molecular and Ionic Basis of Arrhythmias: Pharmacology of Cardiac Ion Channels. G. V. Nacarelly. 19th Annual Scientific Sessions Highlights, Program Chair. NASPE, May 6–9.
- Belhassen B., Glick A., Viskin S. (2004) Efficacy of quinidine in high-risk patients with Brugada syndrome. Circulation, 110 (13): 1731–1737.
- Bonnemeier H., Hartmann F., Wiegand U.K.H. et al. (2000) Course and prognostic implications of QT interval and QT interval variability after primary coronary angioplasty in acute myocardial infarction. JACC, 37 (1): 44–50.
- Chevalier P., Rodriguez C., Bontemps L. et al. (2001) Non-invasive testing of acquired long QT syndrome: Evidence for multiple arrhythmogenic substrates. Cardivasc Res., 50 (2): 386–398.
- Gadaleta F.L., Llois S.C., Sinisi V.A. et al. (2008) Corrected QT interval prolongation: a new predictor of cardiovascular risk in patients with non-ST-elevation acute coronary syndrome. Rev. Esp. Cardiol., 61 (6): 572–578.
- Hisamatsu K., Kusano K.F., Morita H. et al. (2004) Relationships between depolarization abnormality and repolarization abnormality in patients with Brugada syndrome: using body surface signal-averaged electrocardiography and body surface maps. J. Cardiovasc. Electrophysiol., 15 (8): 870–876.
- Hong K., Brugada J., Oliva A. et al. (2004) Value of electrocardiographic parameters and ajmaline test in the diagnosis of Brugada syndrome caused by SCN5A mutations. Circulation, 110 (19): 3023–3027.
- Hu D., Viskin S., Oliva A. (2007) Genetic predisposition and cellular basis for ischemia-induced ST-segment changes and arrhythmias. J. Electrocardiol., 40 (6 Suppl.): S26–29.
- Kanki H., Yang P., Xie H.G. et al. (2002) Polymorphisms in beta-adrenergic receptor genes in the acquired long QT syndrome. J. Cardiovasc. Electrophysiol., 13 (3): 252–256.
- Masaki N., Takase B., Matsui T. (2006) QT peak dispersion, not QT dispersion, is a more useful diagnostic marker for detecting exercise-induced myocardial ischemia. Heart Rhythm., 3 (4): 424–432.
- McNair W.P., Ku L., Taylor M.R et al.; Familial Cardiomyopathy Registry Research Group (2004) SCN5A mutation associated with dilated cardiomyopathy, conduction disorder, and arrhythmia. Circulation, 110 (15): 2163–2167.
- Morita H., Zipes D.P., Fukushima-Kusano K. et al. (2008) Repolarization heterogeneity in the right ventricular outflow tract: correlation with ventricular arrhythmias in Brugada patients and in an in vitro canine Brugada model. Heart Rhythm., 5 (5): 725–733.
- Nishida K., Fujiki A., Mizumaki K. et al. (2004) Canine model of Brugada syndrome using regional epicardial cooling of the right ventricular outflow tract. J. Cardiovasc. Electrophysiol., 15 (8): 936–941.
- Ortega-Carnicer J., Benezet J., Calderon-Jimenez P. et al. (2008) Hypothermia-induced Brugada-like electrocardiogram pattern. J. Electrocardiol. Jun 3.
- Schwartz P.J., Priori S.G., Spazzolini C. et al. (2001) Genotype-phenotype correlation in the long-QT syndrome: gene specific triggers for life-threatening arrhythmias. Circulation., 103: 89–95.
- Sreeram N., Simmers T, Brockmeier K. (2004) The brugada syndrome. Its relevance to paediatric practice. Z. Kardiol., 93 (10): 784–790.
- Tanabe Y., Inagaki M., Kurita T. et al. (2001) Sympathetic stimulation produces a greater increase in both transmural and spatial dispersion of repolarization in L QT1 then L QT2 forms of congential long-QT syndrome. J. Amer. Cool. Cardiol., 37: 911–919.
- Towbin J.A. (2004) Molecular genetic basis of sudden cardiac death. Pediatr Clin North Am., 51 (5): 1229–1255.
- Vitasalo M., Oikarinen A., Swan H. et al. (2006) Effects of beta-blocker therapy on ventricular repolarization documented by 24-th electrocardiography on patients with type 1 long-QT syndrome. Amer. Coll. Cardiology, 48: 747–753.
- Watanabe H., Chinushi M., Hao K. et al. (2004) Postprandial Variations in ST Segment in a Patient with Brugada Syndrome and Partial Gastrectomy. Pacing Clin Electrophysiol., 27 (11): 1560–1562.
- Yamaguchi M., Shimizu M., Ino H. et al. (2003) T wave peak-to-end interval and QT dispersion in acquired long QT syndrome: a new index for arrhythmogenicity. Clin. Sci., 105: 671–676.