В результате нормального развития человек в определенном возрасте достигает максимального показателя костной массы — пиковой костной массы. Сроки достижения пиковой костной массы варьируют, начиная с 17–18 и до 35 лет. Пик костной массы образует плато, сохраняющееся в течение нескольких лет. Размеры и массивность скелета определяются реализованной в течение периода роста генетической программой, гормональным статусом, питанием, механической нагрузкой на скелет. Генетическую программу по строительству костной ткани нельзя эффективно реализовать без достаточного количества энергии, белка, витаминов, минералов, микроэлементов. Дефицит кальция, неполноценная диета препятствуют реализации генетической программы полностью. Достигнутая в процессе роста костная масса имеет резервное значение: в последующем она определяет устойчивость или склонность к переломам костей. Сформировавшаяся кость в течение всей жизни постоянно обновляется. При этом костный обмен могут ускорять самые различные эндогенные и экзогенные факторы. Обусловливая дисбаланс процессов резорбции и формирования кости, они уменьшают костную массу, приводят к остеопорозу. Случаи остеопороза неизвестной этиологии (идиопатического) возможны у юношей и людей молодого возраста (20–44 лет). В возрасте старше 35 лет у женщин и 40 у мужчин костная масса начинает постепенно уменьшаться — развивается возрастзависимый (инволюционный) остеопороз, в основе которого лежат генорегуляторные механизмы (Подрушняк Е.П., 1987; Михайлов Е.Е., Боневоленская Л.И., 1997; Фролькис В.В. и соавт., 1999; 2002). Инволюционные процессы в костной ткани обусловливают то, что у 93–100% людей старческого возраста и у долгожителей диагностируют остеопороз (Подрушняк Е.П., 1987). Потеря костной ткани резко ускоряется после достижения женщинами менопаузального периода — в результате отсутствия остеотропного влияния эстрогенов. Наибольшая потеря костной массы происходит в первые 5 лет после прекращения продукции эстрогенов. У мужчин подобный процесс не наблюдается, поскольку продукция андрогенов у них сохраняется до глубокой старости. Оба типа инволюционного остеопороза (постменопаузальный и сенильный) составляют 80% всех случаев остеопороза (Поворознюк В.В., Григорьева Н.В., 2002).
Однако, кроме этой основной, генетически обусловленной причины, имеется большое количество других факторов, обусловливающих развитие остеопении. Они действуют в течение всей жизни человека: как до включения инволюционных механизмов, так и на их фоне, суммируя эффект, ускоряя деминерализацию кости. К этим факторам относятся:
- неполноценное питание;
- различные патологические процессы в организме:
- нарушение продукции кальцийрегулирующих и системных гормонов (снижение секреции, избыточная продукция);
- воспаление, аутоиммунный процесс;
- инфекция;
- развитие неспецифического адаптационного синдрома;
- усиление свободнорадикальных процессов;
- нарушение иммунитета (функции макрофагов, лимфоцитов);
- нарушение взаимодействия между клетками костного мозга и костной ткани;
- гиперплазия костного мозга;
- легочно-сердечная недостаточность;
- гипоксия, хронический ацидоз (респираторный и метаболический);
- неопластический процесс;
- интоксикация, анорексия;
- атрофические процессы в пищеварительной системе;
- гиперпродукция гастрина;
- энзимопатия;
- холестаз, нарушение синтеза и выделения желчи (желчных кислот);
- мальдигестия, мальабсорбция;
- дисбактериоз;
- тубулопатия, расстройство функции проксимальных почечных канальцев;
- поражение нефронов, развитие ХПН;
- нарушение гомеостаза минералов, метаболизма витамина D;
- системные заболевания скелета, генетические дефекты развития соединительной ткани, синтеза коллагена, обмена калия, холестерина, мукополисахаридов, аминокислот, болезни накопления (в том числе лизосомные);
- нарушение иннервации (парез, паралич), иммобилизация;
- гиперфункция регионарной симпатической нервной системы, нейропатия;
- хронический стресс;
- оперативные вмешательства, иммуносупрессивная терапия после пересадки органов;
- беременность, кормление грудью;
- прием некоторых лекарственных средств, поступление в организм токсических веществ, пестицидов;
- пребывание в длительном плавании, воздействие вибрации, ударного ускорения;
- физические упражнения высокой интенсивности;
- хроническое перегревание организма;
- резкое уменьшение массы тела;
- экологические факторы (радиация, промышленные факторы, избыточное поступление тяжелых металлов, микроэлементов);
- вредные привычки (курение, злоупотребление алкоголем, кофе).
Негативное влияние ряда указанных факторов на метаболизм костной ткани и процессы ремоделирования реализуется при многочисленных заболеваниях. Так, остеопения развивается при:
- эндокринной патологии: гиперпаратиреоз, болезнь Реклингхаузена, псевдогипопаратиреоз, гипопаратиреоз врожденный (иммунологическая недостаточность, аплазия вилочковой железы, синдром Ди Джордже) и приобретенный (аутоиммунный процесс, оперативное вмешательство, гемохроматоз), тиреотоксикоз, гипотиреоз (врожденный, послеоперационный, аутоиммунный тиреоидит), гипогонадизм (агенезия яичек, нелеченный крипторхизм, синдром Кляйнфелтера, дефекты 5α-редуктазы, синдром Шерешевского — Тернера, Нунана, состояние после химио- и лучевой терапии, удаления гонад), гиперпролактинемический синдром, болезнь и синдром Иценко — Кушинга, акромегалия, гипопитуитаризм, дефицит СТГ, сахарный диабет I типа, болезнь Аддисона, феохромоцитома;
- ревматических заболеваниях: ревматоидный артрит, болезнь Стилла, СКВ, ССД, дерматомиозит, болезнь Шегрена, реактивные артропатии, синдром Рейтера, полиостеоартроз, анкилозирующий спондилоартрит (ББ), ревматическая полимиалгия, синдром Шейермана;
- заболеваниях органов пищеварения: атрофический гастрит, пептическая язва, резекция желудка по Бильрот II, гастрэктомия, хронический панкреатит с внешнесекреторной недостаточностью, обструктивный панкреатит, муковисцидоз и рак поджелудочной железы, хронический энтерит (в том числе радиационный), спру, дивертикулез тощей кишки, амилоидоз кишечника, болезнь Крона, целиакия, недостаточность лактазы, наложение обходных анастомозов, резекция тонкого кишечника (синдром короткой кишки), неспецифический язвенный колит, хронический активный гепатит, вирусный и алкогольный цирроз печени, первичный и вторичный билиарный цирроз печени, дисбактериоз, хронический холецистит, желчнокаменная болезнь, пересадка печени;
- заболеваниях легких: бронхиальная астма, хронический обструктивный бронхит, эмфизема, фиброз легких, хронический диффузный интерстициальный фиброз, альвеолярный протеиноз, легочный саркоидоз, первичный легочный гемосидероз, бронхиолярный клеточный рак, пострадиационный фиброз, бериллиоз, асбестоз, хроническое легочное сердце, нагноительные заболевания легких, туберкулез;
- заболеваниях сердечно-сосудистой системы: атеросклероз, ишемическая болезнь сердца, артериальная гипертензия, врожденные и приобретенные пороки сердца, миокардиты, кардиомиопатии на стадии развития хронической сердечной недостаточности, пересадка сердца;
- болезнях почек: хронический гломерулонефрит, пиелонефрит, диабетический гломерулосклероз, поликистоз на стадии ХПН, пересадка почки, почечный канальцевый ацидоз, синдром Фанкони, семейная гипофосфатемия, синдром Лоу, болезнь Гирке, юношеское поражение нефронов, гипофосфатазия, витамин D-резистентный и витамин D-зависимый рахит;
- болезнях крови: апластическая, пернициозная, гемолитические анемии (талассемия, серповидно-клеточная анемия), миеломная болезнь, болезнь Вальденстрема, острый лейкоз, хронический лейкоз (миелолейкоз, лимфолейкоз, мастоцитоз), лимфома, лимфогрануломатоз, лимфосаркома, гемофилия;
- неопластическом процессе: опухоли головы, шеи, пищевода; карцинома почек, мочевого пузыря, яичников; метастазы опухолей молочной и предстательной желез, легких, почек, поджелудочной железы; неэндокринные опухоли, сопровождающиеся аберрантной секрецией гормонов (плоскоклеточная и мелкоклеточная карцинома бронха, карциноидные опухоли, аденокарцинома почек);
- врожденных заболеваниях: несовершенный остеогенез, синдромы Марфана, Элерса — Данлоса, гомоцистинурия, лизинурия, мукополисахаридоз, гемохроматоз, болезнь Вильсона, болезнь Гоше, синдром Тиммана — Флейшера, наследственные системные заболевания скелета (диастрофическая и спондилоэпифизарная дисплазия), первичная гипогаммаглобулинемия взрослых (болезнь Брутона) и др.;
- других заболеваниях, состояниях: повреждение спинного мозга, парезы, паралич, паркинсонизм, детский паралич, длительная иммобилизация, нервная анорексия, рефлекторная симпатическая дистрофия (альгодистрофия), нейропатия, нарушения питания, алкоголизм;
- длительном приеме медикаментов: ГКС, тиреоидные гормоны, агонисты гонадотропин-рилизинг гормона, иммунодепрессанты, седативные, фенотиазины, барбитураты, противосудорожные, антикоагулянты, препараты лития, тетрациклин, диуретики, антациды, содержащие алюминий.
Наличие такого количества факторов развития остеопении свидетельствует о необходимости подхода к этой проблеме как системному биологическому явлению, а также о необходимости создания классификации вторичного остеопороза, которая базировалась бы на учете патогенетических механизмов его развития. Учитывая большое количество заболеваний, сопровождающихся развитием остеопении, важным направлением профилактики остеопороза является предотвращение и лечение этих заболеваний. Метаболизм костной ткани следует рассматривать в связи с другими (генетическими, биохимическими, физиологическими, патофизиологическими) процессами, происходящими в организме, и факторами окружающей среды. Состояние костного метаболизма, процессов ремоделирования определяется влиянием нейрогуморальных, локальных, пищевых факторов: нарушения нейрогуморальной и локальной регуляции, обмена веществ в организме сопровождаются структурно-функциональными изменениями в костях. Снижение синтетических процессов остеобластами, остеоцитами, усиление активности остеокластов находит отражение в разрежении кости, снижении костной массы.
Внимание исследователей сосредоточено преимущественно на постменопаузальном остеопорозе, который развивается у миллионов женщин. Среди больных с постменопаузальным остеопорозом большое количество пациенток, у которых остеопороз начался в предменопаузальный период (потеря костной массы у женщин начинается с 35–40 лет и составляет 0,51% в год), а снижение продукции половых гормонов ускорило его проявление. Начало остеопороза может быть обусловлено воспалительным процессом, а в дальнейшем усугубиться менопаузой. Указанные выше заболевания могут развиться как в молодом возрасте, так и в постменопаузальный период. У многих больных сочетаются несколько этиологических причин остеопороза. Так, у людей старшего и пожилого возраста остеопороз может быть обусловлен несколькими факторами: дефицитом эстрогенов (андрогенов), инволюционными процессами, воспалением, тканевой гипоксией, ацидозом, неполноценным питанием. При хронических воспалительных заболеваниях легких, кроме действия гипоксии, ацидоза, костную резорбцию обусловливает хроническое (рецидивирующее) воспаление легких, сопровождающееся усиленной выработкой провоспалительных цитокинов, ПГЕ1, ПГЕ2. При заболеваниях органов пищеварения, кроме синдрома мальабсорбции, развитию остеопороза способствует хронический воспалительный процесс (энтерит, болезнь Крона, неспецифический язвенный колит, дисбактериоз). Для обеспечения синтетических процессов в костной ткани, осуществляемых остеобластами (новообразования кости в процессе ремоделирования), необходимо постоянное поступление в организм (в соответствии с суточными потребностями) белка (аминокислот), липидов (в том числе полиненасыщенных жирных кислот), углеводов, витаминов, минералов, микроэлементов. При их дефиците в рационе костеобразование нарушается, отмечается недостаточный биосинтез органических веществ в матриксе кости. О важной роли аминокислот, мукополисахаридов, липидов, калия для метаболизма кости свидетельствует развитие остеопороза при врожденных нарушениях их обмена. При недостаточном поступлении с пищей кальций и микроэлементы (20% микроэлементов, имеющихся в организме, находятся в костной ткани) «вымываются» из костей, усиливая имеющийся остеопороз или формируя его первоначально. К развитию остеопороза приводит дефицит в рационе магния и таких микроэлементов, как бор, медь, цинк.
Способность остеобластов к синтезу снижается при прекращении регулирующего влияния гормонов (эстрогенов, андрогенов, СТГ, инсулина), назначении различных медикаментозных средств. Различные заболевания (они сопровождаются развитием общего неспецифического адаптационного синдрома) оказывают влияние на функцию клеток костного матрикса. Медиаторами в этом процессе являются катехоламины, ГК, цитокины, ПГ. Острые заболевания и состояния (стресс, грипп, острые респираторные заболевания, ангина, пневмония, операция, травма и др.), безусловно, оказывают влияние на функцию клеток костной ткани, сопровождающееся ультраструктурными изменениями в костной ткани, но эти кратковременные воздействия значительных последствий для состояния костной ткани не имеют и обычно не регистрируются. (Влияние некоторых факторов на процессы синтеза и распада в костной ткани представлено на схемах 5.1 и 5.2).
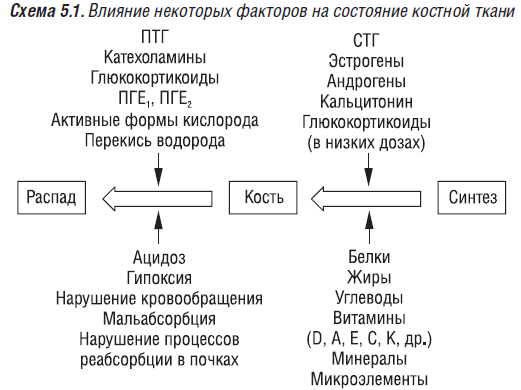
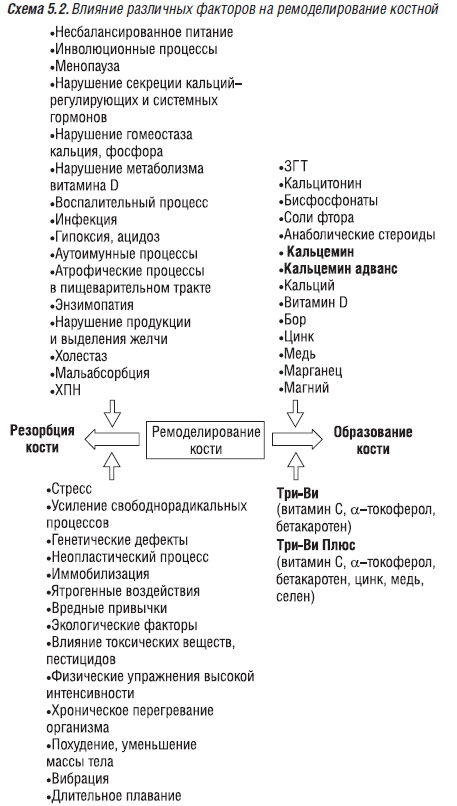
Хронический психоэмоциональный и психосоциальный стресс (схема 5.3), заболевания, сопровождающиеся нарушениями минерального обмена, регулирующих функций гормонов (СТГ, тиреоидных, эстрогенов, андрогенов, инсулина), воспалительным процессом в организме (заболевания легких, органов пищеварения, суставов, костей), аутоиммунным (ревматоидный артрит, системные заболевания соединительной ткани, болезни печени, желудка), гипоксией, ацидозом (заболевания легких, сердечно-сосудистой системы) на первых этапах обусловливают развитие изменений костной ткани на ультраструктурном уровне. Однако в дальнейшем эти изменения накапливаются и на определенном этапе проявляются макроструктурными нарушениями, которые регистрируются инструментальными методами исследования (известно, что эти методы, особенно рентгенологический, обнаруживают поздние грубые изменения в костях).
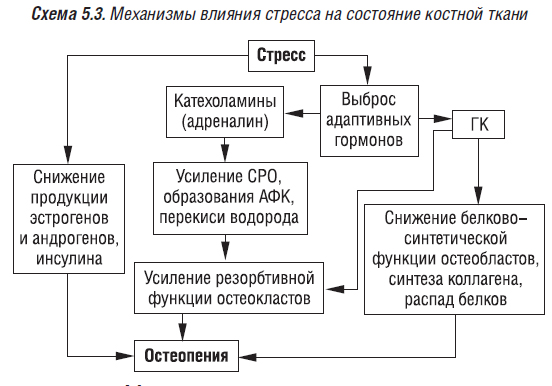
Изменение метаболизма остеобластов, остеоцитов под влиянием регулирующих импульсов приводит к количественным и качественным изменениям компонентов костного матрикса (органического и минерального), изменениям МПКТ, эластических и прочностных характеристик кости.
Независимо от механизмов развития остеопении (остеопороза), важнейшим профилактическим и лечебным средством является кальций, его препараты. Дефицит кальция в пище, нарушение всасывания, усиленное его выведение является одним из факторов развития остеопороза. При недостатке кальция в период роста образуются кости с тонким кортикальным слоем, меньшим числом тонких трабекул. Усиливается эндостально-трабекулярная резорбция, снижается баланс между костеобразованием и резорбцией. При дефиците кальция невозможна реализация генетической программы по строительству костной ткани. После остановки линейного роста продолжается накопление кальция, консолидация костной ткани. Прием препаратов кальция в сочетании с витамином D увеличивает продолжительность жизни населения, повышает ее качество. По мнению R.P. Heanеy и V. Matkovic (1996; 2000), потребность в кальции значительно выше, чем предлагают современные диеты, а усвоение кальция недостаточно в любом возрасте. Взрослый человек, болеющий остеопорозом, должен потреблять ежедневно не менее 1500 мг элементарного кальция. Потребление кальция населением Украины не соответствует рекомендуемым величинам и составляет около 600 мг/сут, то есть 42% рекомендуемых норм (Поворознюк В.В., 1998). Дополнительное применение препаратов кальция необходимо при всех схемах лечения остеопороза в связи с тем, что антирезорбтивные препараты обусловливают гипокальциемический эффект. Препараты кальция повышают эффективность антирезорбентов в комплексной терапии остеопороза: у пациентов, принимающих кальцитонин без дополнительного применения кальция, наблюдается отрицательная динамика показателя МПКТ (Nievis J.W. et al., 1998). Назначение кальция в виде препаратов необходимо всем женщинам независимо от приема антиостеопоротических лекарственных средств. Соли кальция замедляют потерю костной массы, снижают частоту переломов, стабилизируют МПКТ в постменопаузальный период. Необходимым является сочетание кальция с витамином D3, оказывающим регулирующее влияние на гомеостаз кальция: лечение препаратами кальция сопровождается снижением риска переломов на 10%, препаратами кальция с витамином D3 — на 30% (Nievis J.W. et al., 1998). Прием кальция и витамина D предотвращает снижение МПКТ при лечении ГК, корригирует вторичный гиперпаратиреоз у лиц пожилого возраста, снижает у них частоту переломов костей.
На усвояемость и обмен кальция в организме большое влияние, кроме витамина D, оказывают витамины А, Е, С, полиненасыщенные жирные кислоты. Остеопороз, независимо от этиологических факторов его развития, сопровождается интенсификацией СРО. Имеется связь между свободнорадикальным метаболизмом, продуктами окисления полиненасыщенных жирных кислот — ПГ и гомеостазом кальция. АФК повышают резорбирующую активность остеокластов, продукцию ими гидролитических ферментов. АФК повреждают соединительную ткань (органический матрикс) в составе хряща, кости. При усилении перекисного окисления липидов отмечается дезорганизация транспортных механизмов переноса Са2+, нарушение кальцификации матрикса, тормозится биосинтез белков, нуклеиновых кислот, повреждаются лизосомы с выходом гидролитических ферментов, происходит накопление молочной кислоты, оксикислот, кетокислот, развитие ацидоза, усиливающего деминерализацию кости. Эти изменения при остеопорозе требуют применения таких важнейших биоантиоксидантов, как витамин С, α-токоферол, β-каротин в виде антиоксидантных комплексов. Эти витамины играют незаменимую роль в метаболизме костной ткани. Дефицит витамина С сопровождается нарушением синтеза коллагена, окостенения, развитием остеопороза. Витамин А необходим для роста костей, синтеза костного матрикса. Витамин Е повышает синтез активных метаболитов витамина D в почках, усиливает всасывание кальция. Питание населения Украины неполноценно, не сбалансировано по многим компонентам, в том числе по антиоксидантным витаминам, микроэлементам. Такое дефектное питание негативно сказывается на состоянии костного метаболизма и требует сочетанного применения комбинации солей кальция с витамином D и микроэлементами, антиоксидантных комплексов. Преимуществом такого лечения является то, что эти комплексы не просто повышают минерализацию (кальцификацию) костной ткани: содержащиеся в них бор, цинк, медь, марганец, магний, витамин С, α-токоферол, бетакаротен оптимизируют структуру органического матрикса. Применение этих комплексов повышает эффективность ЗГТ, использования таких медикаментозных средств, как кальцитонин, бисфосфонаты, соли фтора, анаболические стероиды, др. Считается, что эффективность лечения остеопороза не может оцениваться только по показателю МПКТ, поскольку риск переломов зависит и от других факторов — скорости ремоделирования, изменений микроархитектоники костной ткани. Дефицит эстрогенов может обусловить развитие болезни Альгеймера. Нейротоксический эффект в-амилоида при этом заболевании может быть опосредован свободными радикалами, поэтому в постменопаузальный период, кроме эстрогенов (оказывающих антиоксидантный эффект), больные нуждаются в применении антиоксидантных комплексов.
Из трех групп препаратов кальция, использующихся для профилактики и лечения остеопороза (простых солей кальция, комбинации солей кальция с витамином D, комбинации солей кальция с витамином D и микроэлементами), преимущество имеет последняя группа, так как она оказывает наиболее выраженное остеопротекторное действие. Представителями этой группы являются Кальцемин, Кальцемин адванс (Sagmel Inc., США). Входящие в состав препаратов цитрат и карбонат кальция относятся к соединениям с наивысшим содержанием элементарного кальция. Благодаря составным компонентам препараты стимулируют синтез коллагена, эластина, гликозамингликанов, входящих в состав костной и хрящевой ткани, повышают темпы накопления кальция в костях. Результаты проведенных исследований (Поворознюк В.В., Григорьева Н.В., 2000; 2001; 2002; Мартынюк Л.П., 2002; Сидельников П.В., 2002; Сытый В.П. и соавт., 2002; Толстопятов Б.А., Паливец А.Ю., 2002; Никула Т.Д. и соавт., 2003; Якименко О.О. та співавт., 2003) свидетельствуют о высокой клинической эффективности вышеназванных комплексных препаратов:
- Кальцемин способствует улучшению структурно-функционального состояния костной ткани при постменопаузальном остепорозе: повышение индекса прочности отмечается у женщин, принимавших Кальцемин в течение 6 мес и более. Препарат восстанавливает прочность костной ткани у экспериментальных животных, подвергнутых двусторонней овариоэктомии: она восстанавливается до уровня данного показателя у неоперированных животных.
- Прием Кальцемина по 1 капсуле 2 раза в сутки в течение 1 года сопровождается снижением уровня интенсивности болевого синдрома у 71% больных остеопорозом уже через 4 мес приема препарата. Улучшение состояния здоровья через 1 год приема препарата отмечается у 85,7% пациентов: у них отсутствует потеря костной массы, не возникают новые остеопоротические переломы позвонков, улучшается качество и МПКТ.
- Монотерапия Кальцемином в стандартной дозе с успехом используется в профилактике и лечении пациентов с вертебральным остеопорозом и его осложнениями в виде остеопоротических деформаций позвонков.
- Эффективность противоостеопоротической терапии повышается при сочетании Кальцемина со средствами ЗГТ и Кальцитонином.
- Кальцемин является эффективным средством профилактики остеопенического синдрома у детей и беременных.
- Препарат снижает выраженность болевого синдрома в области позвоночника, повышает МПКТ. В связи с положительным влиянием на формирование органического и минерального матрикса кости Кальцемин следует использовать при сколиотических деформациях позвоночника.
- Включение Кальцемина в комплексную терапию больных остеоартрозом повышает эффективность терапии у пациентов различного возраста, с разной рентгенологической стадией и степенью функциональной недостаточности суставов за счет действия на суставной и болевой компоненты симптоматики.
- Применение Кальцемина у больных с ренальными остеодистрофиями сопровождается снижением уровня болевого синдрома через 9 мес у 87,5% больных, повышением МПКТ на 1,16%. Использование препарата позволяет отказаться от обезболивающих препаратов. Наблюдающееся повышение содержания кальция в крови предотвращает развитие вторичного гиперпаратиреоза.
- Эффективным и безопасным является использование Кальцемина в комплексном лечении больных с остеопатиями на различных стадиях ХПН. Отсутствие побочных эффектов, возможность комбинировать с другими средствами позволяет индивидуализировать лечение, улучшить кальциевый метаболизм, предупредить развитие гиперпаратиреоза, нормализовать тонус вегетативной нервной системы, улучшить качество жизни больных, достигнуть желаемого терапевтического эффекта.
- Изучение глобальной эффективности в процессе лечения Кальцемином (по шкале CCI) пациентов с хроническими обструктивными заболеваниями легких (принимавших ГК) и у лиц с постменопаузальным и сенильным остеопорозом подтверждает наличие положительной динамики у 79% больных уже на 45-е сутки, более значимые результаты отмечаются на 90-й день (значительное улучшение — у 49%, минимальное — у 44%). Эти данные расцениваются как высокий терапевтический эффект (учитывая медленное течение метаболизма и восстановления костной ткани). У этих больных Кальцемин также оказывает выраженный обезболивающий эффект.
- Применение Кальцемина в комплексной терапии пациентов с генерализованным пародонтитом способствует повышению эффективности лечения, стабилизации дистрофических процессов в альвеолярной кости и тканях пародонта, увеличению периода ремиссии до 16–18 мес. Включение его в курс как консервативного, так и хирургического лечения способствует снижению частоты обострений в 2–3 раза. Особенно эффективно применение Кальцемина при планировании хирургических методов лечения. У больных, принимающих Кальцемин, функциональное состояние периодонтальных сосудов в 2,4 раза лучше по сравнению с теми, кто не принимал препарат. Через 1 год после лечения Кальцемином состояние периферического кровообращения оценивается как компенсированное.
Кальцемин необходим:
- в период активного роста детей и подростков для формирования скелета;
- для профилактики и лечения таких заболеваний, как остеохондроз, остеоартроз, первичный и вторичный остеопороз;
- для лечения травм опорно-двигательного аппарата;
- для коррекции нарушений кальциевого обмена у людей пожилого возраста (особенно у женщин в постменопаузальный период);
- для устранения дефицита и улучшения усвоения кальция в период беременности;
- для профилактики и лечения структурно-функциональных нарушений костной ткани у населения, проживающего в экологически неблагоприятных регионах;
- как базисное средство при профилактике и лечении системного остеопороза антирезорбентами (ЗГТ, кальцитонин, бисфосфонаты);
- для предотвращения резорбции костной ткани при опухолевом процессе, репарации костной ткани на фоне или после проведенного лечения, профилактики остеопороза на фоне терапии КС;
- для коррекции нарушений кальциевого обмена при химиолучевом лечении опухолей костей пациентов онкологических стационаров, областных, районных, участковых больниц;
- для включения в комплекс специальных лечебных мероприятий (лучевой и химиотерапии, хирургических вмешательств, гормонотерапии) у пациентов с миеломной болезнью, костномозговыми опухолями, метастазами в кости;
- как составной элемент комплексной терапии у больных с поражениями опорно-двигательного аппарата.
Показания к применению Кальцемина и Кальцемина адванс:
Профилактика и комплексное лечение пациентов с остеопорозом:
- у женщин в перименопаузальный, менопаузальный и постменопаузальный период;
- у женщин, которые перенесли овариоэктомию;
- при гипоплазии яичников и других эстрогендефицитных состояниях;
- у людей пожилого возраста для профилактики остеопоротических переломов;
- при длительном приеме КС, иммунодепрессантов, противосудорожных средств, гепарина, тироксина;
- при хронических заболеваниях почек, пищеварительного тракта, эндокринной системы;
- при длительной иммобилизации;
- при наследственной склонности к остеопорозу (переломы у старших по возрасту кровных родственников).
Профилактика и лечение пациентов с другими заболеваниями опорно-двигательного аппарата:
- для улучшения консолидации травматических переломов;
- при остеохондрозе и патологии суставов;
- у профессиональных спортсменов.
Восполнение дефицита кальция, витамина D3 и микроэлементов для профилактики остеопенических состояний:
- у детей в период интенсивного роста;
- у беременных и кормящих грудью;
- при дефиците кальция, витамина D3, микроэлементов в рационе.
В комплексном лечении пациентов с заболеванием зубов и парадонта:
- при локальном и генерализованном парадонтите;
- в комплексе медикаментозного обеспечения ортодонтических процедур и челюстно-лицевых операций.
В комплексе лечения пациентов с радиационными поражениями (для защиты стромы костей от накопления радиоактивного стронция).
В комплексе лечения пациентов с нарушениями свертывания крови.
Как сопутствующая терапия в лечении пациентов антирезорбентами и средствами ЗГТ.
Назначение Кальцемина адванс:
курсами по 12 мес:
- взрослым и детям в возрасте старше 12 лет — 1–2 таблетки 1–2 раза в сутки;
- детям в возрасте 6–12 лет — 1–2 таблетки в сутки.
Способ применения Кальцемина: взрослым и детям в возрасте старше 12 лет — по 1 таблетке 2 раза в сутки. Детям в возрасте 5–12 лет — по 1 таблетке 1 раз в сутки.
Противопоказанием к приему Кальцемина, Кальцемина адванс являются повышенная чувствительность к ингредиентам препарата, гиперкальциемия, гиперкальциурия.
Таким образом, результаты проведенных исследований позволяют рекомендовать Кальцемин и Кальцемин адванс как приоритетное средство базисной терапии и профилактики системного остеопороза.