Лимфатические узлы (ЛУ) — только часть общей лимфатической системы человека. Лимфатическая система человека состоит из чрезвычайно разветвленной высокодифференцированной ткани, общая масса которой составляет около 1% общей массы тела. Она состоит из ЛУ, распределенных по всему телу, лимфатических сосудов (от мелких до крупного Ductus thoracicus), миндалин, лимфатической ткани слизистой оболочки дыхательного и пищеварительного трактов, тимуса, белой пульпы селезенки. К лимфатической системе относят также часть костного мозга и лимфоциты в периферической крови и в тканях. То есть даже из беглого обзора видно, что лимфатическая система не является абсолютно единой.
Филогенетически лимфатическая система возникает на достаточно поздних этапах эволюции. Первые лимфатические сосуды выявляют только у амфибий. Скопления лимфоцитов отмечают у птиц, но настоящие лимфатические узлы у них — единичные.
В онтогенезе тимус начинает развиваться на 8-й неделе беременности. Первые ЛУ появляются на 3-м месяце. Первичные лимфатические узелки образуются из спонгиозной ткани, развившейся из лимфатического сосуда. Слияние первичных узелков ведет к образованию собственно ЛУ. К моменту рождения человека лимфатическая система еще очень незрелая. Это проявляется и в незрелости иммунологических реакций. Развитие лимфатических тканей завершается только к 12–15 годам. Диаметр зрелых ЛУ составляет от 2 до 25 мм. Но размеры ЛУ очень сильно зависят от возраста и функционального состояния.
Важнейший лимфоидный орган иммунитета — глоточное лимфоидное кольцо Вальдейера — Пирогова, прежде всего — так называемые миндалины (Tonsilla palatina). Наряду с этим парным органом кольцо построено из непарных глоточной миндалины и миндалины на корне язычка и лимфоидных тяжиков, расположенных латерально на задней стенке глотки. Онтогенетически небные миндалины возникают раньше ЛУ и селезенки. В жизни ничего не бывает случайным. Случайными мы называем вещи, смысл и происхождение которых не знаем. Такое раннее формирование лимфоидной ткани в глотке объясняется, видимо, тем, что ребенок начинает контактировать с антигенами именно per os, заглатывая околоплодные воды. Первичные лимфатические фолликулы появляются в возрасте 16 нед. Вторичные фолликулы появляются после контакта с антигенами. У гнотобиологических животных они никогда не формируются.
Вся структура миндалин предназначена для контакта с антигеном. Поскольку антиген не поступает в миндалину, как в ЛУ, через приносящий сосуд, контакт достигается через поверхность. Миндалины покрыты многослойным неороговевающим эпителием, который легко фиксирует на себе антигены. Площадь контакта значительно увеличивается за счет внедрения эпителия в ткань миндалины с образованием крипт. В каждой миндалине имеется 15–20 кратеров-крипт. В результате площадь активной поверхности миндалины составляет 300 см2. В дополнение к этому в криптах эпителий лежит очень рыхло и базальная мембрана в этой области не сплошная, а представлена отдельными участками. Все это предназначено для облегчения захватывания и контакта с антигенами.
Наибольшей относительной и абсолютной массы миндалины достигают у детей в возрасте 5–11 лет. В этом возрасте лимфоидной ткани у ребенка в 2 раза больше, чем у взрослого. Доброкачественное увеличение миндалин, закономерная реакция их лимфоидной ткани на антигенный шквал в позднем дошкольном и раннем школьном возрасте, когда нарастает активность ребенка, лавинообразно увеличивается число разнообразных контактов, нередко расценивается как хронический тонзиллит. А уж этот диагноз едва ли не автоматически обусловливает тонзилэктомию.
Все вышеприведенные сведения призваны подтвердить сложность строения, этапность созревания и многообразие функций лимфатической системы, ее реакцию на самые разнообразные раздражители. Поэтому врач достаточно часто выявляет у своих пациентов увеличенные ЛУ, ему приходится в сжатые сроки отвечать на вопросы «почему?» и «что делать?».
Традиционно при увеличении ЛУ, не учитывая другие составляющие этого синдрома (анамнез, общую клиническую картину, местную симптоматику), думают об онкогематологическом заболевании. Вследствие этого такие пациенты составляют до 40–60% всех первичных больных, посещающих онкогематолога, что представляется не оправданным. Частота впервые выявленных случаев онкогематологических заболеваний в нашей стране относительно невелика. Отсюда понятно, почему большинство пациентов с увеличенными ЛУ после посещения гематолога возвращается к терапевтам и педиатрам с диагнозом «лимфаденит» (ЛА). То есть причиной увеличения ЛУ в большинстве случаев являются процессы, не связанные с гемобластозами: инфекционные, общетерапевтические, иммунные и другие состояния.
В то же время нельзя настаивать на инфекционном генезе увеличения ЛУ, если двухнедельный курс антибиотикотерапии не обусловил существенного улучшения клинико-лабораторных показателей и результатов инструментального обследования.
Увеличение ЛУ может быть результатом ЛА и лимфаденопатии (ЛАП).
ЛА — воспаление ЛУ, возникающее как осложнение после различных гнойно-воспалительных заболеваний и специфических инфекций (туберкулез, актиномикоз, чума и др.). ЛА, как правило, является вторичным процессом.
ЛАП — системное увеличение ЛУ, не связанное с воспалением (воздействие некоторых медикаментов, пролиферация, метастазирование и т. д.).
Методы исследования ЛУ должны быть максимально стандартизованы.
В клинической практике оценивают жалобы (местная болезненность, местное или общее повышение температуры, общесоматические жалобы), анамнез (эпиданамнез, давность появления, локализация увеличеннных ЛУ в одной или нескольких группах, одновременное их увеличение или постепенное, скорость манифестации болезни).
Особое значение имеет осмотр больного. Наряду с тщательным общетерапевтическим осмотром по системам необходимо обратить внимание на количество измененных ЛУ и локализацию их по группам. ЛУ следует оценивать только объективно (в мм или см). Принятое в нашей стране и широко рекомендуемое в отечественной литературе сравнение ЛУ с зерном, горохом, вишней, лесным или грецким орехом нерационально, дает несопоставимые результаты и должно быть изжито. Необходимо тщательно фиксировать соотношение увеличенных ЛУ между собой. Например, расположение ЛУ по типу «солнечной системы» (один большой ЛУ в центре и по периферии от него ЛУ меньшего диаметра) типично для туберкулеза лимфатической системы.
Осмотр и пальпация позволяют выявить увеличение поверхностных ЛУ: затылочных, шейных, впереди- и заушных, подчелюстных, подбородочных, над- и подключичных, подмышечных, локтевых, паховых, подколенных. Выявление увеличения ЛУ той или иной группы может быть полезным для правильного установления диагноза некоторых заболеваний. Так, увеличение затылочных ЛУ типично для краснухи, заднешейных — для инфекционного мононуклеоза, подчелюстных — для ангины.
Размер ЛУ в каждой из групп в определенной мере индивидуален. Так, подмышечный ЛУ диаметром 1–2 см при отсутствии других проявлений не вызывает тревоги, а такой же размер надключичного узла заставляет думать о метастазе. ЛУ может быть подвижным или спаянным с окружающими тканями. Консистенция характеризуется как эластичная, мягкая, с флюктуацией, средней плотности и плотная. При остром воспалении ЛУ размягчается, часто становится болезненным при пальпации. Болезненные ЛУ редко бывают злокачественными. Метастазы в ЛУ делают их твердыми.
Для более полной характеристики ЛУ, особенно в недоступных для пальпации областях, применяется рентгенография грудной клетки, ультразвуковое исследование брюшной полости, КТ и ЯМР. Они позволяют точно определить размеры ЛУ, изменения групп ЛУ, недоступных осмотру и пальпации, характеристики капсулы, спаянность, топографические особенности, внутреннюю структуру; исключить состояния, симулирующие увеличение ЛУ (опухоли, не исходящие из ЛУ, гематомы, аномалии почек и т. п.). Крайне важно получение информации о состоянии печени и селезенки. На первом месте по доступности и быстроте получения информации стоит эхоГ. Л У диаметром <1,5 см по плотности приближаются к жировой ткани, визуализируются редко, ограничить их опухолевое поражение от иных причин увеличения только по данным эхоГ практически невозможно. Такие ЛУ выявляют прежде всего при инфекционных процессах, реактивных поражениях, в состоянии полной ремиссии гемобластозов. ЛУ диаметром 1,5–2 см хорошо визуализируются в случае, если они проецируются на эхонегативные структуры или изменяют обычные топографо-анатомические соотношения. Весь спектр эхоГ-изменений ЛУ может быть сведен к трем основным группам:
- Увеличение отдельных ЛУ оценивают как небольшое, если они не теряют своей обычной структуры, сохраняют капсулу, четкость и ровность контуров, не изменяют топику органа. Такой тип характерен для инфекционных поражений, особенно туберкулеза, вирусного гепатита, коллагеноза, иммунодефицита, гемобластоза у больных низкой группы риска.
- Дальнейший рост ЛУ приводит к появлению сливающихся между собой масс, оттесняющих сосуды. Отмечают при гнойном расплавлении группы ЛУ, при гемобластозе, метастазирующих опухолях.
- Сдавливание или оттеснение внутренних органов. При этом может возникнуть гидронефроз за счет сдавливания мочеточника, значительное смещение матки, мочевого пузыря. Типично для крайне неблагоприятных вариантов миелолейкозов, лимфом Ходжкина и неходжкинских лимфом.
ЭхоГ заключения могут быть подтверждены данными КТ или ЯМР. Эти методы дополнительно позволяют уточнить структуру ЛУ, их топографические соотношения, выявить другие группы ЛУ. Если поверхностные ЛУ есть смысл оценивать только при помощи эхоГ, а мезентериальные и забрюшинные ЛУ практически одинаково хорошо выявляются методами эхоГ и КТ, то внутригрудные ЛУ выявляют почти исключительно рентгенологически (рис. 5.1).
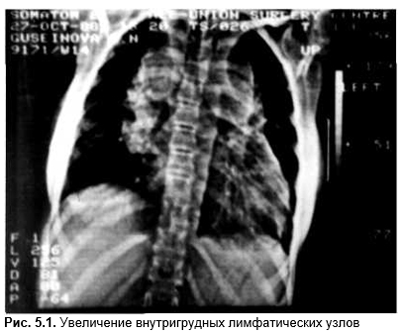
Лимфография во многих случаях уступает эхоГ и КТ. Сцинтиграфия с Ga67 позволяет оценивать воспалительно измененные ЛУ, но не применима для изучения ЛУ брюшной полости, поскольку толстая кишка и печень активно поглощают изотоп. Окончательное заключение возможно после гистологического изучения. Наиболее достоверным методом является биопсия ЛУ, которая имеет свои особенности. Показаниями для оперативного вмешательства, гистологического изучения и выбора ЛУ для проведения биопсии определяются только клинически. При увеличении ЛУ нескольких групп желательно не удалять паховые и подмышечные ЛУ (в них чаще фиксируется инфекция, что может маскировать иные процессы; удаление подмышечного ЛУ технически сложнее, чем в других областях). Кроме того, удаление паховых или подмышечных ЛУ может в будущем спровоцировать лимфостаз конечности. Ткани следует препарировать бережно, не раздавливать. ЛУ необходимо убирать вместе с капсулой и небольшим объемом околоузловой клетчатки. Если в одном регионе изменены несколько ЛУ, то постараться взять не менее двух. Биоптат следует тут же доставлять в патологическую лабораторию. В крайнем случае его можно охладить или фиксировать. Если фиксации подвергается биоптат диаметром более 1,5 см или капсула удаленного ЛУ плотная, то ткань следует осторожно глубоко надрезать или разделить. В качестве фиксатора оптимальным является забуференный формалин. Соотношение ткань/фиксатор=1:10. Биопсии уступает аспирационная биопсия. Но современные методы тонкоигольной биопсии позволяют получить достоверные результаты.
Воспалительное увеличение ЛУ может быть локальным и генерализованным. Локальное увеличение отмечают при местных инфекционных процессах, откуда лимфа оттекает в ЛУ.
Увеличение ЛУ схематически можно представить как связанное с инфекцией (ЛА), так и не связанное с инфекцией (ЛАП). Для инфекционного ЛА типично одновременное увеличение селезенки.
- ЛА вирусной природы:
- цитомегалия;
- инфекционный мононуклеоз;
- корь;
- краснуха;
- синдром Ардмора. Инфекционное заболевание, вероятнее всего, вирусной природы. Пик заболеваемости отмечают осенью. Передается воздушнокапельным путем. Индекс контагиозности высокий, инкубационный период — 3–10 дней. Начинается с фарингита, ринита, субфебрилитета. Протекает с генерализованным увеличением ЛУ, болезненной увеличенной печенью (реже — спленомегалией), миалгией, болью в грудной клетке. Выздоровление без последствий.
- ЛА при бактериальных инфекциях:
- кариес;
- абсцесс;
- скарлатина;
- туляремия;
- болезнь кошачьей царапины (фелиноз). Вызывается Bartanella (Rochalimaea) henselae. Чаще доброкачественно протекающее со спонтанным выздоровлением двустороннее воспаление ЛУ (в том числе мезентериальных и внутригрудных) с общими и кожными неспецифическими симптомами, обусловленное ранениями кожи кошками, собаками, реже — посторонними острыми предметами. Следует подчеркнуть, что основным резервуаром инфекции являются все-таки домашние кошки. В одном из исследований антитела к В. henseltae выявлены в крови у 14–50% кошек. В другом исследовании в США среди всех кошек, доставленных их встревоженными хозяйками в ветеринарную лечебницу по поводу «дурного настроения» питомицы, у 41% животных выявлена бактериемия, хотя никаких других симптомов больше не было.
У заразившихся людей описаны гранулематозный гепатит, спленомегалия, энцефалитические реакции, судорожный синдром. Отмечают в основном у детей и подростков преимущественно поздней осенью и зимой.
Вообще же бартанеллы, ранее Rochalimaea, представляющие собой мелкие плохо окрашивающиеся грамнегативные бактерии, относятся к группе возбудителей риккетсиозов (см. главу 7) и вызывают острую лихорадку с анемией, хронические кожные сыпи или тяжелые общие поражения у иммуноскомпрометированных пациентов (табл. 5.1), где общим является и ЛАП:
- боррелиоз. Известен как псевдолимфома. Лимфопролиферативное поражение ЛУ и кожи при заражении Borrelia burgdorferi после укуса клеща. Описаны переходы в злокачественные лимфомы;
- туберкулез. Наряду с неспецифической инфекцией локальный и/или системный ЛА отмечают при туберкулезе. Ранее достаточно часто выявляли мико-бактериальное воспаление шейных и подчелюстных ЛУ с типичным исходом в звездчатый рубец. ЛУ при этом плотноэластической консистенции, кожа над ним не изменена. При неблагоприятном течении формируется «холодный абсцесс» со свищевым ходом, что вызывает сложности в ДД с актиномикозом. Последнему свойственна синюшная инфильтрация кожи. Микроскопическое и бактериологическое исследование отделяемого разрешает сомнения;
- сепсис;
- аллергический субсепсис. Рассматривают как вариант ювенильного РА;
- сифилис. Увеличение паховых ЛУ наряду с неспецифической флорой и опухолевой гиперплазией должно послужить причиной исключения сифилиса, учтенная заболеваемость которым выросла почти в 3 раза (с 32,6 до 86,1 на 100 000 населения);
- паховая лимфогранулема (болезнь Никола — Фавра). Вызывается некоторыми серовариантами хламидий. На фоне общего плохого состояния больного (повышение температуры, разбитость, снижение аппетита) паховые ЛУ (может быть одностороняя реакция) увеличиваются до 3 см в диаметре, кожа над ними становится синюшно-багровой. ЛУ часто расплавляются. У гомосексуалистов поражение прямой кишки приводит к ее стриктурам;
- генито-аноректальный симптомокомплекс. Состояние, видимо, близкое климфогранулеме Никола — Фавра. Представляет собой осложнение хронического ЛАпри хламидиозе серотипов L1–L2 с перипроктитом, хроническими рецидивирующими перианальными и промежностными свищами, стриктурами и фиброзом генитоуретрального тракта, элефантиазисом вульвы. Возникает в основном у женщин.
Таблица 5.1
Основные клинические характеристики бартонеллеза
| Болезнь | Возбудитель | Основные клинические проявления | Группа риска | Переносчик |
| Окопная лихорадка | Bartonella quintana | Постоянная или возвратная лихорадка (с интервалом 5–6 дней). Лихорадка, ЛАП, выраженная боль в спине и ногах, транзиторная макулезная или папулезная сыпь. Эпидемии — среди солдат Первой и Второй мировых войн. Спорадически — по всему миру. Эндемично — Мексика, Тунис, Эритрея, Польша, территория бывшего СССР, Монголия | Люди, проживающие скученно, в плохих гигиенических условиях | Платяная вошь |
| Болезнь кошачьей царапины | Bartonella nenselae | См. текст | Владельцы кошек | Блохи? |
| Перуанская лихорадка | Bartonella bacilliformis | На месте укуса комара появляется узелок 0,2–4 см в диаметре, болезненный (обычно — лицо, конечности, шея, живот). Без лечения сохраняется месяцы и годы. Сопровождается лихорадкой, болезненный. Кожные проявления напоминают саркому Калоши. Часто — вторичная инфекция. В острый лихорадочный период — гемолитическая тяжелая анемия (разрушаются до 90% эритроцитов) | Путешественники или постоянные жители Анд на уровне 600–2400 м над морем | Москит (Phlеbofomus) |
- ЛА при грибковых заболеваниях:
- гистоплазмоз. Заболевание человека и животных. Вызывается грибком Histoplasma capsulatum. При первичном легочном процессе характерно образование рассеянных очагов, увеличение прикорневых ЛУ. При хроническом легочном гистоплазмозе на рентгенограммах грудной клетки отмечают инфильтративные изменения в верхних долях, образования каверн и обызвествления прикорневых ЛУ. Диссеминированный гистоплазмоз — острое заболевание детей младшего возраста, лиц старческого возраста или пациентов с иммунодефицитом. Характеризуется тяжелым течением, острой лихорадкой, одышкой, кашлем, генерализованным увеличением периферических ЛУ. Смертность — высокая.
- ЛА при паразитарных заболеваниях:
- токсокароз;
- эхинококкоз;
- ЛА при протозойных инфекциях:
- токсоплазмоз. Субклинический вариант — шейный подострый некротизирующий ЛА. Клинически — болезненный, чаще шейный ЛА со спонтанной ремиссией через 3–6 мес, лихорадка, экзантема. Нейтропения. Гистологически — коагуляционные некрозы с гистиоцитарными и иммунобластными клетками без гранулем, без нейтрофильных гранулоцитов. ДД проводят со злокачественными лимфомами, туберкулезом, гистиоцитозом, а по данным гистологии (васкулит) — с СКВ;
- кала-азар;
- малярия.
Формы, не связанные с инфекцией (ЛАП).
- ЛАП медикаментозные:
- гидантоиновые производные. Медикаментозное увеличение ЛУ при применении дифенина и других противосудорожных препаратов этой группы часто сочетается с мегалобластной анемией и тромбоцитопенией. Это представляет сложности в ДД с лимфомами. После отмены лекарственных средств размеры ЛУ возвращаются к норме;
- аллопуринол (применяют при лечении пациентов с гиперурекемий, в том числе при миелопролиферативных заболеваниях);
- противолепрозные средства (применяют в гастроэнтерологии для лечения пациентов с хроническим колитом, в ревматологии — при артрите и спондилоартрите, особенно ассоциированных с HLA В-27;
- поствакцинальные;
- на фоне инородных тел (в том числе тальк, кремний и другие отходы производств).
- Гранулематозы:
- саркоидоз (болезнь Бека). Заболевание с недостаточно выясненными этиологией и патогенезом, может протекать с увеличением всех групп ЛУ и селезенки, в большинстве случаев не выходящей за реберную дугу более чем на 3–4 см. Типичным является изменение ЛУ ворот легких. Размер узлов обычно не превышает 3–4 см. Диагностически значимым представляется увеличение кубитальных ЛУ;
- аллергический гранулематоз Чарга — Штраусса. Сочетается с атопией в анамнезе. Проявляется как БА, выраженная эозинофилия, ЛАП, нейропатия, кожные язвы, поражения сердца, легких, кишечника и васкулита мелких артерий и вен;
- мультицентрический ретикулогистиоцитоз. Системное гранулематозное заболевание с образованием кожных узлов, деструктивным артритом, поражением внутренних органов. Протекает по типу псориатической артропатии;
- ретикулез липомеланотический (синдром Паутриера — Ворингера). Локализованное или генерализованное увеличение ЛУ как сопровождение дерматозов, прежде всего меланоэритродермии.
- ЛАП при метастазировании солидных опухолей в ЛУ.
Выявляя увеличение ЛУ, следует, исключив инфекцию, помнить об опухолевой природе их гиперплазии. Локальное увеличение ЛУ типично для метастазирующих опухолей. Например, патогномоничным для метастаз при раке желудка является увеличение надключичного ЛУ слева.
Об онкогематологическом генезе изменения ЛУ свидетельствует увеличение их диаметра до 4 см и более, каменистая плотность, бугристость, спаянность с окружающими тканями, внутригрудные конгломераты, особенно в верхнем средостении, внутрибрюшинные конгломераты.
- ЛАП при гемобластозах:
- болезнь Ходжкина (ходжкинская лимфома, лимфогранулематоз). Классикой гистологической диагностики является определение гигантских клеток Березовского — Штернберга и клеток Ходжкина. Возрастные пики заболеваемости отмечают в 15–30 и старше 50 лет. Мужчины заболевают чаше. Возможен медленный вариант развития, когда без общих симптомов интоксикации пациент чаще случайно выявляет увеличение ЛУ какой-либо одной группы. Кожа над ними не изменена, узлы плотные, безболезненные, подвижные. Реже первично поражаются внутригрудные и паховые ЛУ. В других случаях увеличению ЛУ предшествет высокая температура, ночное потение, зуд, исхудание. При этом поражаются сразу несколько групп ЛУ, в том числе внутрибрюшные или медиастинальные. Увеличивается печень и селезенка. Лимфогранулематоз — одна из очень редких опухолей, метастазирующих в селезенку. При эхоГ метастазы выглядят как округлые эхонегативные образования, селезенка напоминает «простреленный орган». Эта находка является достаточно патогномоничной для лимфогранулематоза (рис. 5.2). Однако такую же картину эхоГ «мишеневидной» селезенки отмечали у детей с хронической гранулематозной болезнью.
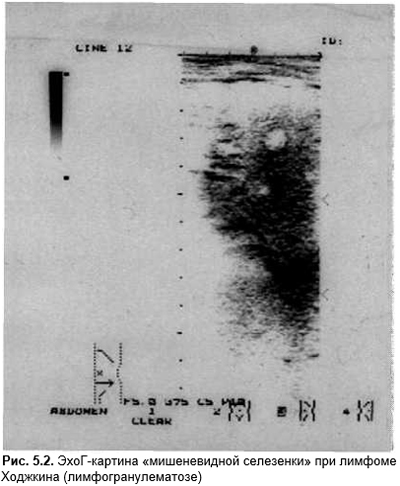
Прогностически неблагоприятно слияние метастазов и деформация селезенки. В поздних стадиях присоединяется боль в костях. На начальных этапах лабораторные признаки минимальны и неспецифичны, позднее — эозинофилия, анемия, лимфопения, резко повышенная СОЭ. Прогностически неблагоприятным является расширение средостения, когда оно при передне-задних рентгеновских снимках занимает более 1/3 поперечника грудной клетки. Для установления полноценного диагноза, определяющего терапевтическую тактику, необходима биопсия ЛУ и оценка стадийности процесса;
- неходжкинские лимфомы (лимфосаркомы) — группа опухолей лимфатической системы разной степени злокачественности, но с общей симптоматикой. Происходят из клона лимфоидных клеток-предшественников различной гистогенетической принадлежности и степени дифференцировки. Неходжкинские лимфомы могут быть В- и Т-клеточными. Становление В-клеточных лимфом возможно на фоне поликлональной В-клеточной гиперплазии. В онтогенезе доказано участие вируса Эпштейна — Барр, обладающего тропизмом к В-клеткам. В-клеточные неходжкинские лимфомы развиваются преимущественно в лимфоидных образованиях кишечника, кольца Вальдейера, реже — в периферических ЛУ, в тканях глазницы, мозговых оболочках. В развитии Т-клеточных неходжкинских лимфом значение вирусов и иммунодефицитных состояний не доказано. Риск их развития повышен при аутоиммунных заболеваниях.
Если раньше неходжкинские лимфомы вывляли у людей в основном зрелого возраста, а у молодых лимфома развивалась на фоне иммунодепрессивных состояний, то в современных условиях повышается заболеваемость детей, составляя 9:1 млн детского населения. ЛУ мягкие, безболезненные, но при быстром росте могут становиться болезненными. Возможны конгломераты. Инициальное поражение периферических ЛУ отмечают при неходжкинских лимфомах только в 12% случаев. Гораздо чаще процесс дебютирует с поражения лимфоидной ткани брюшной полости (35%), переднего средостения (27%). Даже если увеличена только одна группа ЛУ, заболевание рассматривают как первично генерализованное. Граница между лимфомами и лейкозами до некоторой степени условна. Например, если в костном мозгу выявляют более 25% бластных клеток, то лимфому рассматривают как лейкоз и лечат соответственно;
- в особую группу, не всеми принимаемую, выделяют ангиоиммунобластную ЛАП. Проявляется общим плохим состоянием, лихорадкой, генерализованной ЛАП, гепатоспленомегалией. По анализу крови определяют поликлональную гипергаммаглобулинемию, гемолитическую кумбс-положительную анемию. Гистологически типичны пролиферация венул, инфильтрация лимфоцитами, плазматическими клетками и иммунобластами. ДД проводят со злокачественными лимфомами, в которые на поздней стадии ангиоиммунобластная ЛАП достаточно часто и трансформируется;
- генерализованное увеличение ЛУ при лейкозах описано ниже (см. Спленомегалия);
- болезнь гамма-тяжелых цепей. Обусловлена моноклональной гаммапатией. Протекает по типу лимфопролиферативного системного заболевания;
- болезнь альфа-тяжелых цепей (средиземноморская лимфома). Отмечают в основном в детском и юношеском возрасте. Клиника обусловлена тяжелым синдромом мальабсорбции, являющимся результатом лимфопролиферативных процессов с инфильтрацией тонкой кишки и мезентериальной ЛАП;
- гистиоцитарные синдромы.
- Паранеопластические реакции:
- ПОЭМК-комплекс. Паранеопластический симптомокомплекс (особенно часто при склерозирующих плазмоцитомах) = полинейропатия + ор- ганомегалия + эндокринопатия + дисглобулинемия (М-градиент) + поражение кожи.
- ЛАП при системных процессах в организме:
- коллагенозы. В этом случае наибольшее увеличение ЛУ регистрируют все-таки при инфицированных вариантах диффузных болезней соединительной ткани, то есть при сочетании ЛА и ЛАП;
- локальный опухолевидный амилоидоз. Протекает с общей параспецифической реакцией. На 52 случая системного амилоидоза у детей нами отмечен локальный опухолевидный амилоидоз у 2. У лиц старческого возраста локальный опухолевидный амилоидоз выявляют чаще, он не сопровождается бурной общей реакцией;
- амилоидоз Любарха. Генетически детерминированный. Генерализованная ЛАП, ортостатическая гипотония, обструктивная инфильтративная кардиомиопатия, спленомегалия, нейропатия, туннельный синдром;
- синдром Дорфмана — Розаи (интермиттирующая доброкачественная ЛАП). Вероятно, аутоиммунное заболевание с доброкачественной пролиферацией плазмоцитов, гистиоцитов, фибробластов. Пик заболеваемости — в первые 10 лет жизни. Протекает с двусторонним шейным, часто генерализованным увеличением ЛУ, лихорадкой, лейкоцитозом, узловатой эритемой. По нашим наблюдениям, при поражениях внутренних органов прогноз плохой. Прогноз ухудшается при наличии одновременно иммунодисфункции (повышение СОЭ, диспротеинемия);
- десквамативная эритродермия Лейнера. Вероятнее всего, дефект хемотаксиса лейкоцитов и дефицит фрагмента комплемента С5. Заболевание манифестирует в первые 3–4 мес жизни. Проявляется генерализованным увеличением всех ЛУ, вторичной эритродермией, дистрофией ногтей, анемией, рвотой, диарей. Чаще возникает при грудном вскармливании. Известны семейные случаи. Прогноз благоприятен.
- ЛАП при первичных иммунодефицитных состояниях:
- общая вариабельная иммунная недостаточность;
- аутоиммунный лимфопролиферативный синдром;
- гранулематоз септический. Гетерогенная группа дефектов иммунитета, объединенных незавершенным внутриклеточным фагоцитозом каталазопозитивных микробов в результате дефицита перекиси водорода и атомарного кислорода. В настоящее время известны 4 различных молекулярных дефекта:
1) Х-хромосомно связанный рецессивный дефект тяжелых цепей цитохрома В558;
2) а/p наследуемый дефект легких цепей цитохрома В558;
3) дефект 47 kd цитозолфактора;
4) дефект 65 kd цитозолфактора.
Клинические признаки: острые абсцедирующие инфекции кожи, легких, желудочно-кишечного тракта, ЛУ, печени, селезенки, обусловленные каталазопозитивными бактериями (стафилококки, энтеробактерии), а также аспергиллами; хроническое гранулематозное воспаление в желудочно-кишечном тракте и мочевыводящих путях с возможным стенозированием; уменьшение образования атомарного кислорода и перекиси водорода в ответ на растворимые и опсонированные раздражители.
- Генетически обусловленные ЛАП:
- синдром Клиппеля — Треноне. Сочетание локальных лимфангиом и гемангиом;
- синдромы с наследственно обусловленными лимфатическими отеками (Вевера — Смита и Мильроя);
- легочная мышечная гипертрофия — мышечный цирроз легкого. Разрастание гладкомышечных волокон периальвеолярно, перибронхиально, интерстициально, интерлобарно. Увеличение ворот легких.
- Синдром приобретенного иммунодефицита.